扩散微分方程主要研究了有浓度梯度的扩散现象,尤其是物质从高浓度向低浓度的扩散。实际上,物质也可以从低浓度向高浓度扩散,比如日常生活中,我们把一杯泥浆静置一段时间后,杯底会有很多沉淀的泥,而上面部分的水中有很少的泥颗粒。同样,我们把花生米和未剥壳的花生混在一个容器中,抖动容器。我们会发现花生米集中在下部分、未剥壳的花生集中在容器的上部。在材料领域,晶界容易吸附杂质原子,使晶界能降低。这样,杂质原子在晶界处的浓度会增加。这些是有浓度梯度的扩散。没有浓度梯度,物质中原子在热运动等作用下也可以扩散,即自扩散。这些现象表明物质的浓度梯度并不是扩散的必要条件。物质究竟是在什么样的驱动力下产生扩散的呢?根据热力学原理,我们知道一个物理化学过程是否能自动进行,常用Gibbs自由能的变化dG是否小于零来判别:
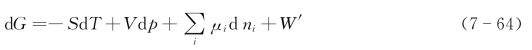
式中,S为熵;T为热力学温度;V为体积;p为压强;μi为i物质的化学势;ni为i的物质的量;W′为其他功。当恒温、恒压,其他功为0时,有

其中,化学势μi表示在恒温、恒压、其他功为0及其他组元不变时,i组元增加或减少1 mol引起的Gibbs自由能变化。dG<0,则物理化学过程(如扩散)可自发进行。
以图7.8为例,假设i物质从A向B扩散。在恒温、恒压、其他功为0的条件下,A中有极微量的i转移到B中。转移后,A中i的物质的量之增量为![]() ,即A中i的物质的量减少了-
,即A中i的物质的量减少了-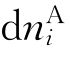 。这样,A、B组成的系统中,Gibbs自由能的变化为
。这样,A、B组成的系统中,Gibbs自由能的变化为
![]()
因为A所失去的i的物质的量即是B所获得的i的物质的量,故-![]() ,代入式(7-66)得(https://www.daowen.com)
,代入式(7-66)得(https://www.daowen.com)
![]()
扩散过程达到平衡时,dG=0;若扩散要自发进行,dG<0,即
![]()
因为![]() <0,故要使dG≤0,则
<0,故要使dG≤0,则
![]()
式(7-69)表明,要使i从A向B扩散,则i在A中的化学势大于其在B中的化学势,即化学势梯度∂μ/∂x>0。当i在A、B中的化学势梯度∂μ/∂x=0,i在A、B间的净扩散为零。
由以上分析,我们知道:物质扩散的驱动力为化学势梯度∂μ/∂x;物质是从高化学势之处流向低化学势之处。了解了扩散驱动力后,我们来看看多元系统中的扩散。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。







