镍氢(MH-Ni)电池是在Ni-Cd电池的基础上发展起来的,相对于镍镉电池,其最大的优点是环境友好,不存在重金属污染。民用镍氢电池又是以航天用高压镍氢电池为基础,由于高压镍氢电池采用高压氢,而且还需要用贵金属作催化剂,这就很难为民用所接受。自20世纪70年代中期,研究者开始探索民用的低压氢镍电池。镍氢电池于1988年进入实用化阶段,1990年在日本开始规模生产。
目前,以储氢合金为负极材料的镍氢电池能满足混合动力电动汽车所要求的高能量、高功率、长寿命和足够宽的工作温度范围要求,成为电动汽车动力电池市场的主流产品,同时该类电池也已经广泛地应用在电子工具、电动自行车等日常生活用品上。
1.镍氢电池结构
镍氢电池由如图3-31所示的几个部分构成,包括以镍的储氢合金为主要材料的负极板、具有保液能力和良好透气性的隔膜、碱性电解液、金属壳体、具有自动密封功能的安全阀及其他部件。图示的圆柱形电池,采用被隔膜相互隔离开的正、负极板,它们呈螺旋状卷绕在壳体内,壳体用盖帽进行密封,在壳体和盖帽之间用绝缘材质的密封圈隔开。
作为镍氢电池负极板的储氢合金,顾名思义就是可以储存氢气的合金。氢是化学周期表内最小、最活泼的元素,不同的金属元素与氢有着不同的亲和力,将与氢之间有强亲和力的A金属元素与另一与氢有弱亲和力的B金属元素依一定比例熔成AxBy合金,若AxBy合金内A原子与B原子排列得非常规则,且介于A原子与B原子间的空隙也排列得很规则,则这些空隙很容易让氢原子进出。当氢原子进入后形成AxByHz的三元合金,也就是AxBy的氢化物,此AxBy合金(主要包括AB、A2B、AB2、AB3、AB5、A2B7)即称为储氢合金。
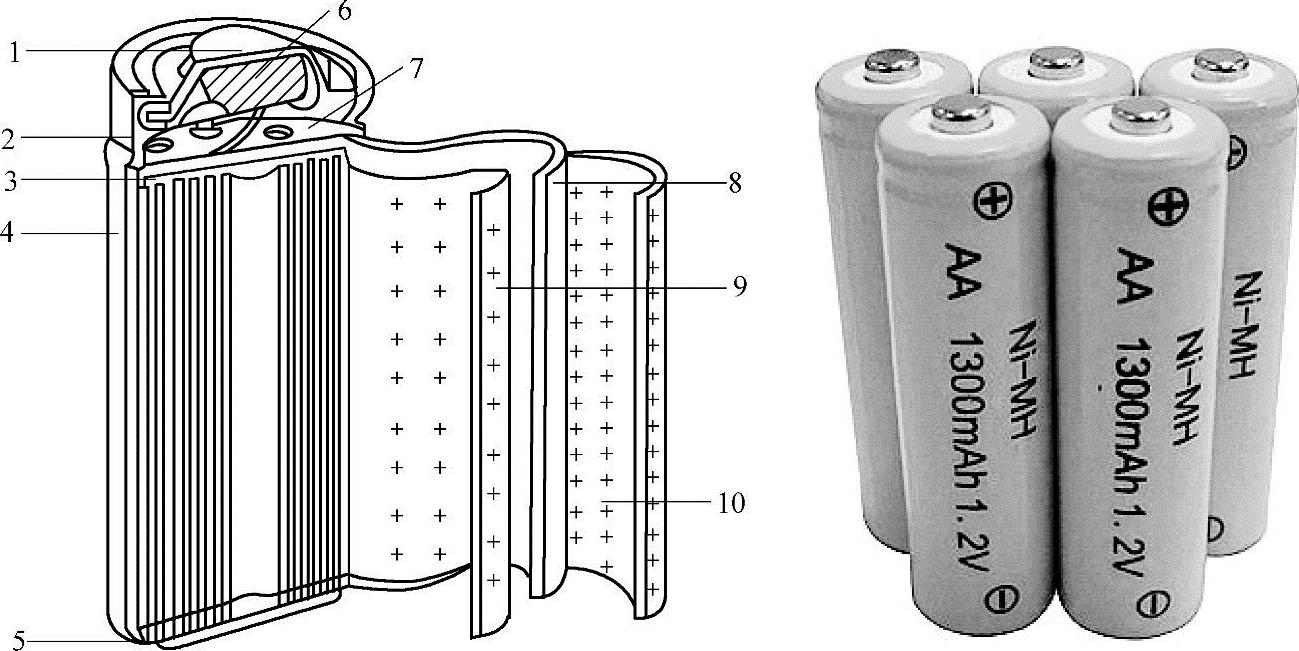
图3-31 镍氢电池结构及外形
1—正极盖帽(+) 2—胶圈 3—集流体 4—电池钢壳(-) 5—底部绝缘片 6—安全防爆孔 7—顶部绝缘片 8—隔膜纸 9—镍正极片 10—金属氢化物负极片
储氢合金在进行吸氢/放氢化学反应(可逆反应)的过程中,也伴随着放热/吸热的热反应(可逆反应),同时也产生充电/放电的电化学反应(可逆反应)。具有实用价值的储氢合金应该具有储氢量大、容易活化、吸氢/放氢的化学反应速率快、使用寿命长及成本低廉等特性。目前常见的储氢合金主要为AB5型(如NaNi5、CaNi5)、AB2型(如MgZn2、ZrNi2)、AB型(如TiNi、TiFe)、A2B型(如Mg2Ni、Ca2Fe)几种。
2.镍氢电池工作原理
镍氢电池正极的活性物质为NiOOH(放电时)和Ni(OH)2(充电时),负极板的活性物质为H2(放电时)和H2O(充电时),电解液采用30%的氢氧化钾溶液,电化学反应如下:
负极反应式 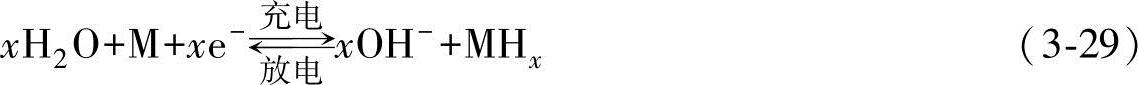 (https://www.daowen.com)
(https://www.daowen.com)
正极反应式 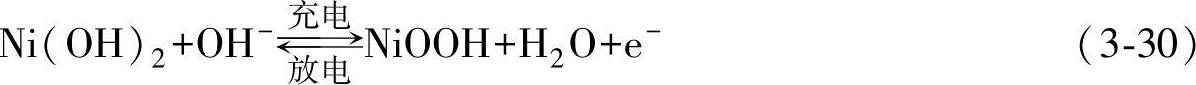
电池反应式 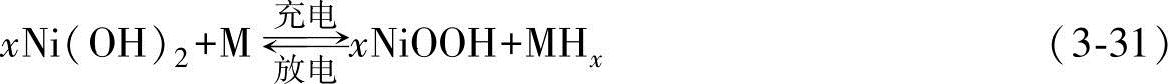
从反应式也可以看出,镍氢电池的反应与镍镉电池相似,只是负极充、放电过程中生成物不同。从反应式也可以看出,镍氢电池在充、放电过程中,正、负极上在进行电化学反应时不生成任何中间态的可溶性金属离子,也没有电解液中的任何组分消耗和生成,因而镍氢电池可以做成密封型结构。镍氢电池的电解液多采用KOH水溶液,并加入少量的LiOH。隔膜采用多孔维尼龙无纺布或尼龙无纺布等。
为了防止充电过程后期电池内压过高,电池中装有防爆装置。圆柱形密封镍氢电池的结构如图3-31所示。当镍氢电池过充电时,金属壳内的气体压力将逐渐上升。当该压力达到一定数值后,顶盖上的限压安全排气孔打开,因此,可以避免电池因气体压力过大而爆炸。
镍氢电池放电时,正极上NiOOH得到电子还原成为Ni(OH)2,负极金属氢化物(MHx)内部的氢原子扩散到表面形成吸附态氢原子,接着再发生电化学反应生成水和储氢合金。在镍氢电池出现过放电时,正极活性物质中的NiOOH已经消耗完了,这时正极上的水分子被还原为氢和OH-离子。负极上由于储氢合金的催化作用,使OH-离子与氢反应又生成水。
过充电时,正极上会析出氧,然后扩散到负极上发生去极化反应,生成OH-离子。在电池过充电和过放电过程中,正、负极上发生的反应可用下式表示
正极:过充电析出氧 4OH-→O2+2H2O+4e- (3-32)
过放电析出氢 2H2O+2e-→2OH-+H2 (3-33)
负极:过充电消耗氧 2H2O+O2+4e-→4OH- (3-34)
过放电消耗氢 H2+2OH-→2H2O+2e- (3-35)
由此可知,储氢合金既承担着储氢的作用,又起到催化剂作用,在电池出现过充和过放电时,可以消除由正极产生的O2和H2。从而使电池具有耐过充电、过放电的能力。但随着充放电循环的进行,储氢合金的催化能力逐渐退化,电池的内压就会上升,最终导致电池漏液失效。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。








