以往材料的生产大多靠工人师傅的经验。今天,材料的制备是在实践经验的基础上,结合一定的理论指导生产出来的。其中,相图在寻找材料合理组成、选择合成温度范围、改进配方,以及指导生产工艺方面起着非常重要的作用。这一点,我们在前面两个专业相图中已做了一些说明。也许你会说普通水泥、传统陶瓷以前就有了,可以根据经验制备,事实的确如此。然而,我们要制备以前没有的新材料,此时没有经验可循。如果没有相图,要想获得它的配方和烧成温度,我们需要在盲目的摸索中做无数的实验,而且还不一定成功。
如今,材料的配料有许多三元相图可用。除了前文的![]() SiO2相图外,Na2O-CaO-SiO2相图的富钙部分也常用于指导钠钙硅酸盐玻璃的生产。MgO-
SiO2相图外,Na2O-CaO-SiO2相图的富钙部分也常用于指导钠钙硅酸盐玻璃的生产。MgO-![]() 相图可用于指导镁质瓷的生产(镁质瓷是一种无线电高频瓷)。骨灰瓷的生产可利用
相图可用于指导镁质瓷的生产(镁质瓷是一种无线电高频瓷)。骨灰瓷的生产可利用![]() 相图(CaO·Al2O3·2SiO2为钙长石CaAl2Si2O8)。从以往的实验和生产数据来看,许多产品的组成在这些相图上有一个大致的范围,故相图可作为配方的一个依据。图8.101示意了
相图(CaO·Al2O3·2SiO2为钙长石CaAl2Si2O8)。从以往的实验和生产数据来看,许多产品的组成在这些相图上有一个大致的范围,故相图可作为配方的一个依据。图8.101示意了![]() 相图中不同种类材料的组成区域。图8.102从配方的角度示意了一些陶瓷品种的配方范围。但是,我们在配料时,原料不是纯物质,它们除了含有某种相图对应的物质外,往往还有其他成分。比如,我们采用
相图中不同种类材料的组成区域。图8.102从配方的角度示意了一些陶瓷品种的配方范围。但是,我们在配料时,原料不是纯物质,它们除了含有某种相图对应的物质外,往往还有其他成分。比如,我们采用![]() SiO2相图进行陶瓷的配料,原料除了有K2O、Al2O3、SiO2外还有Na2O、TiO2、CaO、Fe2O3等。这样我们在配料时就不能直接采用
SiO2相图进行陶瓷的配料,原料除了有K2O、Al2O3、SiO2外还有Na2O、TiO2、CaO、Fe2O3等。这样我们在配料时就不能直接采用![]() 相图。然而,三元相图比四元、五元等相图相对简单。因此,我们往往将这些在三元相图中没有的物质转换成相图中的某些物质,以此来简化配料。在利用
相图。然而,三元相图比四元、五元等相图相对简单。因此,我们往往将这些在三元相图中没有的物质转换成相图中的某些物质,以此来简化配料。在利用![]() 相图配料时,人们常将碱性氧化物(如Na2O、CaO、MgO)转换成K2O来计算;Fe2O3转换成Al2O3;TiO2转换成SiO2。
相图配料时,人们常将碱性氧化物(如Na2O、CaO、MgO)转换成K2O来计算;Fe2O3转换成Al2O3;TiO2转换成SiO2。
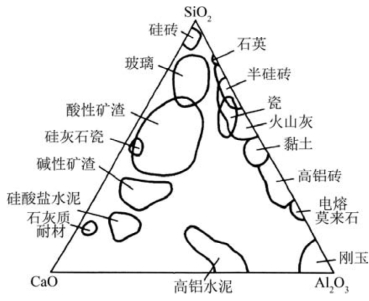
图8.101 CaO-Al2O3-SiO2相图中各材料的组成范围(引自宋晓岚,2006)
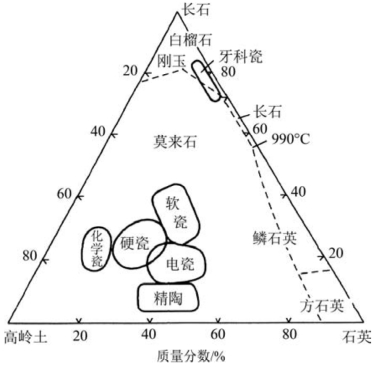
图8.102 以高岭土、长石和石英为原料的瓷料配方范围(引自宋晓岚,2006)
这些物质间的转换依据是Richters近似原则。K2O的“分子量”为94,Na2O的“分子量”为62,则每份Na2O相当于K2O的量为94/62=1.52,1.52就为Na2O转换为K2O的系数。CaO、MgO转换成K2O的系数分别是94/56=1.68,94/40=2.35。同理,Fe2O3转换成Al2O3的系数为101/159.7=0.64,TiO2转换为SiO2的系数为60/79.9=0.75。以上转换系数也叫Richters系数。
例8.2 采用下表中的原料配成某成分的瓷器,试计算各原料的质量分数。瓷器各成分的质量分数为K2O(4.5%)、Al2O3(26.2%)、SiO2(69.3%)。表中数据为质量分数(单位:%)。
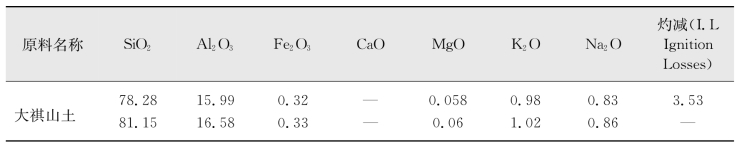
续表
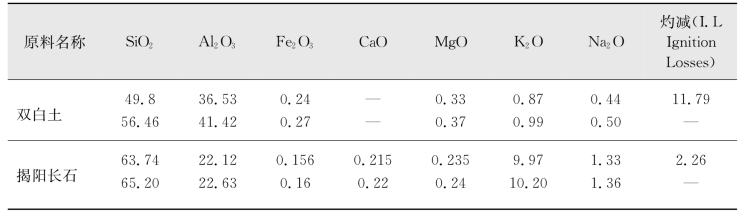
1.成分转换
首先将含有灼减的原料质量分数换算成不含灼减的质量分数(见上表),然后利用转换系数换算相应的氧化物。
以不含灼减的大祺山土为例。取100 g不含灼减的该原料作计算基准,其中SiO2有81.15 g,但没有TiO2。
Al2O3有16.58 g。根据Richters系数,Fe2O3转换成Al2O3的系数为101/159.7=0.64,故0.33 g Fe2O3转换成Al2O3后有0.33×0.64=0.2112(g)。这样,Al2O3的总质量为16.58+0.2112=16.7912(g)。
K2O的质量为1.02 g。CaO、MgO、Na2O转换为K2O后的质量分别为0、0.06×2.35=0.141(g)、0.86×1.52=1.3072(g),故K2O的总质量为2.4682 g。
这样,只含Al2O3、K2O和SiO2的原料总质量为81.15+16.7912+2.4682=100.4094(g)。转换以后,SiO2的质量分数为81.15/100.4094=80.82%;Al2O3的质量分数为16.7912/100.4094=16.72%;K2O的质量分数为2.4682/100.4094=2.46%。
其他两种原料的转换与此相同,结果见下表。
2.在相图中表示出原料和瓷的成分点
将上述原料的成分点和瓷的成分点表示在K2O-Al2O3-SiO2相图中。图8.103仅示意了A、B、C和D的位置,D点为产品瓷的成分点,连接A、D并延长与BC交于R,然后量出各线段的长(当然,连接C、D或B、D也可)。(https://www.daowen.com)
3.按照杠杆原理算出无灼减原料的配比
大祺山土:A′=DR/AR;双白土:B′=(CR/BC)×(AD/AR);揭阳长石:C′=(BR/BC)×(AD/AR)。
4.将无灼减的原料配比换算为有灼减的原料配比
大祺山土A″=[A′/(1-0.0353)];双白土B″=[B′/(1-0.1179)];揭阳长石C″=[C′/(1-0.0223)]。
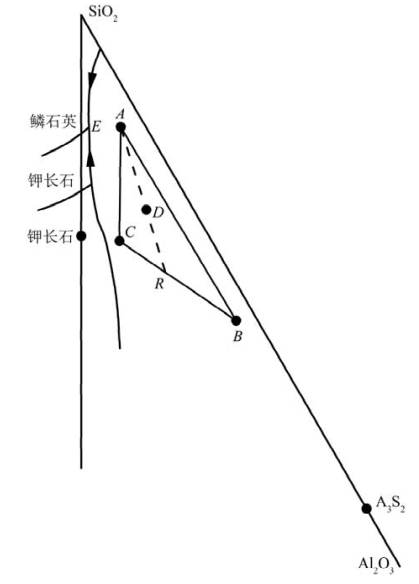
图8.103 利用K2O-Al2O3-SiO2相图进行配方计算示意图(引自刘康时,1990)
结果,有灼减的原料配比为
大祺山土A%=[A″/(A″+B″+C″)]×100%;双白土B%=[B″/(A″+B″+C″)]×100%;揭阳长石C%=[C″/(A″+B″+C″)]×100%。
据此,我们可根据产品瓷与原料成分点的相对位置做一些判断。若瓷的成分点D在原料成分点组成的△ABC之外,则至少需要更换一种原料,否则无法配出符合要求的配方。如果D点在△ABC的某一条边上,则只用相应的两种原料即可满足要求。比如,D点在AB边上,则只需A、B两种原料就可配出相应成分的瓷器,而无需原料C。若D点和△ABC的某一顶点很靠近,甚至重合,则只需要一种原料即可。
以上是由三种原料利用相图进行配方的计算方法。若采用四种或更多种原料,则可把其中某两种原料或某些原料的比例加以固定。这样,我们可使这些有固定比例的原料在相图中成为一个组成点,然后再按上述方法进行计算。最后,再根据先前的比例得出各原料的配比。
利用相图来配方有一定误差。这是由于转换系数是近似的、转化物质的作用与实际有出入,作图和线段测量的不精确。尽管如此,通过相图配方,我们可以找到一个大致的配方范围。然后,我们可通过进一步的实验,甚至中试对最后的配方加以确定。其实,确定配方有很多方法,相图的利用仅是其中一种。其他配方法,读者将在工艺课中学习。
本章结语
本章介绍了单元、二元和三元相图的一些基本理论。通过分析这些相图,我们可知在相平衡条件下,材料中各相间的平衡关系。根据平衡关系,我们可了解材料的显微结构可能是由哪些相构成的,进而预测材料的性能。
读者在分析具体相图时,首先要注意其中的点、线和区域的意义。在三元投影状态相图中,还应划分副三角形将相图简化,并利用连线和切线规则判断界线温度高低和液相在界线上发生共晶还是包晶反应。然后,对某一组成的系统做平衡结晶分析,以此获得平衡条件下的相。要想获得某些平衡相的相对量,则需杠杆规则的帮助。
相图反映的是平衡态时的情形。实际上,材料的制备工艺常使系统处于非平衡态。尽管如此,相图还是可以为某些相的稳定存在的条件指明方向。简言之,相图在新材料的获得、材料的显微结构的形成、材料的配方及工艺制定等方面有着重要的指导意义。
推荐读物
[1]赵慕愚,肖良质.不求闻达、惟求真知的一生——美国物理学家吉布斯传略[J].自然杂志,1985,8(6):466-468.
[2]费一汀,范世骥,孙仁英,等.Bi2O3-SiO2系统相图的研究[J].无机材料学报,1998,13(6):798-802.
[3]苏海军,张军,刘林,等.定向凝固Al2O3/YAG共晶自生复合材料的组织形态及非规则共晶生长[J].金属学报,2008,44(4):457-462.
[4]Huahai Mao,Mats Hillert,Malin Selleby,et al.Thermodynamic assessment of the CaO-Al2O3-SiO2system[J].Journal of the American Ceramic Society,2006,89(1):298-308.
[5]杨增朝,刘光华,徐利华,等.超重力熔铸Y2O3-Al2O3-SiO2玻璃的晶化行为研究[J].无机材料学报,2013,28(7):780-784.
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。






