基因工程两件宝
基因工程两件宝
基因工程所实际进行的就是DNA的剪裁、缝合等基本过程,而要完成这些过程,需要如下两件法宝。
限制性内切酶
进行基因工程,首先就要设法得到我们所需要的基因——目的基因。一个基因在一般物种的DNA大分子中只占其中的一小段,那么用什么手段才能把这个基因从DNA分子中剪裁下来呢?科学家们想到,只要找到一把合适的剪裁工具,就可解决问题。幸运的是,生物本身已为我们准备了这个工具,这就是“分子剪刀”——限制性(核酸)内切酶。
原来人们发现,大肠杆菌的死敌——噬菌体在感染大肠杆菌的菌株K时,可使菌株K全军覆没,即被噬菌体裂解破坏,但在感染大肠杆菌的菌株B时,菌株B却平安无事。后来才知道,这是因为大肠杆菌的菌株B中存在一种酶,能识别噬菌体DNA的某一特定位点,并在这一位点上把DNA的磷酸二酯键“剪断”,以限制噬菌体对菌株B的侵略活动。因此,这种酶就叫限制性(核酸)内切酶。
限制性内切酶的来源广泛,几乎在所有的原核生物中都能找到。限制性内切酶的命名有一定规则:每一种酶的第一个大写字母代表产生该酶的菌属,是拉丁菌属名称的第一字母;接着的两个小写字母代表产生这种内切酶的菌种,是拉丁菌种名称的前两个字母;如果内切酶是由特殊菌株产生的,酶的第四个字母以拉丁菌株的第一个字母表示;内切酶最后的罗马数字表明在这一菌属或特殊菌株中发现该酶的顺序。例如,从大肠埃希氏菌(Escherichia coli)的Ry13菌株中发现的第一种限制性内切酶命名为EcoRⅠ。
一定的限制性内切酶只能识别DNA分子上一定的核苷酸序列,并在该序列两个特定碱基间“剪断”其磷酸二酯键,从而使DNA分子的双链能交错地断开。例如,EcoRⅠ限制性内切酶只能识别DNA分子中如下6对核苷酸序列,并在A和G间“剪断”磷酸二酯键:
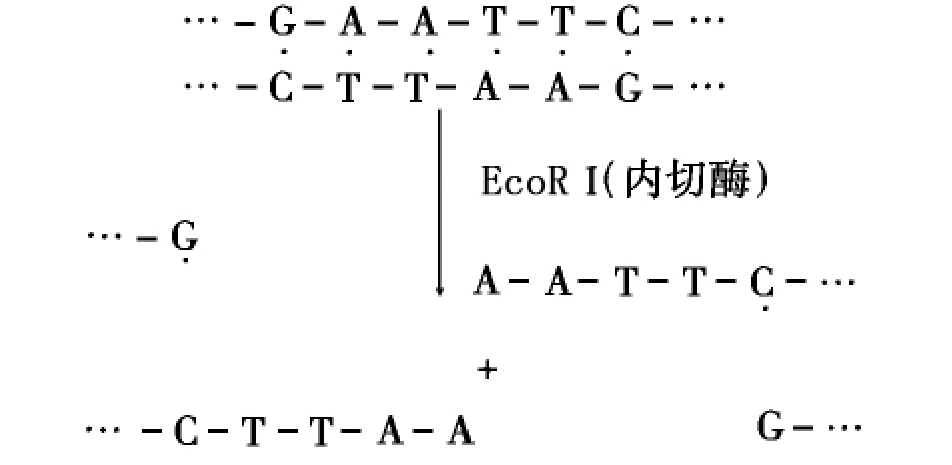
不难想象,当用同一种限制性核酸内切酶来剪裁不同的DNA分子时,它们都将产生核苷酸顺序的碱基恰好互补的单链尾巴(如上述内切酶剪切:DNA得到的两个单链尾巴A-A-T-T-和-T-T-A-A恰好互补)。把它们混合在一起时,来自不同分子的单链尾巴就会根据碱基互补原则,“粘”在一起而构成杂种(重组)DNA分子,因此,这种单链尾巴就叫黏性末端。(https://www.daowen.com)
也许要问:既然生物体内存在着限制性核酸内切酶,那么它自己的DNA链为什么会被剪断呢?原来它还有一种修饰酶,能使自身DNA链中可为限制性核酸内切酶识别的核苷酸序列部分甲基化,即其中有1~2个碱基上的氢原子被甲基(CH3)取代。这个序列由于戴上了甲基的防护“头盔”,就使内切酶不能识别它而被保护起来。
目前人们已在不同生物中找到200余种的“分子剪刀”——限制性核酸内切酶。由于有了种类繁多的“分子剪刀”,人们就可几乎随心所欲地对不同的DNA分子长链进行剪裁了。
DNA连接酶
得到目的基因之后,接下来就要使这一基因与基因的运载体连接起来,如何安全地运到寄主细胞。因为当外源目的基因赤裸裸地进入寄主细胞时,往往会被寄主的限制性核酸内切酶破坏。
对运载体有如下要求:体积要小,这样可使它轻松自如地进入寄主细胞;运载目的基因至宿主细胞时,仍有自我复制能力,借此可繁殖目的基因。
经科学家的努力,已经找到了几种符合上述要求的运载体。一种是细菌的质粒,它是细菌中(环状)染色体外的一种较小的环状DNA分子(质粒DNA),能自由出入细菌,而且当用限制性内切酶把它剪开,再装上一段目的基因(DNA片断)后,依然能自我复制。符合上述要求的还有λ噬菌体,它也是可进入细菌的较理想的运载体。病毒也是可进入动物细胞的较理想运载体,根瘤杆菌的诱导瘤质粒,则是进入植物细胞的较理想的运载体。
有了适当的运载体后,就要用与剪裁目的基因相同的限制性核酸内切酶,去剪裁载运体,使之产生与目的基因相同的黏性末端。当这两种不同来源但是有相同黏性末端的DNA相遇时,由于它们的碱基互补,互补碱基间就会形成氢键。每条DNA长链原来被剪断的磷酸二酯键的缺口,会被专门缝合这个缺口的针线——DNA连接酶缝合。于是,目的基因与运载体就这样重组起来了。
有了这两大法宝后,就可进行基因工程的操作了。
