2.4.7 重组DNA技术
1978年12月与阿尔伯和史密斯一起分享诺贝尔奖的还有一个科学家内森斯(D.Nathans)。他也是约翰·霍普金斯大学的生物化学教授。就在史密斯阐明HindⅡ的特异性切割序列之后,内森斯就把限制性内切酶应用于分子生物学的研究了。他和年轻的研究生达纳(K.Danna)一起以猴病毒SV40作为内切酶的作用靶分子,以SV40对寄主细胞的转化活性作为检测酶处理前后SV40 DNA生物学功能的指标,系统地研究了各种内切酶对DNA分子结构和功能的影响。他们先用限制性内切酶处理过的标记SV40 DNA在聚丙烯酰胺凝胶做电泳分析,然后降温冻结使凝胶变硬以便操作。再用小刀把凝胶切成宽度为1.2 mum的100条凝胶小条带,依次测定每个小带的放射活性,最后做出放射活性分布图。他们发现处理前呈现一个浓度峰的SV40 DNA在处理后出现了11个浓度峰,如果把11个峰值出现区的DNA小片段的分子量累加起来,其总和则等于切割前整个SV40 DNA的分子量。内森斯和达纳的结论是“这种内切酶把每SV40 DNA分子切成了11段,DNA分子被切割后所产生的11种大小不等的片段会在凝胶的一定位置聚集为11条电泳带,各个电泳带的位置取决于相应的DNA片段的分子量”。此后,他们又用不同的内切酶处理SV40 DNA,获得了不同的限制性内切酶谱,酶谱中电泳带的数目反映了整个SV40 DNA分子中这种限制性内切酶的识别序列出现的次数。所以,内森斯和达纳实际上已经发展和建立了一种新的限制性内切酶的活性检测系统。让我们比较一下梅塞尔森和袁、史密斯,以及内森斯和达纳的实验分析方法(表2-3)。
表2-3 梅塞尔森和袁、史密斯、内森斯和达纳的实验分析方法比较

在内森斯和达纳以后,冷泉港研究所的夏普(P.A.Sharp)又在技术上做了两点改进:一是用琼脂糖凝胶代替聚丙烯酰胺凝胶作电泳载体,简化了操作;二是用乙啶染料给凝胶上的DNA染色,在紫外光照射下,乙啶会发出荧光来显示被它染色的DNA片段的位置和数量,使整个操作摆脱了放射性同位素,节省了放射自显影所需的时间和工作量,既推动了实验研究又促进了推广应用。夏普曾经说过:“我肯定不是第一个在生化实验中用琼脂糖作电泳基质的人,但我的工作确实使得这项技术普及起来了。”
在限制性酶识别位点的核苷酸序列测定方面,工作是困难而繁重的。然而,美国威斯康星大学的统计学家富克斯(C.Fuchs)巧妙地运用统计学原理取得了重大突破。因为限制性酶的识别位点都有特定的回文结构,所以富克斯把猴病毒SV40和大肠杆菌噬菌体фx174的核苷酸全序列输入电子计算机,然后用计算机程序检出所有由4个、5个和6个核苷酸组成的回文序列。这样就能知道在SV40和фx174的DNA全序列上有多少个特定的回文序列结构,以及这些结构相隔的核苷酸对数目,富克斯据此制作了相应的软件。当实验科学家发现一种新的限制性酶时,只要用这个软件来处理SV40和ф x174的DNA,并查出切割后的电泳谱上电泳带的总数和各条带所代表的相应DNA片段的分子量,就可以通过计算机推算出这种酶识别和切割的核苷酸序列了。
在短短的几年中,限制性核酸内切酶的研究面貌真可谓是日新月异。袁在1980年十分感慨地说过:“谁能想到那些起初是那么笨重、烦琐而又耗时费力的实验会变得如此轻快和舒服,造成这种变化的正是人类的智慧和精巧的设计。”(https://www.daowen.com)
随着识别、分离和纯化到的限制性酶的种类和数量越来越多,迫切需要一个统一的命名法。现在通用的命名法,是用一个大写字母代表取得酶的菌株的属名,用两个小写字母代表菌株的种名,再用一个大写字母来代表菌株的品系名。例如,大肠杆菌R株中提取的内切酶,可命名为Eco R Ⅰ 、Eco RⅡ等,最末的罗马字代表从这个品系中分离到的内切酶的序号。又如:
从Haemophilus inffuenzae Rd中提取的酶HindⅡ,HindⅢ;
从Diploccus pneumoniae中提取的酶Dpn;
从Bacillus amyloliquefaciens H中提取的酶BamHI等。
限制性酶切割DNA可造成两种切口:一种为平口,另一种为阶梯口,表2-4中HindⅡ等切的是平口,Eco R Ⅰ、Hph Ⅰ等切的是阶梯口。
表2-4 几种限制性酶的比较
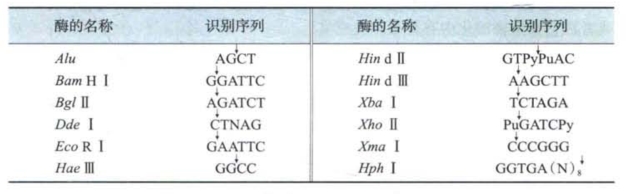
注:A,腺嘌呤;T,胸腺嘧啶;g,鸟嘌呤;C,胞嘧 ;Pu,嘌呤;Py,嘧啶;N,任何一种碱基;↓,内切酶作用切口。
用能产生阶梯切口的限制性酶切割DNA双链分子,会在分子片段的两端各留出一个互补序列,这就是所谓的黏性末端。可以设想,如果用同一种限制性酶去处理不同来源的DNA分子,就可以切出不同来源但却具有互补的黏性末端的DNA片段,把这些具有互补末端的异源DNA片段混合孵育培养,就有可能获得一种新的重组DNA分子,这就是重组DNA技术,或者叫作基因工程。图2-26是关于基因重组技术中重组质粒构筑的示意图。
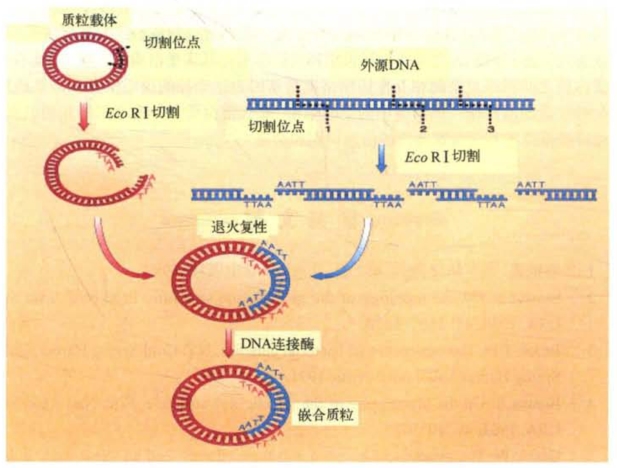
图2-26 外源DNA整合于质粒构筑重组质粒的示意
关于基因工程技术的具体细节,包括目标基因的分离、重组、转染和外源基因在受体细胞中的表达等,在不少教材和专著中都有专门章节讨论,这里就不深入介绍了。
限制性内切酶是基因工程的重要工具酶。然而,我们很难设想生物会经过长期的演化为人类生产一系列工具酶。那么,限制性酶的生物学意义究竟是什么?或者讲它在生物演化中有什么积极意义?
有一种看法认为限制性酶的出现或许只是为了帮助细菌抵御噬菌体的感染。至少有三条理由可以否定这种设想。①这种抵御并不是强有力的。因为某种特异性极强的限制性酶对于稍加修饰的病毒是无能为力的。②从生物演化角度看,发展出一种专门抵御生长于不同株系细菌的噬菌体又有多大作用呢?从抵抗噬菌体侵袭角度看,通过改变细菌细胞表面的附着点结构来阻止噬菌体的吸附和感染是更为有效的途径。③如果限制修饰系统确实是为了抵御病毒感染,那么高等生物体应该会发展出更为完善的限制修饰系统,但是在真核生物细胞中迄今尚未发现类似的系统。所以,这个系统不可能只是为了抵抗病毒感染的。细菌在生物演化中发展限制修饰系统的更有说服力的理由应该说是为了防御外来DNA的入侵,除了病毒DNA之外,作为单细胞原核生物的细菌随时会在接合、转化或转导等过程中接受外源DNA的入侵,而清除异源DNA,确保自身DNA的“纯洁”是维系细菌物种存在的前提,也是新种形成必要的“隔离”机制。这种阻断异种DNA入侵的类似隔离机制在高等生物中不但是普遍存在的,而且是高度发展的,其最高形式就是不同物种之间的种间生殖隔离。
此外,对限制修饰系统的研究还引出了生物学上的一个重要问题。限制性内切酶究竟是怎样工作的?它是通过识别DNA分子上特定的核苷酸序列,进而与这段序列相互作用,最后切割DNA分子。这一系列过程的核心问题是蛋白质(限制性内切酶)和DNA之间的相互识别和共同作用。其实蛋白质和核酸,以及不同蛋白质之间错综复杂的相互作用网络就是基因表达调控的核心所在。如果把复杂的生命活动比作一部演奏中的交响乐章,那么蛋白质和核酸之间的互相识别,也许就是指挥和演奏家之间的信息识别和交流。
