一氧化碳还原氧化铜
一氧化碳还原氧化铜
按照初中化学一氧化碳还原氧化铜的实验进行演示,不但实验需时较多,而且存在有毒的一氧化碳气体逸散和可能爆炸等不安全因素,故宜作些改进。
1实验准备
(1)配制1/3试管澄清饱和的氢氧化钙溶液。
(2)配制CuCl—NH3溶液。方法如下:
CuCl(固体) NH4Cl(固体) 水
重量比 2∶2.5∶7.5
配成溶液后,加浓氨水至所生成的沉淀溶解,在溶液中放入少量铜丝,密闭保存。
(3)装好还原氧化铜的反应管:取一段长6—7厘米由电线中拆出的细铜丝,揉成一团在酒精灯焰上灼烧,使铜丝表面生成黑色的氧化铜(或用石棉绒沾上氧化铜粉)。将它装入内径为10—15毫米、长约20厘米的硬质玻管中部。
(4)硬质玻管一端连接一氧化碳发生装置或贮气装置,另一端与串联的分别盛有氢氧化钙溶液和CuCl—NH3溶液的具支试管连接。实验装置如图6:
2实验操作
(1)缓缓通入一氧化碳约1分钟,拔出通入铜氨溶液的导管,用小试管以排水集气法收集排出的气体,点燃,若无爆鸣声,表示系统中空气已排尽。将导管插入铜氨溶液。
(2)点燃酒精灯,预热玻管后再对准氧化铜加热,同时适当加大一氧化碳气流,约1—2分钟,黑色的氧化铜被还原成光亮的紫红色的铜,石灰水变浑浊,停止加热。
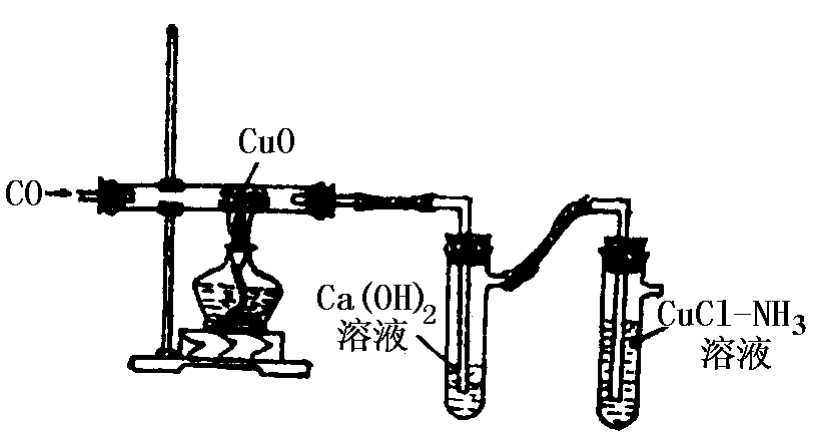
图6
3实验讨论
(1)CO有剧毒,未反应的CO不应使它逸散。如采用火烧,则因驱赶系统中空气所用的CO中混有空气,点火可能爆炸;而还原后尾气中的CO量较少,气流欠稳定常不易点燃。故采用铜氨溶液使形成氯化碳酰铜(I)〔Cu(CO)〕Cl而将它除去。
(2)CO与空气混合物的爆炸极限为12.5%—74.2%,因此在加热反应物之前要做CO的纯度试验,以防止可能发生的爆炸事故。
(3)在气源、反应温度等条件基本相同时,采用表面被氧化的铜丝团或以石棉作载体沾上氧化铜粉进行还原,较之在反应管中堆放氧化铜粉要好。因前者反应物间接触面大,氧化铜用量虽少,但可见范围广,所以既节约演示时间,又能清晰地看到实验现象。同理,氢气还原氧化铜的实验,也可采用表面被氧化的铜丝团代替氧化铜粉。
