选择合适的生石灰与水反应
选择合适的生石灰与水反应
初中化学课本中介绍的生石灰(CaO)跟水的反应虽很简单,但有时反应时间较长,现象不明显。主要原因是在于生石灰本身性质的差异或其已受潮了。
建筑工程上称生石灰加水为石灰的熟化。石灰熟化作用的快慢有很大的差异。1.快熟石灰:熟化速度(CaO+H2O的反应达到高温的时间)在10分钟内;2.中熟石灰:熟化速度在10~30分钟;3.慢熟石灰:熟化速度在30分钟以上。只有快熟石灰才适用于课堂演示实验。
从石灰所含的成份来看,建筑工程上的实践证明钙质石为(MgO含量≤5%)比镁质石灰(MgO含量>5%)熟化快。而且CaO比MgO和H2O的反应放出更多的热量。可查物质的标准生成热,查得CaO(晶)的△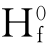 =-635.1kj/mol;Ca(OH)2(晶)的△
=-635.1kj/mol;Ca(OH)2(晶)的△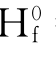 =-986.2kj/mol;H2O(液)的△
=-986.2kj/mol;H2O(液)的△ =-285.84kj/mol;MgO(晶)的△
=-285.84kj/mol;MgO(晶)的△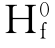 =-601.24kj/mol;Mg(OH)2(晶)的△
=-601.24kj/mol;Mg(OH)2(晶)的△ =-924.66kj/mol。根据△
=-924.66kj/mol。根据△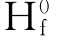 =∑△
=∑△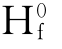 (生成物)-∑△
(生成物)-∑△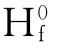 (反应物)可计算出1mol的CaO比1mol的MgO分别与水反应多放出27.68kj/mol的热量。若用镁质石灰,会使实验不准确。质纯多孔块小的生石灰熟化快。含杂质且煅烧不良的生石灰熟化慢。
(反应物)可计算出1mol的CaO比1mol的MgO分别与水反应多放出27.68kj/mol的热量。若用镁质石灰,会使实验不准确。质纯多孔块小的生石灰熟化快。含杂质且煅烧不良的生石灰熟化慢。
在准备实验时,要选择新制的煅烧良好的质纯多孔小块的钙质石灰。如果没有新制的生石灰,就取大块的生石灰,去掉外表已吸湿的部分,把中间干燥的生石灰制成小块状,密闭保存。
装置实验仪器:夹在铁架台的铁圈上放一个蒸发皿,在蒸发皿的上方悬挂着一支红色酒精温度计(150℃的)。课本实验是把水加入生石灰。对快熟石灰,为了避免加水后石灰过热表面形成硬壳而影响进一步反应,改为先将水倒入蒸发皿中,约占1/2容量。再放进生石灰(体积约为蒸发皿容量的1/3)。5分钟之内,就可看到明显的现象,生成的熟石灰就像一朵刚出笼的热气腾腾的疏松的裂开着的碗糕。生石灰和水反应,体积膨胀。质纯且煅烧良好的生石灰反应后体积可增大3~3.5倍。而含杂质且煅烧不良的生石灰反应后体积才增大1.5~2倍。冒出的热蒸气使温度计的红色液柱明显上升。
