第一节 概述
第一节 概述
计算机辅助手术导航系统是经典框架立体定向技术、现代影像诊断技术、微创手术技术、电子计算机技术和人工智能技术等相结合的产物。1986年,Roberts等率先将这一技术用于神经外科手术;1993年,Steinmann等将此技术应用于脊柱外科手术,使脊柱外科手术取得了突破性的进展。近几年,国内陆续报道应用手术导航系统于脊柱外科手术中。计算机辅助手术导航系统具有创伤小、精度高、辐射小等优点。目前应用的导航系统主要是基于C形臂X线透视的导航系统和基于CT的导航系统(图20-1)。

图20-1 基于CT技术的三维手术导航系统工作原理
基于术前CT扫描的三维导航系统的原理如图20-1所示。其中手术器械装有发光二极管,标定后系统将其几何参数储存起来,供立体定位系统在术中进行跟踪;动态参考基准(dynamic reference base,DRB)固定在患者脊柱上,可跟随脊柱运动,补偿由于患者呼吸或者移动导致的坐标变化;立体定位系统多采用红外摄像技术,可高精度确定手术空间内发光二极管和动态基准的坐标,并将数据传递给计算机。上述部件组成了手术中的光电导航系统(图20-2)。
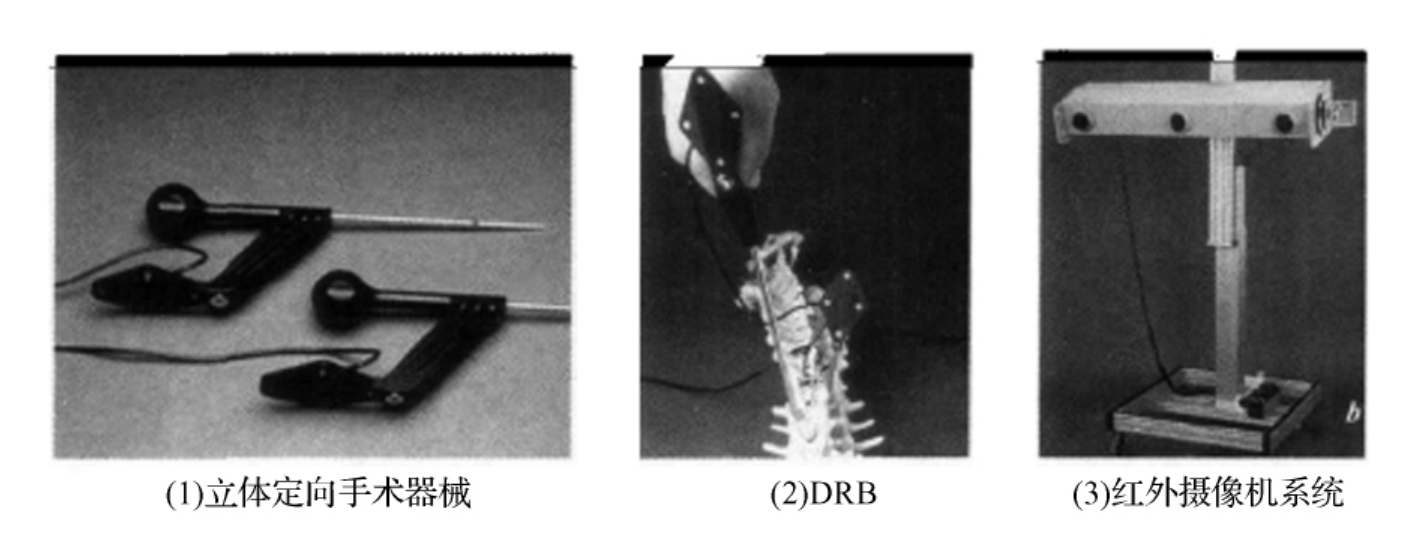
图20-2 光电导航系统
对于脊柱外科手术来讲,由于要进行手术操作的椎体往往不止一个,各椎体间的位置容易出现相对移动,如脊柱表面的皮肤贴标记点容易移位,从而导致较大误差。因此,现有的商业化的导航系统一般都是采用椎体上易识别的特征点作为解剖特征标志点用光电跟踪系统进行对应点配准,或采用激光定位探测器进行点云配准。
医师手术时手工选取脊椎骨棘突上的特征点进行粗配准,然后再用光电跟踪工具在脊椎骨表面取更多的点与CT图像中相对应的脊椎骨表面点通过迭代最近点算法(iterative closest point,ICP)进行精细配准。配准后,为了校验精度医师会在脊椎骨上点取若干个点,然后系统在三维图像显现对应的点,如果配准效果不好,需要重复配准过程。如果误差可以接受,则开始导航手术。这种方法的缺点在于医师手工取点的难度较大,需要较长时间,且配准误差也较大。点云配准指激光定位探测器发射激光到骨表面并反射,通过计算返回时间得到骨表面上每一点的深度距离信息,然后与骨表面点自动配准。由于采用点云配准需昂贵的激光定位仪器,扫描时需要暴露较大的脊椎骨面积,且激光扫描时间较长,目前很少采用。
一、基于X线透视的导航系统
为克服CT导航中存在实时性差、手术时间长等缺点,Hofstetter提出了基于X线透视的导航系统。该系统由立体定位系统,C形臂和影像增强器、图形工作站等组成。手术时,手术器械(T-COS)、患者动态基准(P-COS)和C形臂图像增强器(ACOS)都装有红外发光二极管(图20-3)。
为了求出两坐标系之间的转换关系,C形臂上设有双层铅板结构的定位靶,铅板上有按照一定规则分布的铅点列阵,铅点在C形臂X线机曝光中能够成像,这样就可以根据铅点在该图像的分布,建立X线图像坐标系和影像增强器的坐标转换关系。除此之外,传统C形臂的成像系统还需要对其影像增强器进行内部校正,通过插值算法对透视图像进行几何校正,以得到准确的空间坐标位置。(https://www.daowen.com)
C形臂X线导航的优缺点:优点:①术者对术中透视过程非常熟悉,学习曲线过程短,操作简便;②手术过程中自动注册,避免了耗时的匹配过程;③透视图像在手术体位下采集,并可随时采集加入导航工作站;④患者和医师的X线被动辐射量显著减少;⑤手术整个过程中医师可以直观地判断出最佳的内固定位置和所需内置物的大小型号。缺点:①直接透视所得图像并不能反映真实的解剖结构,其精确度达不到影像辅助手术的要求,为了达到导航所需图像的精确度,必须对透视系统进行校准,消除放大率对图像的影响;②缺少断层图像,术中不能在多个层面指导内置物的角度和深度;③对于椎弓根的透视影像显示不清的颈椎和胸椎以及脊柱重度屈曲旋转畸形的患者应用受限;④骨质疏松、肠胀气、肥胖、肋骨和肩胛骨遮挡及患者体位等因素均可影响X线图像质量。
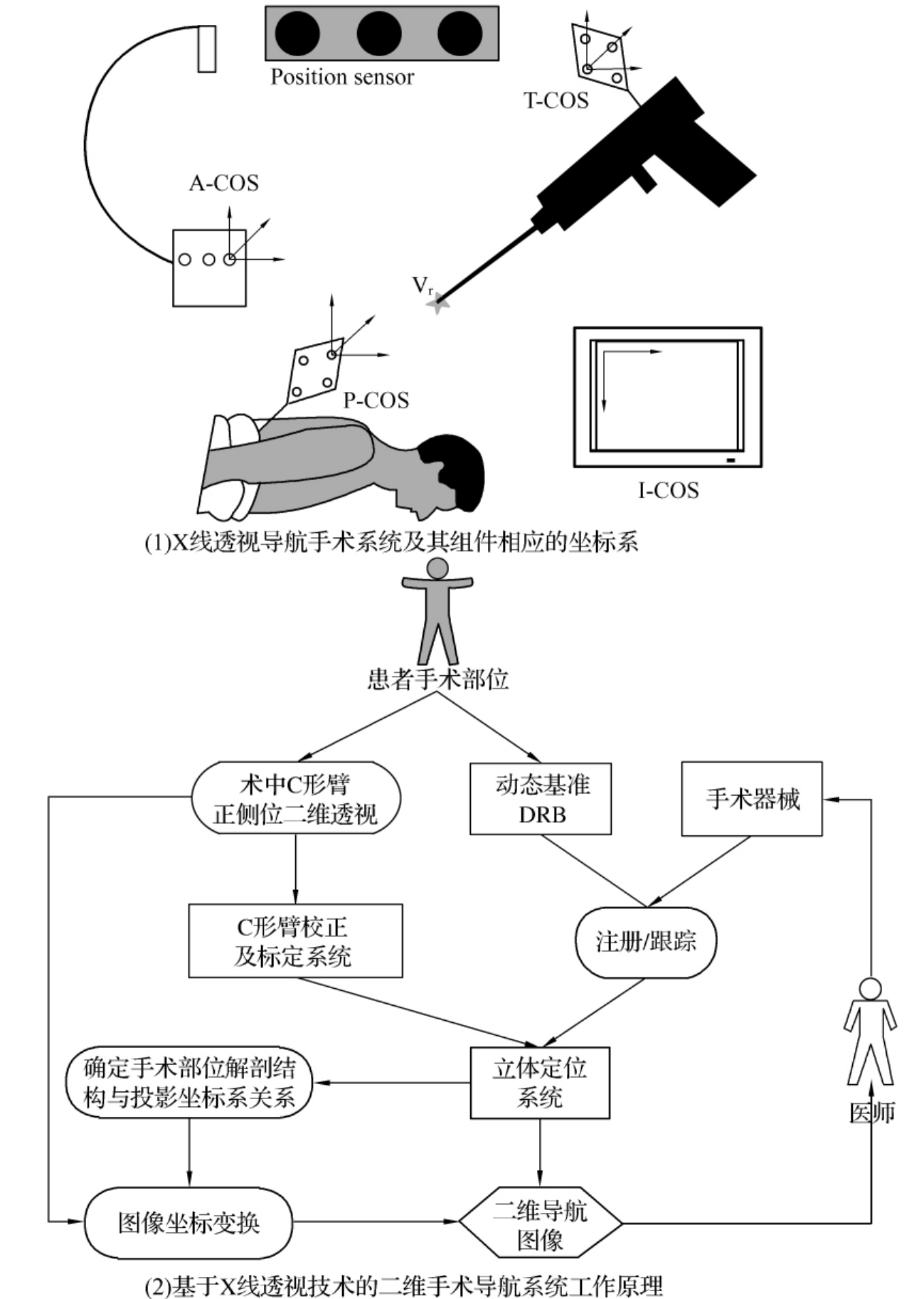
图20-3 基于X线透视的导航系统
CT在导航的优缺点:优点:①术前计划,了解手术部位形态有无变异;②术中导航下操作直观、形象,提高了手术安全性,特别是对严重爆裂脊柱骨折,涉及椎板、关节突等解剖标志的骨折,有解剖变异而致局部解剖标志显示不清的患者;③减少了术中X线透视的次数,大幅度降低术者和患者接受的放射线剂量;④减小了手术窗口,减少失血量及术中的创伤,有利于患者术后的恢复;⑤扩大了手术适应证。缺点:①设备昂贵,使用费用高,大大增加了患者的经济负担;②术者必须熟悉导航系统所有功能及操作,否则必会大大延长手术时间,影响其临床应用与发展;③患者CT资料只能术前获取,如术中体位变化明显,则虚拟三维图像不能真实反映三维关系(即影像漂移,这是CT三维导航系统的最大缺陷),误导术者,增大乎术风险,甚至导致手术失败;④存在一个学习曲线过程。
二、其他方式的导航系统
考虑到术中X线投射图的实时性和CT三维数据的精确性,可将术中二维图像(X线)和三维数据集(术前CT)数据进行配准和定位导航,其工作原理如图20-4所示。

图20-4 术中X线与术前CT配准导航工作原理
此类配准方法主要分为两类。一类是基于特征的方法,借助解剖学特征或人为标记来确定配准关系,通常利用区域分隔以减少数据量。虽然这样可以加快运算速度,但在患者体内植入人为标记很不方便,并且区域分隔有时会导致配准错误,需要不同程度的人为干预。Hamadeh等从术中二维X线图像中提取脊柱轮廓线与术前三维图像进行配准,在实验中的坐标平移变换精度为1.5mm,旋转精度为20,基本可以满足手术要求。另一类是基于图像体素或像素灰度的方法,虽然需要配准的点比基于特征的方法更多,但它不需要特征提取这一步骤。Penney以脊椎骨模型为对象,对比了6个不同目标函数(归一化互相关系数、嫡、互息、图像灰度、梯度相关和梯度差异)对CT和X线图像配准的影响,结果表明不同模态配准时,以图像灰度和梯度差异为目标函数效果最好,其Shear-warp算法配准误差分别为0.5°(旋转),0.5mm(平行于投影平面),5~6mm(正交于投影平面)。
利用术中超声图像与术前CT图像进行配准也是研究热点,超声无辐射、易操作,且实时性较好,但由于手术中只能暴露出部分骨骼,超声得到的是骨骼部分表面的三维图像,而CT三维重建后为体积图像,所以还需要在CT图像中提取表面图像来进行配准。另外,利用标定超声在术中获取图像也会面临相关问题。现在主要采用的A型超声测量时,必须要保证超声探头和测量面垂直,由于骨骼表面形状的变化,一般很难保证。B型超声能瞬时扫描较大区域,信号接收虽不是问题,但获得图像的干扰比较大,只有手动进行扫描。由于手术中骨骼表面往往覆盖残留的软组织,而超声在骨骼和软组织中传播速度不同,由此产生非线性问题及所引发的弹性配准,也是研究的一个难点。
