实验二 维生素C含量的测定
一、实验目的
(1)掌握电子天平的使用方法,容量瓶、移液管、滴定管的洗涤和使用方法。
(2)学会用直接碘量法测定维生素C含量。
二、实验原理
维生素C(Vc)分子中的烯二醇基具有还原性,能被I2定量氧化成二酮基。
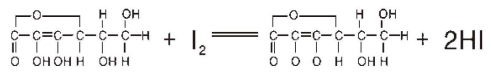
该反应进行很完全,可用于维生素C的含量测定。由于维生素C的还原性很强,在碱性条件下,极易被空气或其他氧化剂氧化。因此,反应常在稀醋酸(HAc)的弱酸性溶液中进行。
三、器材与试剂
100ml小烧杯3个,250ml锥形瓶1个,电子天平一台,25ml的聚四氟乙烯滴定管1根,25ml移液管1根,玻璃棒1根,100ml容量瓶1个,10ml量筒1个。
I2标准溶液(0.05000mol·L-1),维生素C(AR),淀粉指示剂,稀HAc(6mol·L-1)。
四、实验步骤
1.VC溶液的配制
用差减法准确称取维生素C试样0.75~0.85g于小烧杯中,加6mol·L-1的HAc 10ml和少量新煮沸并已冷却的蒸馏水,玻璃棒搅拌使溶解,定量转移到100ml容量瓶中,准确配成100ml溶液并充分摇匀。
2.移取25mLVc
用移液管移取25.00mlVC溶液于250ml锥形瓶中,各加淀粉指示剂2ml,立即用I2标准溶液滴定,直至溶液显示持续的蓝色,并保持30s不褪色。
3.数据记录


4.计算

五、注意事项
(1)维生素C在碱性条件下,极易被空气或其他氧化剂氧化,而在酸性条件下氧化速度大大下降,故而在称量维生素C后马上加入稀醋酸。
(2)I2标准溶液有颜色,在滴定管中较难读数,可采取初读数、末读数均读液面两侧的最高点。
六、分析思考
(1)配制维生素C溶液时,为什么要用新煮沸并冷却的蒸馏水来稀释试样?(https://www.daowen.com)
(2)测定维生素C含量时,如果试样中含有少量的还原性杂质,对测定结果有何影响?
七、维生素C含量测定
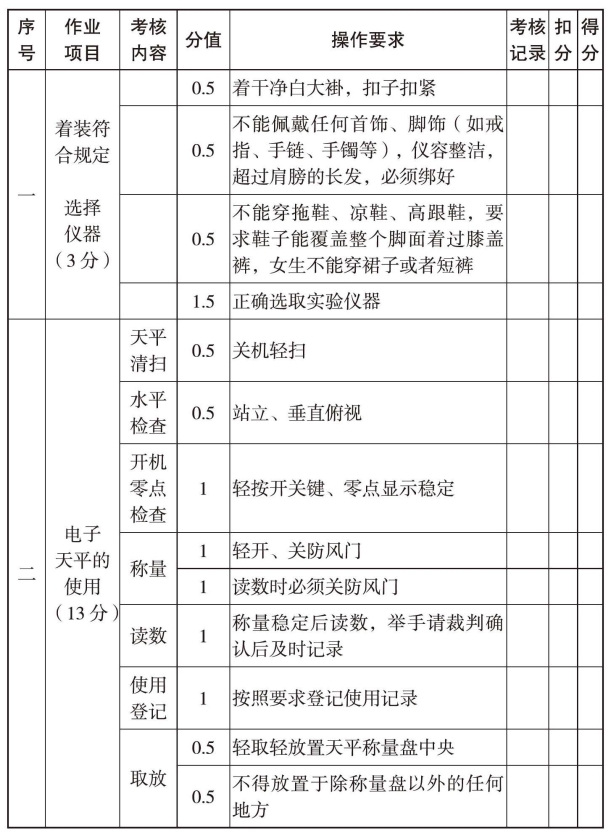
维生素C含量测定评分表
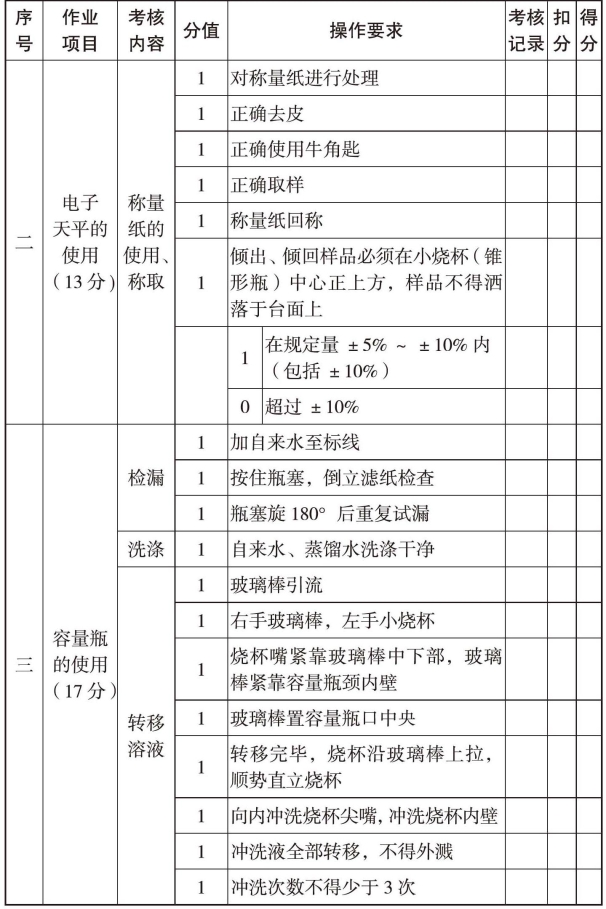
续表
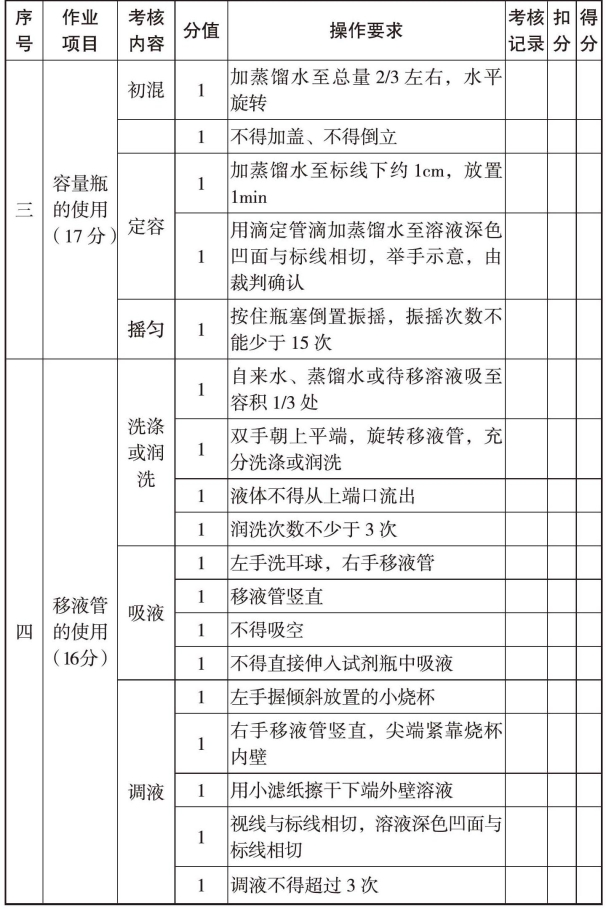
续表
续表
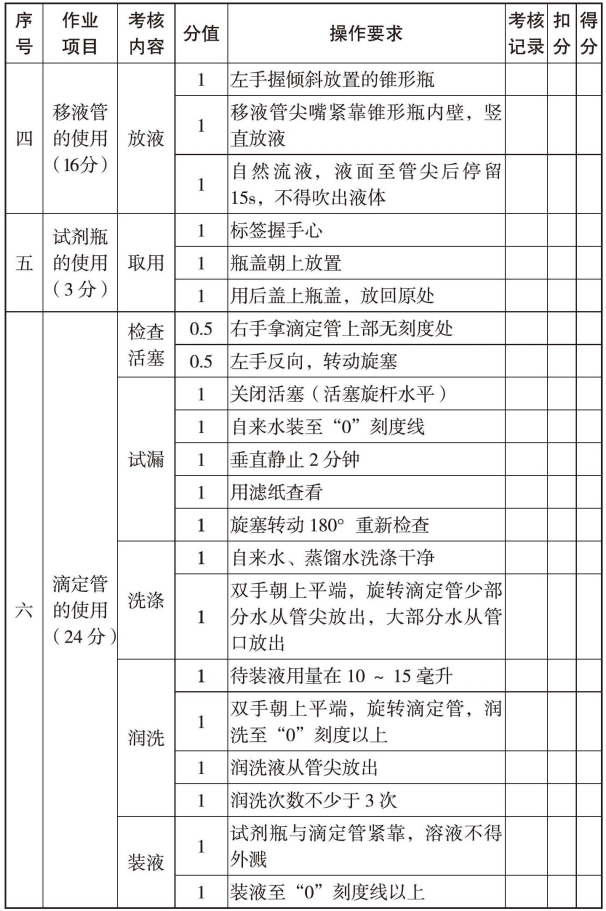
续表
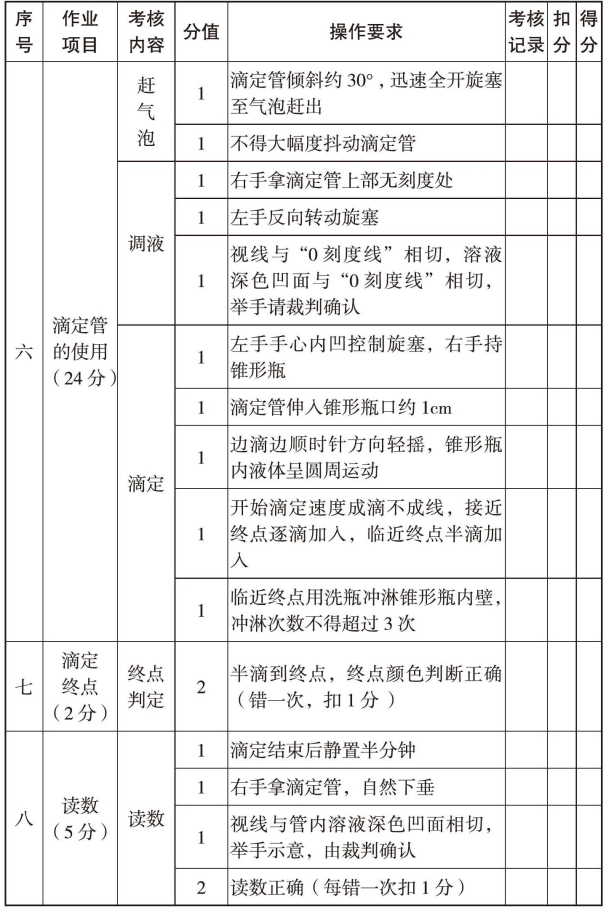
续表
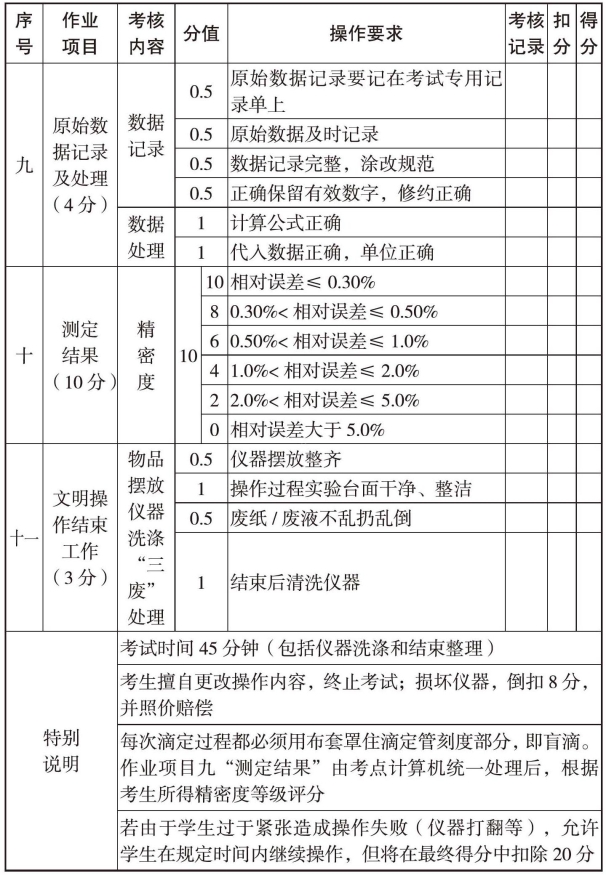
八、实训报告单附表
维生素C含量的测定原始记录单
(每场按台架号从小到大排列后装入回收专用袋。)
学 校____,姓 名____,准考证号____
考点名称____,场次号____,台架号____
题目:维生素C含量的测定
1.能准确使用电子天平、容量瓶、移液管、滴定管,能正确进行原
始记录并计算。
2.称取维生素C试样0.75~0.85g,配制成100ml溶液,精密移取25.00mlVc溶液,用I2标准溶液(0.05000mol·L-1)滴定,测定Vc的含量。
操作步骤:
记录人:日期:
