实验三 生理盐水中NaCl含量的测定
一、实验目的
(1)学会银量法中硝酸银溶液的配制和标定方法。
(2)掌握莫尔法测定卤素负离子的原理和方法。
二、实验原理
银量法是以生成难溶性银盐反应为基础的沉淀滴定法。其根据确定终点所用指示剂不同有三种方法:莫尔法(Mohr法)、佛尔哈德法(Volhard法)、法扬司法(Fajans法)。本实验采用莫尔法。莫尔法是在中性或微碱性溶液中,以K2CrO4为指示剂,用AgNO3标准溶液直接滴定Cl-(或Br-)。由于AgCl的溶解度小于Ag2CrO4,因此首先发生滴定反应,析出AgCl白色沉淀。当AgCl定量沉淀后,过量的Ag+即与CrO42-反应,生成砖红色的Ag2CrO4沉淀,指示滴定达到终点。有关反应式如下:

该滴定反应适宜的pH为6.5~10.5。如果有铵盐存在,溶液的pH需控制在6.5~7.2。
AgNO3溶液可用基准NaCl标定。
三、器材与试剂
250ml烧杯1个,250ml棕色试剂瓶1个,250ml量筒1个,25ml量筒1个,5ml量筒1个,250ml锥形瓶1个,电子天平一台,25ml的聚四氟乙烯滴定管1根,10ml移液管1根。
AgNO3固体(AR);K2CrO4指示剂(50g·l-1水溶液);生理盐水;NaCl:基准试剂,在500~600℃高温炉中灼烧30min后放置于干燥器中,冷却待用。
四、实验步骤
1.0.05mol·L-1 AgNO3溶液的配制
称取AgNO3约2.1g,溶于250ml蒸馏水中,摇匀后将溶液转入棕色试剂瓶中,置暗处保存。
2.AgNO3溶液的标定
(1)用差减称量法准确称取0.12~0.16g已恒重的基准NaCl,置于250ml锥形瓶中,加25ml蒸馏水溶解,再加入50g·L-1K2CrO4溶液1ml,在不断振摇下,用AgNO3溶液滴定至呈现砖红色,即为终点。
(2)数据记录:
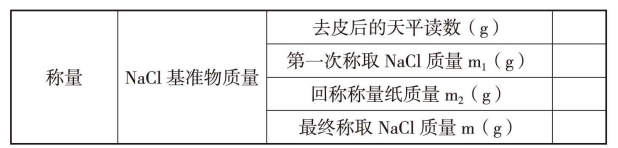

(3)计算:
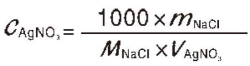
3.生理盐水中NaCl含量测定
(1)用移液管准确量取生理盐水10.00ml,置于250ml锥形瓶中,加蒸馏水10ml,再加入50g·L-1 K2CrO4溶液1ml,在不断振摇下,用AgNO3标准溶液滴定至呈现砖红色,即为终点。
(2)数据记录:

(3)计算:
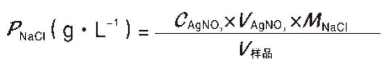
五、注意事项(https://www.daowen.com)
(1)AgNO3溶液使用时要小心,尽量避免与皮肤直接接触。
(2)为减小误差,测定条件和标定条件尽可能一致。故本实验标定和测定均采用莫尔法。
六、分析思考
(1)AgNO3标准溶液为什么要转入棕色试剂瓶中?
(2)莫尔法指示剂是什么?指示剂的量过多或过少有何影响?
(3)如何洗涤装过AgNO3的滴定管?
(4)在生理盐水中NaCl含量测定的过程中,10.00ml样品溶液中为何还要加蒸馏水10ml。
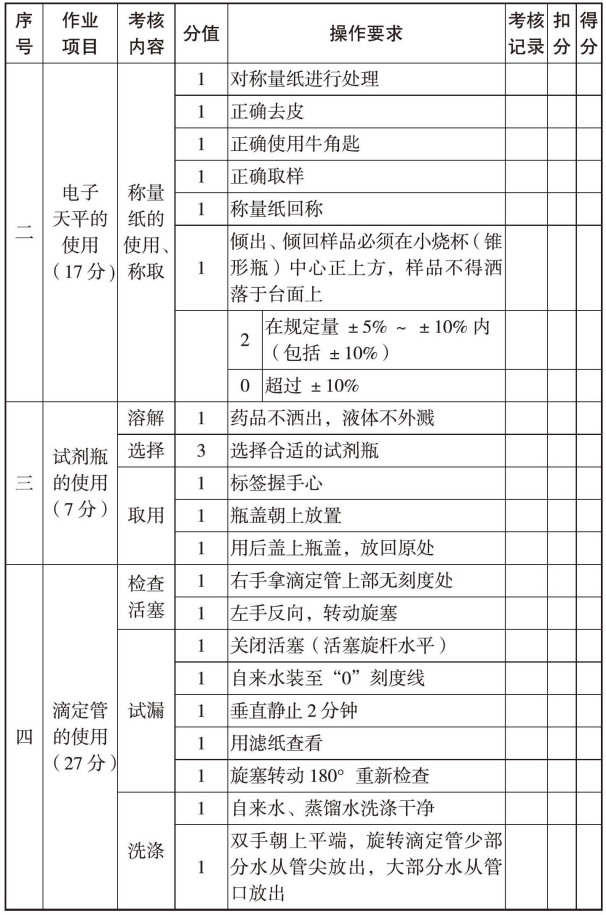
七、生理盐水中氯化钠含量的测定评分表
生理盐水中氯化钠含量测定评分表
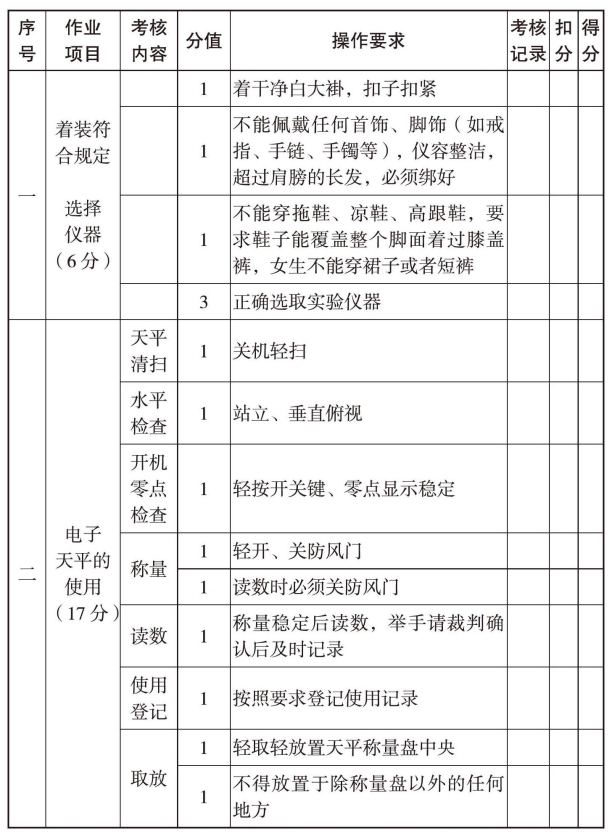
续表
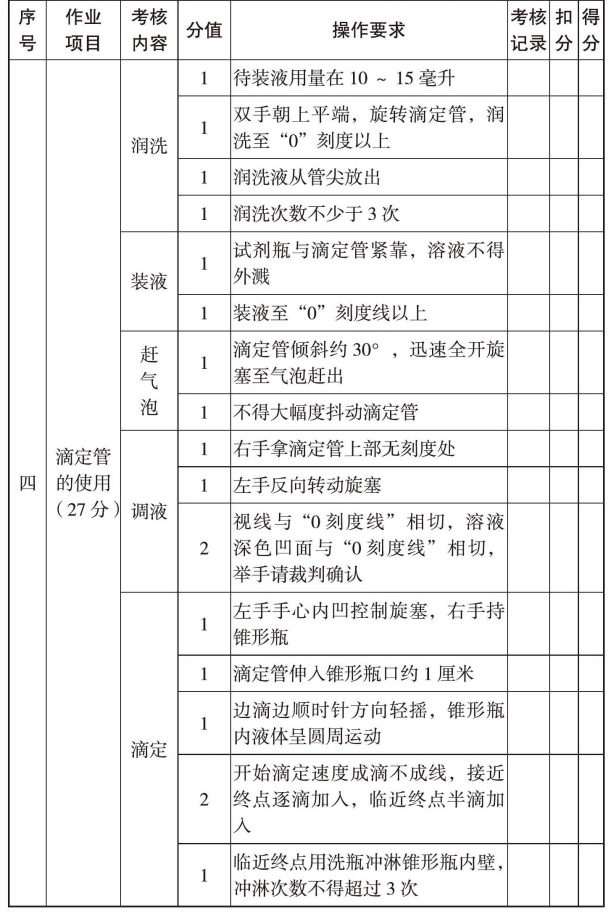
续表
续表
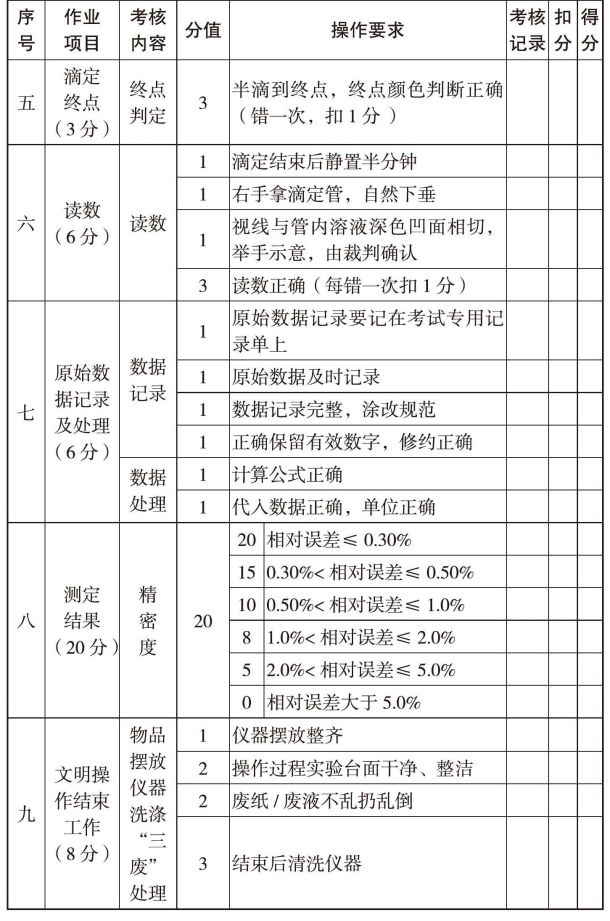
续表

八、实训报告单附表
生理盐水中氯化钠含量的测定原始记录单
(每场按台架号从小到大排列后装入回收专用袋。)
学 校____,姓 名____,准考证号____
考点名称____,场次号____,台架号____
题目:生理盐水中氯化钠含量的测定
1.能准确使用电子天平、移液管、滴定管,能正确进行原始记录并计算。
2.称取2.1g AgNO3,配制0.05mol·L-1AgNO3溶液,标定AgNO3溶液,测定生理盐水中NaCl的含量。
操作步骤:
记录人:日期:
