我国和亚洲部分国家在疫苗招采、配送及监管上的比较分析
我国地处亚太地区,与周边邻国有着密不可分的合作和联系。亚太地区各国之间经济发展和公共卫生事业发展不平衡,且由于地理环境和疾病流行的差异性,不同国家对疫苗种类的需求和配送管理要求各有特点。日本、泰国和越南是亚太国家中疫苗覆盖率较高、配送系统相对完善的国家。本节通过对日本、泰国和越南这3个国家免疫规划和配送系统进行梳理和总结,并与我国进行比较分析,旨在为完善我国的疫苗配送管理提供参考。
1.免疫规划背景
我国自1978年起开始实施儿童计划免疫,后引入免疫规划的概念,预防接种工作逐步与国际接轨。2005年以后,我国陆续出台了《疫苗流通和预防接种管理条例》《预防接种管理规范》《疫苗储存和运输管理规范》和《预防接种异常反应鉴定办法》等法规文件。2019年6月出台了《中华人民共和国疫苗管理法》,对疫苗的使用和管理、冷链运输、预防接种服务和预防接种异常反应与事故报告等方面做出了明确规范要求。我国疫苗分两类:一类是国家免疫规划疫苗,由国家支付疫苗和接种费用,要求儿童必须接种,我国国家免疫规划疫苗包括14种,可预防的传染病有15种;另一类是非国家免疫规划疫苗,以预防控制疾病、满足群众预防保健需求为目的,遵循知情、自愿、自费原则接种,是对国家免疫规划疫苗的一种补充。
亚太不同国家或地区儿童免疫计划有所差异。由表5-6-1可见,2010年12个亚太国家或地区疫苗实施计划均包括的疫苗有:白喉-破伤风-百日咳(DTaP)疫苗、脊髓灰质炎疫苗和麻疹疫苗。日本是其中唯一没有将乙肝疫苗纳入国家免疫规划的国家。在日本,乙肝病毒携带者母亲所生的新生儿和其他婴儿可选用乙肝疫苗。除澳大利亚和新西兰外,所有国家的国家免疫规划(NIPs)中都含有卡介苗(BCG)。疾病流行的地区差异在决定哪些疫苗应纳入国家免疫计划中起着重要作用。例如,日本脑炎(JE)疫苗接种常规用于日本、韩国、泰国,以及我国台湾地区和马来西亚沙捞越州的儿童,因为JE在这些地区普遍存在。另外,虽然各国或地区的卫生部门都建议进行季节性流感疫苗接种,但在大多数国家,这仍然是可以选择而非强制性的。在我国台湾地区和韩国,由政府向儿童、老年人和其他高危人群提供免费流感疫苗。
日本免疫法也将疫苗分为两类:常规推荐疫苗和自愿接种疫苗。日本现行国家免疫规划包括6种疫苗(预防8种目标疾病),其余可用疫苗被归类为自愿接种疫苗,人们需要自付费用,才能获得接种。这导致自愿接种疫苗的接种率很低,目标疾病的发病率较高。两者之间的具体差别见表5-6-2。
2013年4月,日本对免疫法进行了重大修订,最重要的变化是:①在国家免疫规划中纳入3种新疫苗(Hib、PCV7和HPV疫苗),并继续讨论是否将其余重要疫苗纳入国家免疫规划;②政府对免疫接种的进一步资助;③疫苗接种时间的变化;④建立新的国家免疫政策委员会;⑤启动疫苗不良事件报告系统的立法授权及发展国家免疫政策。以前,日本法律要求疫苗的免疫预算由国家和地方政府平均分配。然而,国家的财政支持不足是一个严重问题,给地方政府财政造成了负担。修订后的法律将国家的财政支持从50%增加到90%,减轻了地方政府的财政负担。
泰国于1977年正式启动全国扩大免疫规划(EPI),扩大和加强了原有的免疫服务基础设施。图5-6-1是泰国的国家免疫框架。泰国的公共卫生基础设施旨在覆盖农村和城市地区的所有人口,在该国926个地区,每个地区至少设有一家社区医院,每个分区设有一家医疗保健中心,扩大的免疫规划已完全被纳入基本卫生服务。目前,泰国EPI包括涵盖以下10种疾病的疫苗:结核病(BCG)、乙肝、白喉、破伤风(TT)、百日咳、脊髓灰质炎、麻疹、腮腺炎、风疹和日本脑炎(JE)。除婴儿EPI疫苗外,自2004年以来,泰国还向医护人员提供流感疫苗;自2008年以来,也开始向某些慢性病患者提供流感疫苗。
表5-6-1 2010年12个亚太国家或地区的儿童免疫规划疫苗品种对比
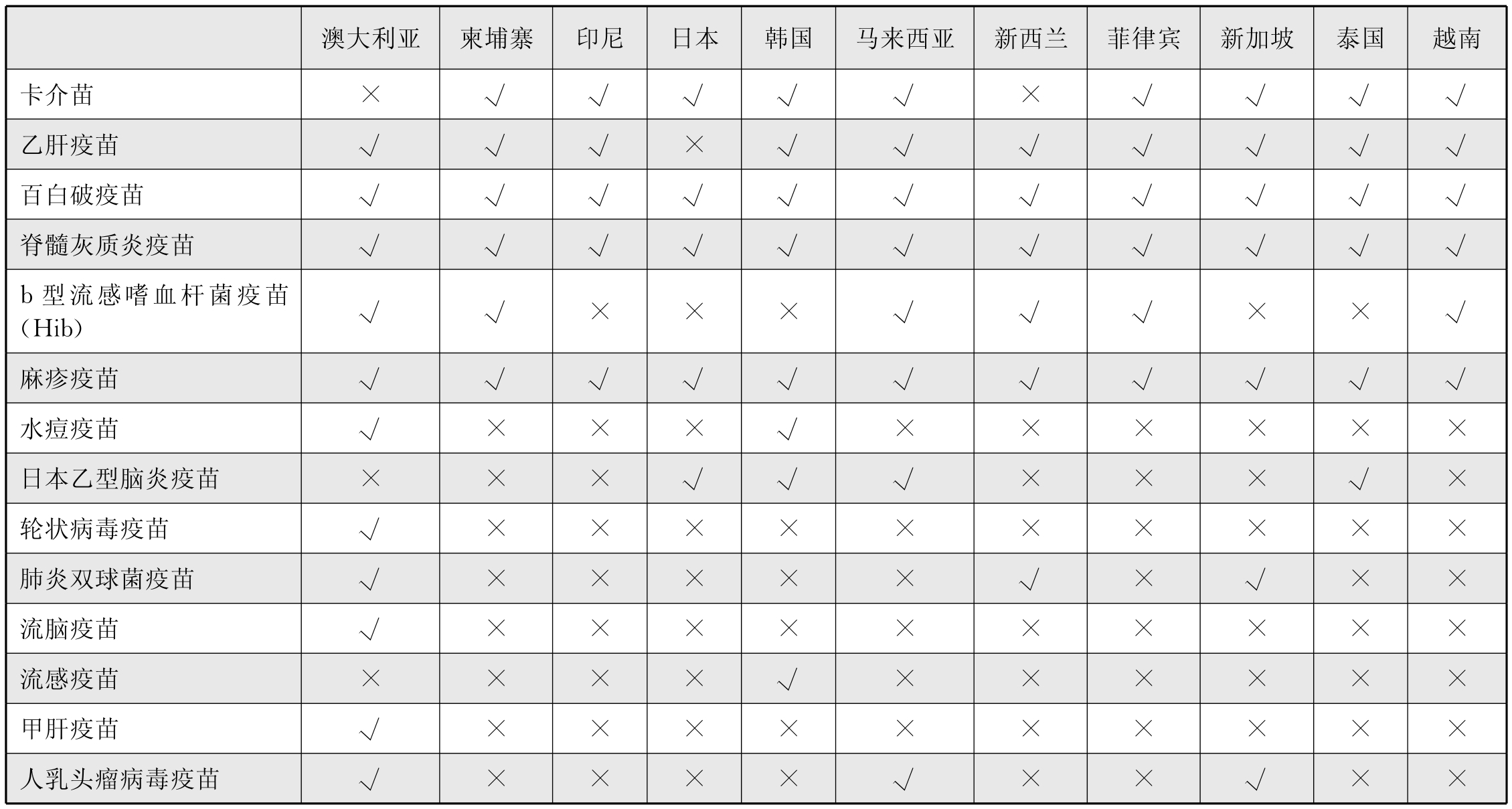
表5-6-2 日本儿童国家免疫规划与自愿接种疫苗比较
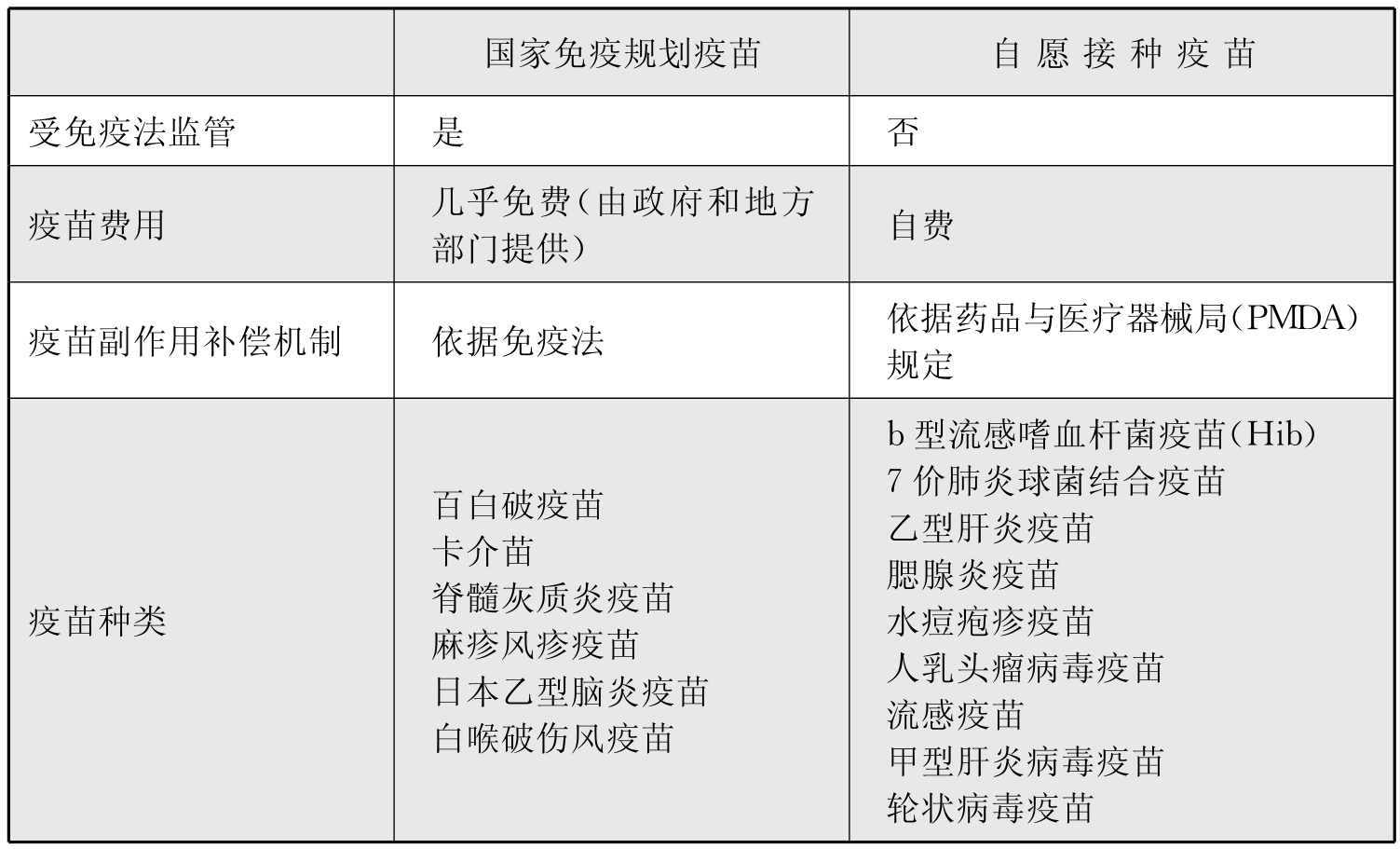

图5-6-1 泰国国家免疫框架
越南《疫苗接种中疫苗的管理和使用指南》规定的疫苗使用管理原则是:①只有获得疫苗接种资格证书的医疗机构才可以开展疫苗接种活动;② 只有固定的疫苗接种机构才能获得疫苗接种资格证书;③获得疫苗接种资格证书的医疗机构必须按照本通知的规定,定期保持实施疫苗接种活动的条件;④具有疫苗接种功能的政府医疗机构必须按规定组织疫苗接种活动,有新生儿的卫生机构必须按规定对新生儿进行疫苗接种;⑤使用EPI范围内的疫苗进行疫苗接种。
2.招采模式
我国《疫苗法》规定:国家免疫规划疫苗由国务院卫生健康主管部门会同国务院财政部门等组织集中招标或者统一谈判,形成并公布中标价格或者成交价格,各省、自治区、直辖市实行统一采购。国家免疫规划疫苗以外的其他免疫规划疫苗、非免疫规划疫苗由各省、自治区、直辖市通过省级公共资源交易平台组织采购,各省也会根据自身情况略有不同。
在泰国,EPI疫苗的采购、技术支持和评估在国家层面开展,同时将负责该计划实施的权力下放到该国的76个省卫生厅。泰国公共卫生部已经建立了一些有关免疫接种的原则和政策,包括人人有权免受疫苗可预防的疾病的伤害;将免疫接种纳入基本保健服务;免费向所有人提供安全、高质量的免疫接种服务,根据国家政策,政府部门的医院和医疗保健中心必须免费提供EPI包含的所有免疫接种,只有私立医院和诊所可能会收取这些服务的费用。免疫接种服务及其他预防和治疗服务由国民健康保险计划(NHIP)资助,该计划成立于2002年,适用于所有未被其他健康保险覆盖的人;其他健康保险计划(例如社会保障计划)适用于私营部门员工和政府员工。
3.冷链配送
我国2017年最新修订的《疫苗流通和预防接种管理条例》中对疫苗冷链运输机构、冷链设备装备水平、冷链温度监测管理水平和疫苗储存、运输中的管理工作都作了进一步的规范:疫苗上市许可持有人、疾病预防控制机构可自行配送疫苗,也可以委托符合条件的疫苗配送单位配送疫苗,且配送非国家免疫规划疫苗的疾病预防控制中心可以收取储存、运输费用;疫苗配送单位应当遵守疫苗储存、运输的管理规范,保证疫苗质量。
日本有世界上先进的条形码技术与温度传感器技术,可以通过载入地图系统实现合理路线规划,提高配送效率;日本合理规范低温性药品运输,禁止疫苗全国性运输而只能进行区域性运输,以减少疫苗运输风险。日本疫苗监管的信息化水平也很高,监管部门可以利用电子手段监测疫苗管理的全过程。
越南采用EPI疫苗供应链,根据世界卫生组织的覆盖率估算,越南有一个运作良好的疫苗供应链,使大多数EPI疫苗的覆盖率超过90%。当地制造商生产多种疫苗并将其运送到国家冷藏库或直接送到4个区域冷藏库。进口疫苗,如五价疫苗(白喉-破伤风-百日咳疫苗、脊髓灰质炎疫苗、b型流感嗜血杆菌疫苗)运输到区域库之前,先运到国家冷库,然后经过越南卫生系统的4个区域冷藏库,并在省和地区各级储存,然后进入社区保健中心。一般来说,每月只向社区级机构提供1~3天的疫苗,用于每月1天的免疫接种,其他时间疫苗不会储存在社区一级,除非在一些为疫苗提供了冰箱的偏远社区。在越南,疫苗必须根据需要,并以适合疫苗制造商要求的温度储存在冷链系统中,并在运输过程中配备监测疫苗温度的设备。疫苗必须在制造商向卫生部登记的温度下保存,按照疫苗接种机构规定的冷链要求分开储存,不得与其他产品一起保存,同时应监测疫苗的日常温度和储存条件。
2009年前,泰国EPI疫苗的采购和分发由疾病控制部(DDC)负责,隶属于卫生部(MOPH)。2002年前,采购疫苗DDC向MOPH提出预算申请,并通过招标程序从生产商或经销商处购买疫苗;政府药品组织(GPO)是一个半官方组织,负责采购疫苗和药品,并为MOPH分发药品。2002年,泰国根据“国家健康安全法”成立了泰国国家卫生安全办公室(NHSO),它是一个由国家卫生安全委员会管理,并由公共卫生部部长担任主席的公共自治组织,旨在管理国家健康保障基金和向泰国公民提供全民医疗保健。2002年医疗改革之后,EPI的预算是根据NHSO管理的全民医疗保险计划支付的,NHSO一直负责管理疫苗的EPI融资。在此系统下,由DDC负责管理疫苗供应链和物流系统。从生产商/进口商向MOPH的中央仓库运送疫苗,再运送到12个预防和控制区域办事处,然后到76个省级保健办事处,最后向约10 000个保健机构(包括医院和保健中心)提供疫苗。该系统包括多个分配步骤,有些步骤可能导致疫苗过期和浪费,以及在某些分布点的过量库存。此外,由于缺乏报告制度,库存控制和疫苗损耗无法追溯,现有冷链设备的更换和维护成本也很高。为了简化疫苗供应和物流系统并改进信息流,NHSO和DDC于2009年启动了一个试点项目,将疫苗供应管理外包给GPO。GPO引入并管理供应商库存(VMI)系统,同时与一家私营物流公司分包,在76个省中的28个省分发疫苗产品。在试验阶段,由DDC采购的疫苗直接从GPO的中央仓库分发到省级/地区医院的药房部门和当地保健中心的初级保健单位(PCU)。(图5-6-2)

图5-6-2 泰国传统和VMI供应链系统比较
在VMI系统中,疫苗供应链从GPO仓库开始,直接进入地区仓库(省和地区医院),然后从地区仓库转到PCU(保健中心或医院免疫诊所)。在传统系统中,该系统自疾病预防和控制中心药房的中央仓库开始,从地区仓库(疾病预防和控制机构办事处)到省级仓库(省级保健办公室),然后到地区仓库(地区卫生办公室和医院),直至PCU。VMI是一种简化的库存管理和订单执行方法,涉及供应商和客户(如分销商、零售商、原始制造商或产品最终用户)之间的协作,从而改变传统的采购和分销流程。客户以电子方式向供应商发送日常需求信息。供应商根据需求为客户生成补充订单。该流程以客户的库存水平、填充率和交易成本的共同商定目标为指导。VMI的目标是调整业务目标,并为供应商及其客户简化供应链操作。VMI的主要优点是降低成本和改善客户服务,大大降低了库存携带成本和库存问题,同时也提供了使库存和运输决策同步的能力。
在韩国,疫苗的冷链运输中必须遵循与疫苗管理相关的原则,如安装温度计、保持适当的温度、记录温度和疫苗在冰箱内的位置、解冻冷冻疫苗,以及检查专门用于疫苗储存的冰箱,以确保注射疫苗的温度。韩国为相关人员配备了教育手册,内容如下:①接收疫苗时,保持冷链,检查包装是否已被损坏,并检查有效期;②储存疫苗时,适宜的温度为2~8℃;③每小时记录冰箱的温度;④保留过去2年的每日温度记录;⑤在冰箱中央安装冰箱温度计;⑥不要将疫苗储存在容易发生温度变化的区域,如冰箱门架或冰箱前部;⑦ 不要将其他种类的药物或食品放在疫苗冰箱中;⑧根据疫苗类型储存疫苗,以便区分;⑨过期的疫苗需要立即丢弃;⑩在停电的情况下,应急电源需要每周检查一次;⑪需要记录多剂量小瓶的开放时间;⑫打开的疫苗不要再次存放,第二天不能再使用。
4.伤害补偿制度
我国实行预防接种异常反应补偿制度,实施接种过程中或者实施接种后出现受种者死亡、严重残疾、器官组织损伤等损害,属于预防接种异常反应或者不能排除的,应当给予补偿。补偿范围实行目录管理,并根据实际情况进行动态调整。接种免疫规划疫苗所需的补偿费用,由省、自治区、直辖市人民政府财政部门在预防接种经费中安排;接种非免疫规划疫苗所需的补偿费用,由相关疫苗上市许可持有人承担。国家鼓励通过商业保险等多种形式对发生预防接种异常反应的受种者予以补偿。预防接种异常反应补偿应当及时、便民、合理。预防接种异常反应补偿范围、标准和程序由国务院规定,各省区市制定具体实施办法。
在韩国,AEFI管理系统始于1994年,2000年引入了通过电子文件传输AEFI报告的系统,并且所有系统在2001年前都已计算机化;2001年,韩国的传染病控制法要求医疗保健专业人员向公共卫生中心报告所有注意到的AEFI;2005年,该系统引入了基于互联网的报告系统,使报告更加便利。目前,韩国的疫苗安全管理系统由四部分组成:快速反应系统、AEFI监测系统、AEFI调查系统和疫苗伤害补偿计划(VICP)。韩国疾病预防控制中心(KCDC)和国家免疫规划部对AEFI实施常规和临时监测措施,并对某些AEFI进行流行病学调查,如严重不良反应或聚集性的AEFI。
日本在1994年和1999年两次修改《预防接种法》后,形成了突发疫苗事故的解决方案,其核心是结果责任原则。方案规定,只要是由预防接种导致的损害,经认定后都能获得一定的补偿金,包括医药费、一次性死亡补助金、残疾人补助和丧葬金等。这种严格的法律规定使得疫苗案件发生后,能够最大限度地保障民众利益。日本在疫苗安全事件后的救济工作尤为突出,规定也尤为明确和细致,若接种导致死亡,要处以4 250万日元的罚款,并且每年还要付给家属相应赔偿。接种疫苗伤害救济制度只在极少数情况下提供救济,即一个人患病、残疾或死于疫苗接种的副作用。该法在1976年修订后首次引入,1994年修订后得到改进。认证过程始于疫苗接种后健康损害报告所在的市政当局。市政府首先成立一个调查委员会,由专家和医学协会成员等组成。该委员会收集有关案件的信息,包括疫苗接种时的情况及其他接种疫苗的儿童的状况,并将它们组织成文件,通过县政府提交给厚生劳动省(MHLW)。该文件具体提交给由MHLW建立的疾病和残疾证书审查委员会,该委员会负责检查疫苗接种与接种人健康状况之间的因果关系,MHLW将根据此次检查的结果发布证明。
在越南,当疫苗接种发生副作用时,免疫机构的负责人必须做到以下内容:立即停止免疫接种;接种疫苗后出现严重并发症的,应紧急治疗和诊断;如果超出其救治能力,有必要将接种疫苗后发生严重事故的人员转移到最近的医院,记录完整信息和疫苗接种期间使用的所有疫苗的统计数据,按规定报告上级;疫苗接种后发生严重事故后24小时内,卫生服务机构应组织调查,卫生署必须组织省专业咨询委员会会议,以确定事故原因;如果怀疑是因疫苗质量而发生接种后的严重事故,卫生部主任将做出暂停使用疫苗以避免严重并发症的决定;当得出与疫苗质量无关的结论时,卫生部主任将决定允许再次使用该疫苗批次,并通知药品管理局。
5.小结与启示
总体而言,日本、泰国和越南的疫苗管理各有特点。日本是信息化技术在疫苗配送管理中应用得比较好的国家之一;泰国在将疫苗供应管理外包给GPO并引进VMI系统后,也形成了高效完备的冷链配送模式;越南疫苗配送管理的特点是疫苗储存和服务区域较集中,这些国家的配送管理经验可以为改善我国的疫苗管理提供一些参考。
为提升疫苗配送的效率,完善监管追溯制度,建议将信息化技术充分应用于疫苗配送管理。国家免疫规划内的免疫规划疫苗招标采购程序相对完善,关于非免疫规划疫苗的销售渠道、冷链储存、配送等流通环节也有明确的规定及全程追溯制度,但冷链配送实时温度监测结合GPS监控的方式成本高、时效性较差,我国疫苗配送管理的技术基础较薄弱。或可参考国外药品所推行的GS1码,规定疫苗生产企业建立精准的疫苗信息追溯系统,实现每支疫苗都有相应的贴码,使疫苗配送和服务交付过程中的每个环节都可扫码查证,企业的信息疫苗管理系统与全国疫苗信息追溯系统衔接。不过,实现这种精准的追溯制度会带来疫苗生产企业和物流体系相应成本的增加,需要一定的准备和缓冲时间。
为充分利用社会资源实现高效的疫苗配送管理和利用,建议在部分经济发达地区引入第三方机构承担疫苗储存和配送的外包服务。我国大基数的人口基础对疫苗的市场需求持续升高,虽然“十三五”期间政府也上调了用于扩大国家免疫规划的经费标准,但我国单一的疫苗物流体系不能满足日益扩大的疫苗储存和冷链需求。目前,我国部分城市(如北京、上海等)已经开始探索政府购买服务、第三方物流公司承担疫苗储存和配送的模式。建议引入有政府认证资质的第三方机构,同时建立标准化绩效评估和监管体系,政府购买服务、定期评估和监督第三方企业,企业发挥物流和专业人才的优势,在疫苗的储存和冷链配送环节严格按照规定进行,从而减少疫苗浪费,保障疫苗质量安全。
本章主要参考文献:
[1]Office of Health Economics.The Publicly Funded Vaccines Market in the UK,2010.
[2]Public Health England.Storage,distribution and disposal of vaccines,the green book,chapter 3.2013.
[3]Khandaker G,Beard FH,Dey A,et al.Evaluation of bacille Calmette-Guerin immunisation programs in Australia.Commun Dis Intell Q Rep.2017,41(1):E33-e48.
[4]Joint purchasing of vaccines and medicines becomes a reality in the EU.http://ec.europa.eu/health/newsletter/132/focus_newsletter_en.htm.
[5]Integrating the supply chains of vaccines and other health commodities.2013.
[6]GAVI.Guidance on Procurement of Vaccines and Cold Chain Equipment.2017.
[7]GAVI.Gavi Alliance Procurement Policy Version 1.0//GAVI.2013.
[8]WHO.WHO Expert Committee on Biological Standardization//WHO.61.2012.
[9]UNICEF.UNICEF PROCEDURE ON SUSTAINABLE PROCUREMENT.2018.
[10]Public Health England.Protocol for ordering,storing and handling vaccines,2014.
[11]NSW Government Department of Health.Immunisation Schedule.Sydney:NSW Government Department of Health,2019.Available from:https://www.health.nsw.gov.au/immunisation/Pages/default.aspx.
[12]MVUNDURA M,KIEN V D,NGA N T,et al.How much does it cost to get a dose of vaccine to the service delivery location?Empirical evidence from Vietnam's Expanded Program on Immunization.Vaccine,2014,32(7):834-838.
[13]SUCHADA JIAMSIRI M M.Thailand Expanded Program on Immunization.Ministry of Public Health,Thailand,2017.
[14]CHOE Y J,BAE G.Management of vaccine safety in Korea.Clinical and Experimental Vaccine Research,2013,2(1):40-45.
[15]YADAV P,LYDON P,OSWALD J,et al.Integration of vaccine supply chains with other health commodity supply chains:a framework for decision making.Vaccine,2014,32(50):6725-6732.
[16]BROWN S T,SCHREIBER B,CAKOUROS B E,et al.The benefits of redesigning Benin's vaccine supply chain.Vaccine,2014,32(32):4097-4103.
[17]GAVI.Considerations for countries on targeting Gavi investments to achieve immunisation outcomes.2018.
[18]GAVI.Cold chain equipment technology guide//GAVI.2018.
[19]WHO.Annex 5:Guidelines on the stability evaluation of vaccines for use under extended controll temperature conditions//WHO.2016.
[20]WHO,PATH.Direct-drive solar vaccine refrigerators—a new choice for vaccine storage.2013.(https://www.daowen.com)
[21]UNICEF.Supplies and Logistics/Immunization.2016.
[22]UNICEF.General Procurement Guidelines.2014.
[23]UNICEF.Cold Chain Support Package.2019.
[24]UNICEF.Walk-In Cold Rooms and Freezer Rooms (WIC/WIFs)Procurement Guidelines.2016.
[25]GUYER B,SMITH D R,CHALK R.Calling the shots:Immunization finance policies and practices—Executive summary of the report of the Institute of Medicine.AMERICAN JOURNAL OF PREVENTIVE MEDICINE,2000,19S(3):4-12.
[26]LYDON P R T A M.Outsourcing vaccine logistics to the private sector:The evidence and lessons learned from the Western Cape Province in South-Africa.Vaccine,2015,29(33):3429-3434.
[27]Shimazawa R,Ikeda M.The vaccine gap between Japan and the UK.Health Policy,2012,107(2-3):312-317.
[28]Public health England,Vaccine uptake guidance and the latest coverage data.https://www.gov.uk/government/collections/vaccine-uptake.
[29]The Publicly Funded Vaccines Market in the UK.
[30]Australian Government Department of Health.National Immunisation Program Schedule.Canberra:Australian Government Department of Health,2019.Available from:https://beta.health.gov.au/resources/publications/national-immunisationstrategy-for-australia-2019-to-2024.
[31]Australian Government Department of Health.National Immunisation Program Schedule.Canberra:Australian Government Department of Health,2019.Available from: https://beta.health.gov.au/health-topics/immunisation/immunisationthroughout-life/national-immunisation-program-schedule.
[32]Khandaker G,Beard FH,Dey A,et al.Evaluation of bacille Calmette-Guerin immunisation programs in Australia.Commun Dis Intell Q Rep.2017,41(1):E33-e48.
[33]Johnson SA,Wang D,Bennett N,et al.Influenza vaccination of Australian healthcare workers:strategies to achieve high uptake.Aust N Z J Public Health.2017,41(5):545-546.
[34]Salmon DA,Teret SP,MacIntyre CR,Salisbury D,Burgess MA,Halsey NA.Compulsory vaccination and conscientious or philosophical exemptions:past,present,and future.Lancet(London,England).2006,367(9508):436-442.
[35]Australian Government Department of Health.National Immunisation Strategy for Australia 20132018.Canberra:Australian Government Department of Health,2013.
[36]Kirby T.No jab,no play:Australia and compulsory vaccination.Lancet Infect Dis.2017,17(9):903.
[37]Australian Government Department of Health.Immunisation policy and governance.
[38]Canberra:Australian Government Department of Health,2019.Available from:https://beta.health.gov.au/health-topics/immunisation/getting-started/immunisationpolicy-and-governance.
[39]Nolan TM.The Australian model of immunization advice and vaccine funding.Vaccine.2010,28 Suppl 1:A76-83.
[40]Lydon P,Raubenheimer T,Arnot-Kruger M,et al.Outsourcing vaccine logistics to the private sector:The evidence and lessons learned from the Western Cape Provincein South-Africa.Vaccine,2015,33(29):3429-3434.
[41]Mitchell AS,Isaacs D,Buttery J,Viney R.Funding of drugs:do vaccines warrant a different approach?Lancet Infect Dis.2009,9(5):269-270;author reply 270-261.
[42]Raina MacIntyre C,Menzies R,Kpozehouen E,et al.Equity in disease prevention:Vaccines for the older adults—a national workshop,Australia 2014.Vaccine.2016,34(46):5463-5469.
[43]Shimazawa R,Ikeda M.The vaccine gap between Japan and the UK.Health Policy,2012,107(2-3):312-317.
[44]NSW Government Department of Health.Immunisation Schedule.Sydney:NSW Government Department of Health,2019.Available from:https://www.health.nsw.gov.au/immunisation/Pages/default.aspx.
[45]LU C,SANTOSHAM M.Survey of national immunization programs and vaccine coverage rates in Asia Pacific countries.Vaccine,2012,30(13):2250-2255.
[46]SAITOH A,OKABE N.Current issues with theimmunization program in Japan:Can we fill the“vaccine gap”?.Vaccine,2012,30(32):4752-4756.
[47]Thailand Expanded Program on Immunization.
[48]TECHATHAWAT S,VARINSATHIEN P,RASDJARMREARNSOOK A,et al.Exposure to heat and freezing in the vaccine cold chain in Thailand.Vaccine,2007,25(7):1328-1333.
[49]MUANGCHANA C, THAMAPORNPILAS P, KARNKAWINPONG O.Immunization policy development in Thailand:The role of the Advisory Committee on Immunization Practice.Vaccine,2010,28:A104-A109.
[50]MVUNDURA M,KIEN V D,NGA N T,et al.How much does it cost to get a dose of vaccine to the service delivery location?Empirical evidence from Vietnam's Expanded Program on Immunization.Vaccine,2014,32(7):834-838.
[51]An Assessment of Vaccine Supply Chain and Logistics Systems in Thailand.
[52]CHOE Y J,BAE G.Management of vaccine safety in Korea.Clinical and Experimental Vaccine Research,2013,2(1):40-45.
[53]Medicines and Healthcare products Regulatory Agency(MHRA),www.mhra.gov.uk,info@mhra.gsi.gov.uk.The Human Medicines Regulations 2012.
[54]Public Health England.Surveillance and monitoring for vaccine safety the green book,chapter 9.2013-03-20.
[55]董铎,陈易新,孙利华.美国疫苗不良事件报告系统.中国药物警戒,2005,2(4):241-243.
[56]李峰,吴晓明.我国药品审评专家咨询制度的沿革与发展.中国新药杂志,2018,18(27):5-11.
[57]李荣,张译匀.中国疫苗流通存储现状与发展对策.办公自动化,2018,23(08):42-46.
[58]王守业.美国的疫苗安全是如何监管的.决策探索,2018(15):79-81.
[59]王树文.借鉴国际经验完善我国疫苗监管体系.中国市场监管报,2018-12-27.
[60]吴坚,周祥国.如皋市疫苗冷链管理的实践与建议.中国农村卫生事业管理,2017,37(10):1201-1203.
[61]阎立红,高志刚,宋旺.天津市免疫规划疫苗储存配送服务外包管理策略.职业与健康,2017,33(11):1565-1567.
[62]雍佳松,杨世民.我国医药冷链体系的现状及其发展建议.中国药房,2014(25):2308-2311.
[63]张雪娇.我国疫苗致损救济制度存在问题及对策分析——以现阶段救济制度及司法实践为视角.广西政法管理干部学院学报,2016,31(5):50-58.
[64]张蕾.CDC对二类疫苗的经营现状.企业改革与管理,2017(20):99.
[65]周围,刘艾林,杜冠华.中国与英国药品不良反应监测制度的对比研究.中国药物评价,2015,32(6):376-380.
[66]中国生物技术股份有限公司内部研究报告.《中国疫苗产业现状及相关问题研究》.
[67]中华商务网.中国保温冷藏车市场运行动态及发展战略咨询报告.http://www.chinaccm.com/48/4804/480406/news/20110117/155741.asp.
[68]赵贤.中美药品冷链物流体系的比较研究.中国药业,2012,21(16):15-16.
[69]朱利兵.我国疫苗流通监管法律问题研究.兰州大学行政法与行政诉讼法,2017.
[70]祝晨竣.论我国疫苗监管的缺陷及完善对策.现代商贸工业,2019,40(03):148-149.
