分析探究题(共44分)
20.(2021·苍南)(6分)为了探究原子结构的奥秘,1911年英国科学家卢瑟福进行了著名的α粒子轰击金属箔实验。
【实验装置】如图甲所示:
①α粒子发生器——放射性物质放出α粒子(带正电荷),其质量是电子质量的7000多倍;
②金属箔——作为靶子,厚度1μm,重叠了3000层左右的原子;
③探测屏——α粒子打在上面发出闪光。
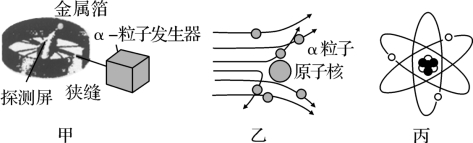
第20题图
【实验现象】如图乙所示:绝大多数α粒子穿过金属箔后仍沿原来的方向前进,但是有少数α粒子却发生了偏转,甚至有极少数α粒子几乎达到180°的偏转,像是被金属箔弹了回来。
【分析解释】
(1)卢瑟福推测“除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的”,其中的“很小的结构”指的是原子结构中的________。支持卢瑟福推测的实验现象是________________________________________________。
(2)卢瑟福在分析实验结果的基础上,提出了图丙所示的原子核式结构。卢瑟福的这一研究过程是个 ( )
A.建立模型的过程 B.得出结论的过程
C.提出问题的过程 D.验证证据的过程
21.(2021·金华婺城)(10分)根据CO分子和CO2分子的化学式分析计算:
(1)相同分子数的CO和CO2,氧元素的质量比为________。
(2)相同质量的CO和CO2,氧元素的质量比为________。
(3)使CO和CO2中含有相同质量的碳元素,则CO和CO2的质量比是________。
(4)已知一个CO分子的质量为n千克,一个CO2分子的质量为m 千克(假设两种分子中碳、氧原子分别具有相同的中子数),若以碳原子质量的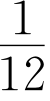 为标准,则CO2的相对分子质量是________(用m、n表示)。
为标准,则CO2的相对分子质量是________(用m、n表示)。
22.(2021·三门)(16分)1989年世界卫生组织把铝列为食品污染源之一,建议每人每日的摄入量控制在0.004g以下。若在1千克米面食品中加入明矾2克(明矾的化学式为KAl(SO4)2·12H2O,相对分子质量为474),请回答下列问题:
(1)人从食物中摄入的铝指的是 ( )
A.铝元素 B.铝单质 C.铝原子
(2)明矾中钾元素与硫元素的质量比为________。
(3)明矾中铝元素的质量分数为多少? (结果精确到0.1%)
(4)如果某人一天吃了100克上述米面食品,通过计算说明其摄入的铝的量是否超过安全摄入量。
23.(2021·兰溪)(12分)科学家发现世界最深的海沟——马里亚纳海沟受到了多氯联苯的污染。已知六氯联苯(C12H4Cl6)是多氯联苯的一种,难溶于水,有致癌性。
(1)C12H4Cl6由________种元素组成。
(2)一个C12H4Cl6分子由________个原子构成。
(3)C12H4Cl6中碳、氢元素的质量比是________。
(4)多少克C12H4Cl6中含有213克的氯元素? (列式计算)
