1.3.3 热力学基本定律
热力学第一定律和第二定律是科学界公认的宇宙普遍规律。能量守恒定律认为,能量可以由一种形式转变为另一种形式,但其总量既不能增加也不会减少,是恒定的。这个定律应用到热力学上,就是热力学第一定律。这一定律指出物质和能量既不能被消灭,也不能被创造。热力学第二定律是描述热量传递方向的:分子有规则运动的机械能可以完全转化为分子无规则运动的热能;热能却不能完全转化为机械能。此定律的一种常用表达方式是每个自发的物理或化学过程总是向着熵增加的方向发展。
1.热力学第一定律
在工程热力学中,热力学第一定律主要说明热能和机械能在转移与转换时,能量的总量是守恒的。它确定了热能与机械能在转换时相互间的数量关系,是热力学的基本定律,是进行热力分析的基础。
能量守恒与转换定律是自然界中最重要的普遍规律之一。它说明自然界中物质所具有的能量既不能被创造,也不能被消灭,只能从一种形式转变为另一种形式,在转变的过程中,能量总和保持不变。热力学第一定律是能量转换和守恒定律在热力学上的应用,它确定了热与其他形式能量相互转换在数量上的关系。热和功都是能量的形式,因此,它们可以相互转换。热和功相互转换的数量关系便是由热力学第一定律来阐明的。
能量转换和守恒定律指出:在自然界,一切物质都具有能量。能量有各种不同的形式,能量转换和守恒定律不是从任何理论中推导出来的,而是人类长期的生产斗争和科学实验中丰富经验的总结,并为无数实践所证实。它是自然现象中最普遍、最基本的规律之一,普遍适用于机械、热、电(磁)、原子、化学、生物等能量的变化过程。物理学中的功能原理、工程力学中的机械能守恒定律等,其实质都是能量转换和守恒定律。热力学第一定律就是能量转换和守恒定律在热现象领域的应用。
热力学第一定律可以表述为:热可以变为功,功也可以变为热。一定量的热消失时,必产生与之数量相当的功;消耗一定量的功时,也必出现相当数量的热。
历史上曾有不少人企图制造一种不消耗能量而能连续不断做功的所谓第一类永动机,但所有此类永动机都违反了能量转换和守恒定律,均归于失败。因此,热力学第一定律也可表述为:第一类永动机是不可能造成的。
2.热力学第二定律
在自然界中,热力过程具有方向性。热力学第一定律只是准确地肯定了过程中的能量平衡关系,并不能说明过程的方向性,而研究过程的方向性,正是热力学第二定律的任务。研究热力学第二定律,分析发动机的理论循环,主要目的是弄清楚怎样把加入的热能更多地转换为机械能,明确提高热效率的方法。目前,广泛用在航空发动机上的热力循环是航空活塞发动机采用的奥托循环和航空燃气涡轮发动机采用的布莱顿循环。
以下介绍航空活塞发动机的理想循环(奥托循环)。
如图1-18所示,奥托循环是由绝热压缩1—2、等容燃烧2—3、绝热膨胀3—4和等容放热4—1四个热力过程组成的。这个循环首先由德国工程师奥托在1876年成功地应用于内燃机并由此得名。由于该循环在等容条件下燃烧加热,因此也称为等容加热循环。现代航空活塞发动机都是按奥托循环来工作的。
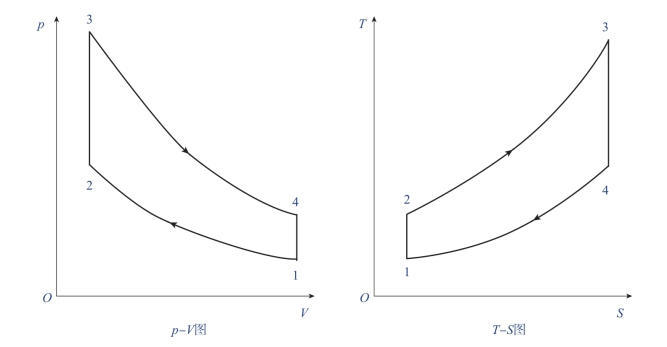
图1-18 航空活塞发动机的理想循环(奥托循环)
在奥托循环中,工质首先被活塞压缩,进行绝热压缩。在这个过程中,首先发动机对工质做功,气体压力和温度升高,为气体燃烧、膨胀做准备;然后进行等容加热,实际上是燃料燃烧释放出热能的过程,气体温度、压力急剧升高,为膨胀做功准备条件;接着进行绝热膨胀,在这个过程中,工质推动活塞做功,气体压力、温度降低;最后气体进行等容放热过程,工质向外界放出热量,气体温度、压力降低,直到恢复到原来状态。这样,工质就完成了一个循环。由此可见,通过工质气体不断地完成热力循环,最终发动机就不断地输出机械功。这一切都依赖燃料可靠燃烧,因此必须确保可靠的点火源。(https://www.daowen.com)
3.热力学第二定律的表述
人们在研究机械能与热能相互转化的过程中,通过大量的实践发现,机械能可以通过摩擦自发地全部转换成热能,但反过来,热能却不可能全部转换成机械能。无数实践表明:热能转变成机械能的过程中,必须损失一部分,才能将另一部分转变成机械能,不可能将全部热能转变成机械能。
热力学第二定律是人们在实践中总结出来的客观规律。它有各种不同的说法,其中涉及范围最广泛的一种说法是:自然界中凡是有关热现象的自发过程都是不可逆的。
这里所说的自发过程是指不需外界辅助就能自动进行的过程。例如,有两个被分隔开的容器,甲容器内盛有气体,乙容器内为真空,当它们连接在一起并互相沟通时,气体就会自发地从甲容器流入乙容器,这是一种自发过程;反之,已经流进乙容器的气体,却决不会自发地逆向全部流回到甲容器中。
在长期的生产实践中,人们早就熟悉这样的事实:热能不会自发地转换为机械能,而机械能通过摩擦能自发地转换为热能。为什么机械能转换为热能与热能转换为机械能这两种过程之间会有这种区别呢?这是由热能的本质所引起的。热能是物质内部大量分子做无规则运动所产生的能量。大量分子的无规则运动是一种漫无秩序的混乱运动,一切有规则的运动往往很容易被破坏而转变为这种无规则的运动。也就是说,有规则的运动转变为无规则的运动的机会较多。反之,大量分子漫无秩序的混乱运动自发地转变为同一方向有规则运动的机会则非常少。因此可以说,这种转变是不可能自发性出现的。机械运动是大量分子的有规则运动,所以,可以自发地转变为热能,而热能却不能自发转变为机械能。
要想使自发过程逆向进行,必须提供一定的条件。例如,要使热从温度较低的物体逆向传至温度较高的物体,必须有制冷机,同时要靠外界对制冷机做功,这里所说的“外界做功”,就是使热由温度较低的物体传至温度较高的物体必须具备的条件。没有这个条件,热绝不会从温度较低的物体自发地传到温度较高的物体上。
热力学第二定律有多种表述形式,比较著名的有以下两种:
(1)克劳修斯表述。克劳修斯将热力学第二定律表述为:热不可能从低温物体传到高温物体而不引起其他任何变化。
航空发动机工作时,燃料在气缸或燃烧室中燃烧,释放出热能,对工质加热,相当于热源向工质供热,工质膨胀做功后排出发动机。无论工质膨胀得如何彻底,膨胀后的温度总是比大气温度高,从而不可避免地有一部分热能排入大气中,这可以看作向冷源排热。所以,任何一种热机要将热能转变成机械能,必须具备热源和冷源,工质必须向冷源排热,因而只能将部分热能转变成机械能。这是热机热效率不高的根本原因之一。
由于任何热力发动机都要向冷源排热,因此,从热源获得的热量不可能全部转换为功,只有热源获得的热量与排到冷源中的热量的差额,这部分热量才能转换为功。
(2)开尔文-普朗克表述。开尔文-普朗克将热力学第二定律表述为:不可能制造出只与单一温度的热源交换热量并对外界做功又不引起其他变化的循环热力发动机。
克劳修斯表述指出,为了使热从低温物体传到高温物体,必须由外界做功;开尔文-普朗克表述指出,为了使热力发动机运行,必须同时具备高温热源和低温热源。因此,不可能把吸收的热量全部转变为功,即不可能制造出热效率为100%的热力发动机。那种所谓不违反热力学第一定律,能利用存在于自然界中的无限能量并永久运转下去的发动机,称为第二类永动机。热力学第二定律表明制造出第二类永动机是不可能成功实现的。
热力学第二定律的两种表述法在语句表达方式上虽然不同,但实质上是等效的。如果否定其中一种表述,必定导致否定另外一种表述。
热力学第二定律是人们在实践中总结出来的自然界中的一条客观规律,不能违背。历史上曾有人企图创造一种发动机,利用大气所含热能来源源不断地做功。这种只从一个热源(大气)吸收热能来做功的发动机(称为第二类永动机)是违反热力学第二定律的(没有冷源),只有转变为机械能的热量而没有废气带走的热量,这种想法是不可能实现的。根据热力学第二定律,人们虽然不能把加入发动机的热量全部转变成机械功,但是,在尽可能的范围内,必须想方设法尽量减少损失,把加入的热量尽可能多地转变为机械功,以提高发动机的效率。
