霍乱弧菌检验操作规程及医院感染管理
一、范 围
本操作规程规定了一天内腹泻3次或3次以上的患者、带菌者粪便、患者粪便、呕吐物等标本中的霍乱弧菌的检验方法。
二、标本采集及处理
1.采集时间:在未服用抗生素前采样。
2.采集方式:用棉拭子或采便管从肛门插入直肠3~5cm取样,必须看到有粪便黏附才可;水样便采取1~2mL,成形便采取指甲大小的粪量。
三、设备材料及试剂
1.冰箱:-20~4℃,恒温培养箱:35±1℃。
2.暗视野显微镜:10×~100×、电脑。
3.灭菌注射器1mL,载玻片、盖玻片及接种环。
4.无菌棉签,一次性接种环、生物安全柜:Ⅱ级。
5.碱性蛋白胨水,庆大霉素琼脂平板。
6.霍乱弧菌单克隆抗体。
四、检验程序(https://www.daowen.com)
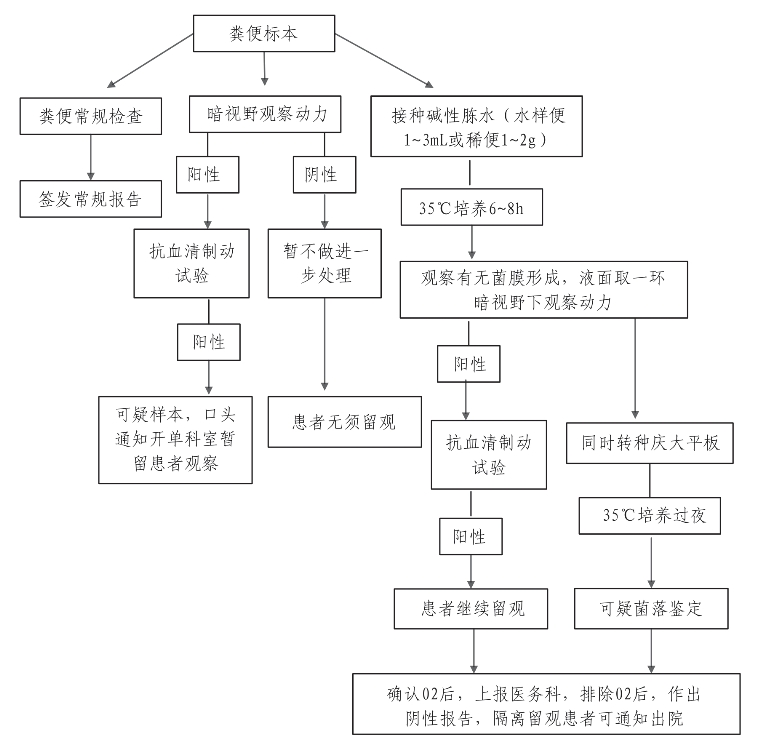
图4-21 流程图
五、动力及动力抑制试验操作步骤
1.如是急性期患者的水样便,则用接种环或滴管取1滴水样便在玻片上然后盖上盖玻片,直接用暗视野显微镜观察动力。或加生理盐水1滴在玻片上,用接种环取较干的便1环放置生理盐水中研匀,盖上盖玻片直接用暗视野显微镜观察动力。高度可疑的标本可取已增菌的碱性蛋白胨水1滴在玻片上然后盖上盖玻片,直接用暗视野显微镜观察动力。如在镜下见到穿梭样运动(像夜空中的流星)即动力试验阳性,否则阴性。
2.动力试验阳性的标本,则取O1和O139群霍乱弧菌诊断用单克隆抗体各2滴放置玻片上,取标本1滴或1环放在其中研匀,盖上盖玻片,用暗视野显微镜观察是否有原来的穿梭样运动,如穿梭样运动已迅速停止并凝集成块状即动力抑制试验阳性,否则阴性。
3.动力试验和动力抑制试验结果可口头初步报告,但不是确诊报告。双阳时口头报告高度可疑。
六、增菌及分离培养
1.所有粪便标本都应经过增菌,尤其是恢复期患者、带菌者或用过抗菌药物的患者标本含菌量少,单靠直接分离不易检出。需经碱胨水37℃增菌6~8h后分离。
2.标本含菌量少时,为提高检出率可实行2次增菌,取第一次碱胨水增菌后的培养物表层液0.1~0.2mL,接种于8~10mL的碱胨水中,37℃培养6~8h后再做分离。
3.霍乱弧菌好氧,易形成菌膜,故在取出增菌管时动作要轻,接种环于菌膜下取一满环,划线接种于TCBS或4号琼脂平板37℃10~14h孵育培养。
七、报疫程序
一旦发现阳性可疑标本立即电话通知医院职能部门,确认患者资料,逐级上报。
八、实验室消毒
实验室物体表面,每日清洁消毒(如用500mg/L含氯消毒液擦拭消毒。抹布用后500mg/L含氯消毒液浸泡30min,清洗后晾干备用)。实验室内安装非手触式洗手装置等设施,应严格执行手卫生规范。地面每日清洁消毒(如用500mg/L含氯消毒液拖地一次,有可见血液体液污染物时,先用2000mg/L含氯消毒液作用30mim,擦拭后,湿式清扫。拖把用后1000mg/L含氯消毒液浸泡30min,冲洗后晒干备用)。
九、个人防护
严格执行标准预防,医务人员穿工作服、佩戴一次性医用外科口罩和工作帽。进入隔离观察室时应外加隔离衣,离开时应及时脱卸。需接触患者呕吐物、排泄物等污物时应戴手套。处理频繁呕吐患者时,建议在隔离衣外穿戴塑料围裙与戴眼罩,以避免体液性污物的渗透污染,以及对脸部黏膜的直接溅入。脱卸隔离衣、手套、围裙和眼罩后应立即洗手。配制消毒剂溶液时,应注意操作者脸部(佩戴口罩、眼罩或面罩)、手部(戴塑胶手套)以及身体的保护(穿戴防水围裙)。
十、生物安全
凡接触患者排泄物等检验样本时,应加强生物安全意识,采取有效的个人防护措施。有条件的单位应配备生物安全柜(推荐使用A型生物安全柜),所有潜在感染的操作均应在生物安全柜内执行。标本盒采用带有螺旋盖的,逐步淘汰开放式标本盒。残留标本应严格按感染性废弃物的管理要求处置。发现可疑细菌应立即转移至生物安全Ⅱ级(P2实验室)实验室内操作,相关的检验人员应持证上岗。肠道门诊、检验室等重点区域应做好防蝇设施。医疗废物用黄色垃圾袋双层密封包扎按《医疗废物管理条例》处理。
十一、检验依据
1.国家传染病诊断标准:WS 289—2008。
2.卫生部疾病控制司《霍乱防治手册》第五版。
3.北京市卫生防疫站《卫生防疫微生物检验操作规程》。
4.《北京市常见传染病防制工作手册》。
