3.1.1 概 述
3.1.1.1 硫酸的用途
硫酸工业是重要的基本化学工业之一,硫酸是多种工业生产的基本原料,广泛地应用于国民经济的很多重要部门。硫酸最主要的用途是生产化学肥料,用于生产磷铵、过磷酸钙、硫铵等,每生产1t过磷酸钙(以18% P2 O5计)消耗350~360kg的硫酸(100%硫酸)。另外,硫酸可以用于生产硫酸盐、塑料、人造纤维、染料、油漆、药物、农药、杀草剂、杀鼠剂等;可用作除去石油产品中的不饱和烃和硫化物等杂质的洗涤剂;在冶金工业中用作酸洗液,电解法精炼铜、锌、镉、镍时的电解液和精炼某些贵重金属时的溶解液;在国防工业中与硝酸一起用于制取硝化纤维、三硝基甲苯等。
3.1.1.2 硫酸的性质和规格
硫酸的分子式为H2 SO4,相对分子质量为98.078,外观为无色透明油状液体,密度(20℃) 为1831kg/m3,常压下沸点为279.6℃。硫酸是重要的强酸,有很强的吸水性和氧化性。硫酸在溶于水时放出大量的热,溶解热为92kJ·mol-1。含H2 SO4 98.4%的浓硫酸是硫酸-水体系的最高恒沸点组成,在硫酸生产的吸收工序中吸收能力强,不生成酸雾。但98%的硫酸结晶温度(3℃)高,不适宜于冬季或寒冷地区使用。在寒冷条件下可生产92%硫酸(结晶温度为-34℃)或93%硫酸(结晶温度为-32℃)。发烟硫酸是SO3的H2 SO4溶液,SO3与H2 O的摩尔比大于1,为无色油状液体,因其暴露于空气中逸出的SO3与空气中的水分结合形成白色酸雾,故称为发烟硫酸。发烟硫酸主要是为有机化学工业的多种需要生产的。
生产中,可以根据硫酸的密度和当时硫酸的温度来确定硫酸的浓度,其关系如表3.1所示。大致来说,硫酸水溶液的密度随温度的降低和硫酸含量的增加而提高。
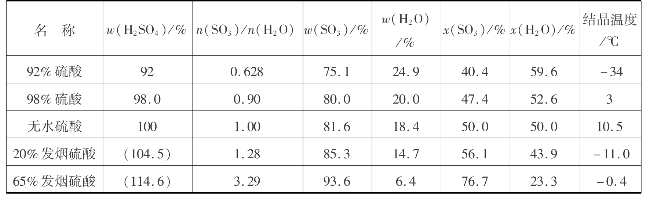
常用的硫酸有质量分数为75%,92%,98%硫酸和w(SO3)为20%的发烟硫酸。75%硫酸原是塔式法生产的,主要用于磷肥生产,现由一些接触法硫酸厂副产。接触法硫酸厂主要生产98%或93%的硫酸。98%的硫酸密度最大,20℃为1836kg/m3;无水硫酸的密度反而稍降。对发烟硫酸来说,含游离三氧化硫62%时密度最大,20℃为2003kg/m3。
表3.1 各种工业硫酸的组成
3.1.1.3 硫酸的生产方法和原料
目前广泛使用接触法生产硫酸,生产过程通常包括以下几个基本步骤:
含硫原料→原料气的生产→含二氧化硫的炉气→炉气净制→净化炉气→二氧化硫催化转化→含三氧化硫气体→成酸→硫酸
制酸原料来源较广,硫化物矿、硫磺、硫酸盐、含硫化氢的工业废气,以及冶炼烟气等都可作为硫酸生产的原料。其中以硫铁矿和硫磺为主要原料。
(1)硫铁矿
硫铁矿是硫元素在地壳中存在的主要形态之一,是硫化铁矿的总称。硫铁矿分为普通硫铁矿和磁硫铁矿两类。普通硫铁矿的主要成分是FeS2,纯净的FeS2多为正方晶系,呈金黄色,称为黄铁矿;另一种斜方晶系的FeS2,称为白铁矿。还有一种比较复杂的含铁硫化物,一般可用Fe n S n+1表示(5≤n≤16),最常见的是Fe7 S8,称为磁硫铁矿或磁黄铁矿。
同种矿石,含硫量越高,焙烧时放热量越大;在相同含硫量时,磁铁矿比普通硫铁矿放热量大30%左右。
自然界开采的硫铁矿都是不纯的,矿石中除FeS2以外,还含有铜、锌、铅、砷、镍、钴、硒、碲等元素的硫化物和氟、钙、镁的碳酸盐和硫酸盐以及少量银、金等杂质,而呈现灰色、褐绿色、浅黄铜色等不同颜色。最常见的普通硫铁矿是黄铁矿,质量分数一般为30%~50%。含硫量在25%以下,称为贫矿。根据来源不同,硫铁矿又可分为:块状硫铁矿、浮选硫铁矿和含煤硫铁矿3种。
块状硫铁矿是为生产硫酸专门开采的,或在开采硫化铜矿时取得的,主要成分为FeS2,另外还含有铜、铅、锌、锰、砷、硒等杂质。块状硫铁矿入焙烧炉前,应先进行破碎、筛分等预处理。
与铅、锌、铜等有色金属硫化物共生的硫铁矿经浮选富集了有色金属硫化物后,称为精矿或精砂,余下的以硫铁矿为主的部分,称为尾砂。由于矿石经过研磨和浮选,尾砂粒度很小,含水较多且易燃。尾砂再经浮选,把废石分出,所得含硫量较高的硫铁矿称为硫精砂或称浮选硫铁矿。
含煤硫铁矿也称黑矿,与煤共生,在采煤时同时采出。这种硫铁矿中含少量煤,一般不单独使用,常和其他原料配合使用。
(2)硫磺
硫磺是制造硫酸使用最早而又最好的原料。硫磺的来源有天然硫磺、从石油和天然气副产的回收硫磺以及用硫铁矿生产的硫磺。
天然硫磺是用高压热水熔融地下硫磺矿的方法开采的。回收硫磺是从石油和天然气中的硫化氢转化回收的。由于石油和天然气开采量急剧增长,对环境污染的控制和生产工艺的进步,以及高效加氢脱硫方法的发展,回收硫磺的产量逐年增加。
天然硫磺和回收硫磺的纯度很高,可达99.8%以上,有害杂质的含量很少。作为生产硫酸的原料,不需要复杂的炉气净制工序,还可以省掉排渣设备,工艺流程短,生产费用低,生产中热能可合理利用,对环境污染少。
