任务解析
2026年01月14日
任务解析
1.实验室制备氯气
实验室利用二氧化锰和浓盐酸制备氯气的化学方程式如下:
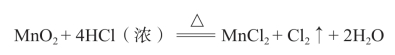
实验过程中为了制备纯净干燥的氯气,可采用如下方法:
(1)将产生的气体通入饱和食盐水,以除去反应中挥发出的氯化氢气体。
(2)再将气体通入浓硫酸溶液,以除去反应中产生的水分。
(3)由于氯气的密度比空气的大,故应采用向上排空气法收集气体。
(4)由于氯气有毒,故通入氢氧化钠溶液中以吸收多余的氯气。化学方程式为
![]() (https://www.daowen.com)
(https://www.daowen.com)
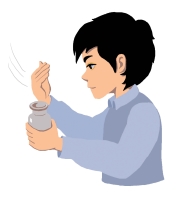
图3-3 实验室闻气体气味的方法
在实验过程中,闻氯气时应该采用一扇、二飘、三闻的方法。即用手在瓶口轻轻扇动,仅使极少量的氯气飘进鼻孔,仔细辨别气味。注意:实验室无论闻什么气体都应采用这种方法。
2.氯气性质的检验
氯气溶于水后,部分氯气分子与水反应生成了次氯酸,HClO具有极强的氧化性,能使有机色质褪色,因此,干燥的红色布条不褪色,而湿润的则褪色。
灼热的铜丝在氯气中剧烈燃烧,瓶里充满棕黄色的烟(氯化铜晶体微粒),再注入少量水于瓶中,出现蓝绿色溶液。
3.氯离子的检验
三支试管中分别放入2 mL稀盐酸、2 mL氯化钠溶液和2 mL碳酸钠溶液,分别滴加硝酸银溶液后,三支试管均产生沉淀,分别是氯化银沉淀和碳酸银沉淀,分别滴加稀硝酸后,碳酸银沉淀溶解,而氯化银沉淀不溶解。化学方程式如下: