任务解析
2026年01月14日
任务解析
一、硫的物理性质、化学性质的检验
固体硫不溶于水,微溶于酒精,易溶于二硫化碳。
硫单质能与铁等金属发生反应,当用灼热的玻璃棒触及硫粉与铁粉的混合物时,混合物呈红热状态,并有火星产生;移开玻璃棒,反应仍在进行,说明该反应放热。化学方程式如下:
![]()
灼热的硫粉在纯氧气中燃烧时,会产生明亮的蓝紫色火焰,生成一种有刺激性气味的气体——SO2。
二、二氧化硫性质的检验
二氧化硫是一种酸性气体,溶于水后生成亚硫酸,能使湿润的蓝色石蕊试纸变红色。同时,二氧化硫具有漂白性,可使品红溶液变无色,这是因为二氧化硫的水溶液可以和某些色素化合成无色化合物,但这种无色化合物不稳定,受热易分解而恢复为原来的颜色,因此,将二氧化硫漂白褪色的品红溶液加热又恢复了原来的红色。
三、浓硫酸特性的检验
浓硫酸极易溶于水,并放出大量的热。因此在配制硫酸溶液时,切勿将水倒入浓硫酸中!应该在搅拌下将浓硫酸缓缓倒入水中,以免造成烫伤。(https://www.daowen.com)
浓硫酸具有极强的脱水性和腐蚀性,能使白纸炭化,因此蘸取浓硫酸在白纸上写字后,字迹处会变黑,使用时要注意安全。
浓硫酸还具有强氧化性,能和不活泼的金属铜发生反应,化学方程式如下:
![]()
生成的硫酸铜溶于水后呈蓝色。
四、硫酸根离子的检验
在三支试管中分别放入2 mL稀硫酸、硫酸钠溶液和碳酸钠溶液,分别滴加氯化钡溶液后,三支试管中均产生白色沉淀,分别是硫酸钡沉淀和碳酸钡沉淀,逐次滴加稀硝酸后,碳酸钡沉淀溶解,硫酸钡沉淀不溶解。化学方程式如下:
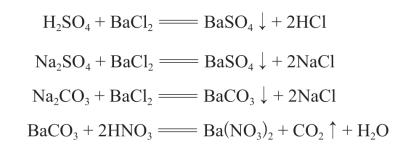
观察思考
浓硫酸与稀硫酸的氧化性是否相同?为什么?
