任务解析
2026年01月14日
任务解析
一、硅酸的制取
由于硅酸钠溶液呈碱性,滴加无色的酚酞溶液后变红色。滴加盐酸后,生成了白色的硅酸凝胶,故红色逐渐消失。化学方程式如下:
![]()
二、硅酸酸性的检验
在锥形瓶A中,稀盐酸与碳酸钠固体反应,生成了CO2,同时由于盐酸会挥发出少量HCl,因此将生成的气体通过碳酸氢钠溶液以吸收HCl而只剩下CO2,当CO2通过试剂瓶C时,与饱和的硅酸钠溶液反应,生成了白色的硅酸凝胶,这说明碳酸的酸性强于硅酸。化学方程式如下:(https://www.daowen.com)
![]()
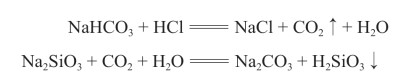
课外实验
水中花园
在水槽或大玻璃容器的底部铺一层洗净的细沙(约1 cm厚),再放置一块形状像假山的石头或炉渣。向容器中注入过滤后的质量分数为20%的Na2SiO3溶液(约占容器体积的3/4),用玻璃棒将底部的沙子摊平。静置,待液面停止晃动后,用镊子分别将各种盐的固体(红豆粒大小),如硫酸铜、氯化锰、氯化钙、氯化钴等,投入槽底细沙的不同位置。不久,可以看到,在投入了盐的地方,有晶体慢慢从水底的细沙中向上“生长”。几小时后,就形成美丽的“水中花园”。
