脂代谢紊乱
第二节 脂代谢紊乱
病史摘要
患者,男,20岁,因反复发作劳力性胸痛、胸闷7年余,近1周加重入院。患者于13岁开始反复出现活动后心前区闷痛,有时胸痛向左肩背部放射,每次发作持续3 ~ 10分钟,休息可缓解。7年来曾多次因劳力性胸痛到院诊治,近一周上述症状明显加重,胸痛、胸闷发作时间延长,休息难缓解,再次来院就诊。
体格检查:BP 110/70 mm Hg(1 mm Hg=0.133 k Pa),神志清,发育良好。手掌指关节膨大,双手指蹼、双肘部伸侧和肘关节处、背部、双足趾蹼、双膝部和膝关节处、骶尾部、臀部、双跟腱部均可见大面积黄色结节性皮损,大小不一,直径0.1 ~ 5.0 cm,多数为2 cm。心界达域值,心率110次/分,律齐,未闻及病理性杂音。双肺呼吸音粗,未闻及啰音。腹部等检查未见异常。
实验室检查:血白细胞计数和分类、血红蛋白、血小板正常,尿常规及肾功能正常。生化:ALT(丙氨酸转氨酶)40 U/L,AST(谷草转氨酶)94 U/L,LDH(乳酸脱氢酶)884 U/L。血糖(FBS)4.3 mmol/L, TC 19.27 mmol/L,TG 1.73 mmol/L。高密度脂蛋白胆固醇(HDL—C) 0.89 mmol/L,低密度脂蛋白胆醇(LDL—C)17.37 mmol/L,极低密度脂蛋白胆固醇(VLDL—C)1.01 mmol/L。
心电图提示:下壁病理性Q波、ST—T变化;胸片无明显异常,超声心动图示左心室稍增大,冠状动脉造影(CAG)检查示左侧冠状动脉前降支完全闭塞,左回旋支近端狭窄约75%,右侧冠状动脉主干狭窄约80%。
家族史:父母非近亲结婚,患者系第3胎,足月顺产,有2个姐姐和1个妹妹,其大姐总胆固醇(TC)8.52 mmol/L、三酰甘油(TG) 1.64 mmol/L,VLDL—C 0.61 mmol/L。血压和心电图正常。二姐今年初发生胸闷和胸痛,临床表现同本例患者,因家境贫困未诊治,发病当日即心源性猝死。其妹妹在沪打工,未能前来检查。其父亲40岁死于心脏病。其母亲TC 7.18 mmol/L、TG 2.46 mmol/L、VLDL—C 0.91 mmol/L,血压和心电图正常。其舅舅TC 4.95 mmol/L、TG 1.39 mmol/L、VLDL—C 0.51 mmol/L,血压正常。心电图示下壁和左室壁ST段压低,合并T波变化。其大姐、妹妹、母亲、舅舅尚无胸痛、肥胖、高血压表现,其外公和外婆已故,外婆生前有黄脂瘤表现。
诊断解析
从该患者的脂代谢相关指标来看,其脂代谢紊乱的情况非常明确,同时,从体格检查的结果来看,该患者还有脂质在真皮内沉积引起黄色瘤(黄瘤、黄疣)的体征。经询问其家族史,发现包括其大姐、母亲、舅舅均有高脂血症的实验室检查数据,其已故的外婆也有黄脂瘤的临床表现,可见该患者患有家族型的脂代谢紊乱病征。
下一步需要在其家族中进一步细化脂代谢的实验室检查,以明确其分型,并进行针对性的治疗,以预防或推迟各家族成员动脉粥样硬化的发展趋势,降低发生心脑血管意外事件的风险。
知识拓展
1. 血脂的定义 血浆所含脂类(脂质)统称血脂(lipids)。主要包括:总胆固醇(TC)(游离胆固醇加上胆固醇酯)、中性脂肪(主要是三酰甘油,TG)、非酯化脂肪酸(游离脂肪酸,FFA)、磷脂、糖脂。血脂不溶于水,以脂蛋白的形式运输。
血脂的来源包括:食物脂类、体内合成脂类、脂库动员。脂肪组织是贮存脂肪的重要场所,以皮下、肾周围、肠系膜、大网膜等处贮存量最多,称为脂库。其去路为氧化供能、进入脂库贮存、构成生物膜和转变为其他物质。脂质中TG的主要作用是能量储存和能量产生,胆固醇的主要作用是提供甾体激素合成、细胞膜、胆酸合成的原料。
2. 脂蛋白分类和组成特征及其功能 血浆中脂质是和蛋白质结合成脂蛋白这一类大分子复合物形式存在,可使非水溶性脂类分散在血浆中,使血浆清晰而不混浊。血浆脂蛋白主要由蛋白质、三酰甘油、磷脂、胆固醇及胆固醇酯组成(表3—2)。绝大多数脂蛋白是在肝脏和小肠合成,并主要经肝脏进行分解代谢。
表 3—2 主要脂蛋白的分类和组成(超速离心法与电泳法分离血浆脂蛋白的相应关系)
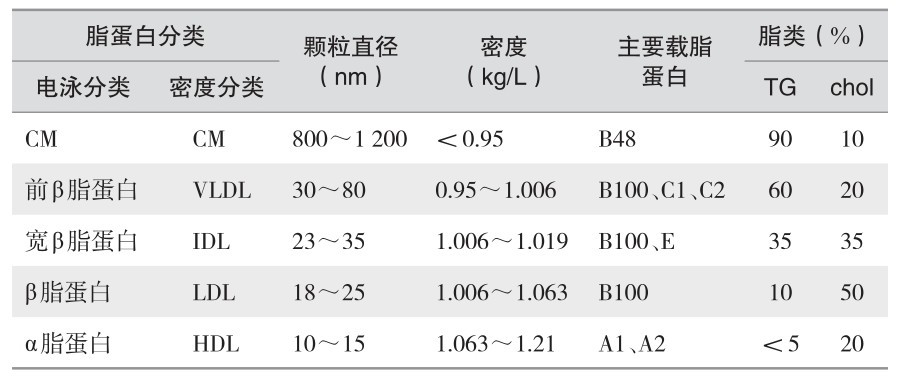
CM主要功能是转运外源性TG及chol,LDL主要功能是转运内源性TG,LDL主要功能是将肝合成的内源性chol转运至肝外组织,HDL主要功能是参与chol的逆向转运。
另外,在1963年Berg发现并命名了脂蛋白(a)[Lp(a)]。Lp(a)的核心部分由TG、PL、chol、CE等脂质和Apo B100组成,结构类似LDL,且含有特异性抗原成分Apo(a),Lp(a)中1分子Apo B通过二硫键与1分子Apo(a)共价结合,Apo(a)与PLG(纤溶酶原)具有高度同源性,肝脏是Apo(a)合成的主要场所。超速离心时Lp(a)密度涵盖LDL与HDL范围,多数密度在1.050 ~ 1.100 kg/L之间,Lp(a)是一类独立的由肝脏合成的脂蛋白,其分解代谢可能主要经非特异途径(非LDL受体途径),对Lp(a)分解代谢机制了解较少,Lp(a)是动脉粥样硬化的独立危险因素,且与血栓形成密切相关。
3. 载脂蛋白分类和组成特征及其功能 血浆脂蛋白中的蛋白质部分称为载脂蛋白(Apo),迄今已发现20余种Apo。不同脂蛋白含不同的Apo:CM含Apo B48而不含Apo B100,VLDL除含Apo B100外,还含Apo CⅠ、CⅡ、CⅢ及E,LDL几乎只含Apo B100,HDL主要含Apo AⅠ、AⅡ。
载脂蛋白的功能在结合和转运脂质及稳定脂蛋白的结构上发挥主要作用,调节脂蛋白代谢关键酶(如LPL、卵磷脂胆固醇脂酰转移酶LCAT、HL)活性,参与脂蛋白受体的识别如HDL受体、LDLR(或称为Apo B/E受体)、清道夫受体、Apo E受体(即LRP:LDL受体相关蛋白)(表3—3)。
表 3—3 各种载脂蛋白的特征、分布及生理功能
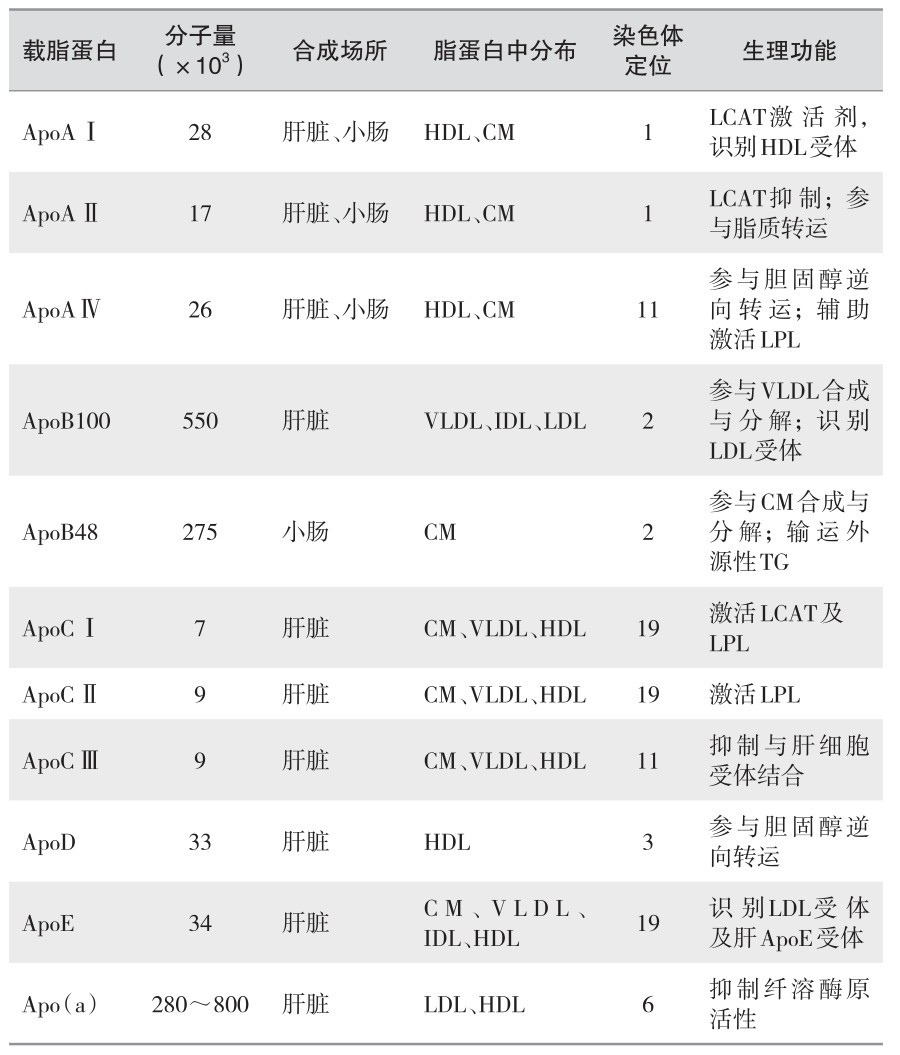
4. 脂蛋白受体和脂质转运蛋白 脂蛋白受体是一类位于细胞膜上的糖蛋白,这些蛋白质能以高亲和性方式与相应的脂蛋白配体(ligand)相互作用。目前已阐明的受体包括:LDL受体、清道夫受体、LDL受体相关蛋白、VLDL受体。
LDL受体(LDL receptor,LDL—R,LDLR)亦称为Apo B/E受体,为Goldstein和Brown于1973年发现,并因此荣获1985年诺贝尔医学奖。LDL—R是一种细胞膜表面的糖蛋白,成熟的LDL—R是由836个氨基酸残基组成的36面体结构蛋白,分子量约115 000,由5个不同的结构域组成。主要分布在:肝、动脉壁平滑肌细胞、肾上腺皮质细胞、血管内皮细胞、淋巴细胞、单核巨噬细胞等处。在体内LDL代谢中, LDL—R起双重作用:①清除循环中的IDL,限制LDL的生成;②介导细胞摄取LDL,增加LDL的降解。正常情况下,约2/3的LDL经由LDL—R途径清除,其中肝脏起主要作用。其他含Apo B100、E的脂蛋白如VLDL、β—VLDL均可与LDL—R结合,内吞入细胞使其获得脂类,主要是胆固醇。LDL—R通过介导LDL进入细胞内,来调节胆固醇水平,用于细胞增殖、固醇类激素及胆汁酸盐的合成等。
清道夫受体(Scavenger receptor)是Brown和Goldstein等在20世纪70年代末发现。当LDL被化学修饰(如乙酰化修饰),其与受体的结合特性发生明显改变,丧失了与LDL—R的结合能力,转而通过“乙酰化LDL—R”进入细胞。由于这类受体识别范围广,能与多种配体结合,因此现称清道夫受体。人和小鼠清道夫受体的基因位于第8号染色体,由于编码信息的不同拼接,形成了1型和2型清道夫受体。C—末端为半胱氨酸的为1型,具有短肽结构的为2型。清道夫受体有2种亚基,以三聚体存在,分子量为220 000。分布于胎盘、肝、脾等脏器的单核巨噬细胞系统。清道夫受体的配体广泛,有乙酰化修饰或氧化修饰的LDL、多聚次黄嘌呤核苷酸、多聚鸟嘌呤核苷酸、硫酸右旋糖酐、丝氨酸磷脂、内毒素等。清道夫受体的生理功能不清,由于其与多种配体结合,因此认为其与巨噬细胞功能相关,如黏附和宿主防御功能。体外实验表明,清道夫受体能介导氧化LDL(ox—LDL)进入巨噬细胞,参与动脉粥样硬化形成。
LDL受体相关蛋白(LDL receptor related protein, LRP)是Herz等于1988年发现。LRP组成及结构与LDL—R相似,可能属于残粒受体的一种。研究证明,LRP又是α2—巨球蛋白受体。LRP由4 526个氨基酸残基组成,是一种大分子量的糖蛋白(约600 000)。LRP是LDL—R基因家族中的一员,主要表达于肝脏、大脑和胎盘等组织。LRP是一种内吞性肝脏受体,能识别多种配体:① LRP是含Apo E残粒脂蛋白的受体,如VLDL、β—VLDL。② LRP是蛋白酶和蛋白酶抑制剂复合物的受体,如α2—巨球蛋白、PAI—1。③ LRP是毒素的受体,如铜绿假单胞菌的外毒素A。LRP的基因表达与LDL—R不同,它很少受细胞胆固醇负荷的影响,这是因为在LRP的启动子中没有固醇调节性反应子。
VLDL受体(VLDL receptor, VLDL—R)是新近发现的一种脂蛋白受体,其一级结构于1992年在家兔心脏首先得到阐明。VLDL—R与LDL—R类似,由与LDL—R相近的5部分组成,同源性分别为55%、52%、19%、32%、46%。人VLDL—R基因定位于第9号染色体,小鼠VLDL—R则位于第19号染色体。人VLDL—R分布于骨骼肌、肾脏、脑组织和脂肪组织,在肝脏仅见极低水平的受体m RNA。VLDL—R仅对含Apo E的脂蛋白有高亲和性,对LDL则呈现低亲和性。与LDL—R不同,VLDL—R不受胆固醇负反馈抑制。VLDL—R的生理功能尚不清楚,可能与内源性TG从肝脏转移至肌肉与脂肪组织有关。VLDL—R在脂肪细胞中多见,可能与肥胖成因有关。
5. 高脂蛋白血症 高脂血症是指血浆中chol和(或)TG水平升高,高脂血症实际上是血浆中某一类或某几类脂蛋白水平升高的表现,严格说来应称为高脂蛋白血症(hyperlipoproteinemia)。近年来,已逐渐认识到血浆中HDL—C降低也是一种血脂代谢紊乱。因而,有人建议采用脂质异常血症(dyslipidemia),并认为这一名称能更为全面准确地反映血脂代谢紊乱状态。
(1) 高脂蛋白血症的分型
1) 按病因分型:①继发性高脂蛋白血症:指某些原发病在病理演变过程中造成脂蛋白代谢紊乱,而继发出现高脂蛋白血症。如糖尿病、肾病综合征、甲状腺功能减退症等。②原发性高脂蛋白血症:指在排除了继发性高脂血症后,即可诊断为原发性高脂血症。已知部分原发性高脂血症是由于先天性基因缺陷所致。
2) 从临床角度分型(简易分型):①高胆固醇血症:血清TC水平增高。②混合型高脂蛋白血症:血清TC与TG水平均增高。③高甘油三酯血症:血清TG水平增高。④低高密度脂蛋白血症:血清HDL—C水平减低。
(2) 脂蛋白血症的分型及特征:见表3—4。
表 3—4 脂蛋白血症的分型及特征
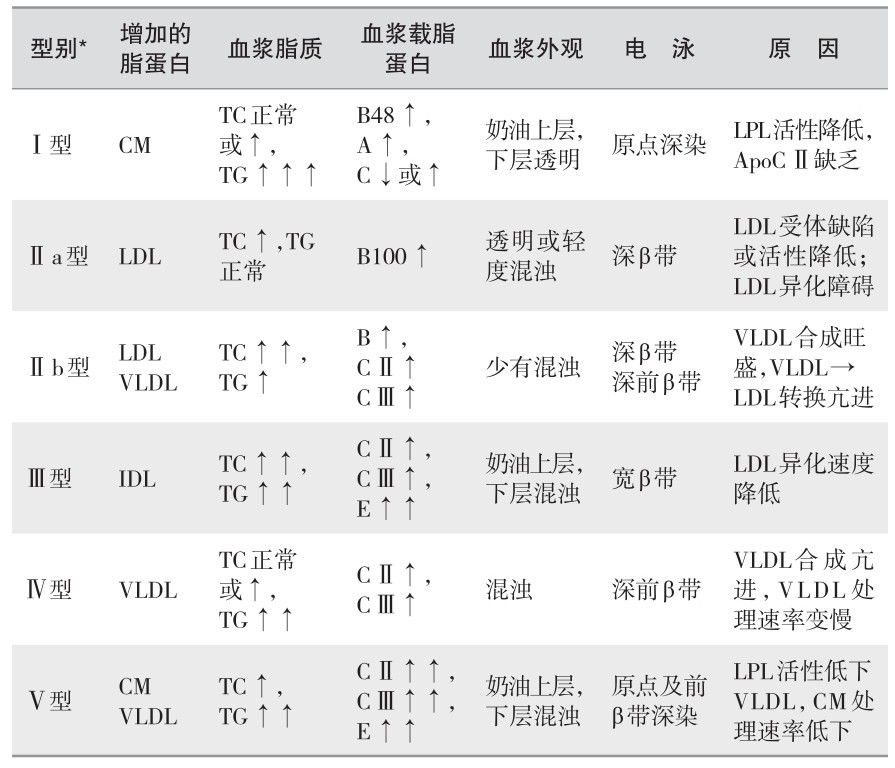
注:*除Ⅰ和Ⅴ型易发胰腺炎外,其余各型均易发冠心病。
(3) 高脂蛋白血症的基因分型法:见表3—5。
表 3—5 高脂蛋白血症的基因分型法

(续表)
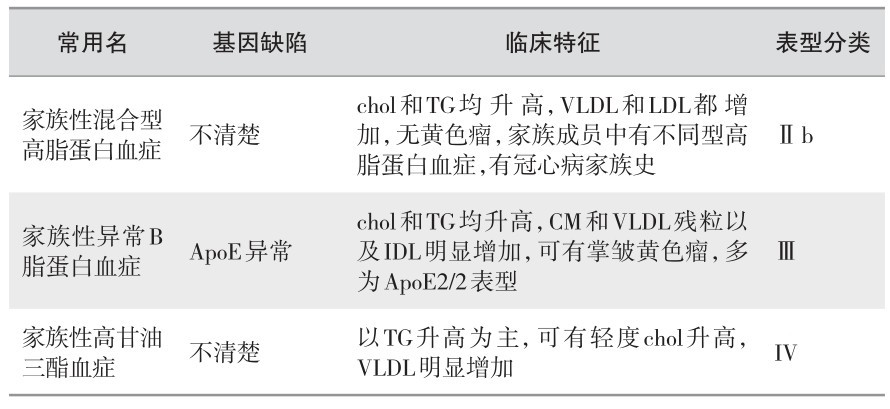
诊断思路
脂代谢紊乱的诊断主要是根据患者的临床表现、实验室检查及相关基因检测来开展。
1. 高脂蛋白血症的临床表现 多数无任何症状和异常体征,常常是在进行临床血脂检查时被发现。脂质在真皮内沉积引起黄色瘤(黄瘤、黄疣),脂质在血管内皮沉积所引起的动脉粥样硬化,产生冠心病和周围血管病等,40岁以下出现明显角膜老年环或眼底出现“番茄酱”样高脂蛋白血症性视网膜。另外,部分患者也可出现肝脾肿大、反复腹痛(胰腺炎)等症状。
黄色瘤(xanthoma)是一种异常的局限性皮肤隆凸,其颜色可为黄色、橘黄色或棕红色,多呈结节、斑块或丘疹形状,质地一般柔软。主要是由于真皮内集聚了吞噬脂质的巨噬细胞(泡沫细胞),又名黄色瘤细胞所致。根据黄色瘤的形态、发生部位,一般可分为以下几种:扁平黄瘤、睑黄瘤、结节性黄瘤、发疹性黄瘤、腱黄瘤、掌黄瘤及播散性黄瘤病。
2. 原发性高脂蛋白血症常见类型的诊断要点
(1) 家族性高胆固醇血症(FH):病因是常染色体显性遗传性疾患,LDL受体基因异常。血清TC和LDL—C水平明显增高,血清TG可正常或稍高,成人血清TC水平>7.8 mmol/L(300 mg/dl),16岁前青少年血清TC水平>6.7 mmol/L(260 mg/dl),血清LDL—C水平>4.9 mmol/L(190 mg/dl),可伴有腱黄瘤和早发冠心病。根据上述特点,结合患者高胆固醇血症的家族史可下此诊断。
(2) Ⅲ型高脂蛋白血症:病因是常染色体隐性遗传,纯合子载脂蛋白E(Apo EⅡ—2)基因型。血清TC和TG水平明显升高,TC 8 ~ 16 mmol/L(300 ~ 600 mg/dl),TG 6 ~ 12 mmol/L(500 ~ 1 000 mg/dl),可伴有早发睑黄瘤和皮肤黄色瘤以及早发冠心病和周围血管病。根据上述特点,结合患者超速离心法测定TC/TG的较高比值结果、基因分析证实Apo E(E2/2)纯合子的存在可下此诊断。
(3) 乳糜微粒血症:病因是罕见的常染色体显性遗传病,脂蛋白脂酶缺乏或Apo CⅡ缺乏。血清TG水平明显增高可高达22 mmol/L (2 000 mg/dl),血清TC水平轻度增高,可伴有反复不明原因的腹痛,反复发作胰腺炎、肝脾肿大和暴发性黄色瘤。根据上述特点,结合患者脂肪清除试验、测定静脉注射肝素后的LPL降解活性、测定血清Apo CⅡ水平的结果可下此诊断。
(4) 家族性高甘油三酯血症:病因是常染色体显性遗传性疾患,血清TG中至重度增高,为6 ~ 12 mmol/L(500 ~ 1 000 mg/dl),严重者常并存有糖尿病、肥胖、过量饮酒和妇女口服避孕药等。根据上述特点,结合患者家族其他成员有相似的高脂蛋白血症可下此诊断。
(5) 普通(多基因的)高胆固醇血症:病因是多个基因与环境因素之间相互作用的结果,血清TC水平轻至中度升高、无黄色瘤,其诊断有赖于排除其他各种脂质代谢紊乱。
3. 继发性高脂蛋白血症常见类型的诊断要点
(1) 糖尿病继发高脂蛋白血症:该种疾病类型的患者中,80%死于糖尿病者有动脉粥样硬化,75%为冠状动脉粥样硬化,25%为脑动脉或周围血管病,>75%住院的糖尿病患者并发有动脉粥样硬化,>50%新诊断的2型糖尿病患者有冠心病。第一型典型的“糖尿病性”高甘油三酯血症,血清VLDL水平增高,甚至见乳糜微粒,TG可高达28 mmol/L;疹状黄色瘤,脂血性视网膜病;对无脂膳食和胰岛素的治疗反应良好。第二型血清VLDL增高,但无乳糜微粒。第三型VLDL轻至中度增高,多见于肥胖者,糖尿病控制后血清TG下降可接近正常。
(2) 肥胖继发高脂蛋白血症:肥胖是指体内脂肪过多的堆积,体重超过标准体重20%者。肥胖分为单纯性肥胖和继发性肥胖两类:单纯性肥胖多发生在过量摄食及较少运动者;继发性肥胖多继发于内分泌代谢紊乱性疾病,如下丘脑或垂体、胰原性疾病等。肥胖时, FFA增加与胰岛素抵抗促使胰岛素分泌亢进,而引起TG水平升高,导致VLDL、TG和s LDL增加。
体重指数(BMI)=体重(kg)/身高(m)2,此公式已被广泛采用,我国成人正常BMI为19 ~ 24,BMI≥24为超重,BMI≥28为肥胖。中心型肥胖判断标准:① WHO(1999年),腰/臀比:男性>0.90,女性>0.85;和(或)BMI>30。② NCEP ATPⅢ(2001年):腰围:男性>102 cm;女性>88 cm。NCEP:美国国家胆固醇教育计划(National Cholesterol Education Program),ATPⅢ:成人治疗指导原则第3次报告(Adult Treatment Panel Ⅲ)。
(3) 甲状腺功能减低继发高脂蛋白血症:由于VLDL和LDL降解减少,致血清LDL水平增高,主要表现为Ⅱa型。
(4) 肾脏疾患继发高脂蛋白血症:尿毒症时由于脂蛋白脂酶活性降低,表现为IV型高脂蛋白血症;肾病综合征时肝脏分泌LDL增多和VLDL降解减少,表现为Ⅱa或Ⅱb型。
(5) 酗酒继发高脂蛋白血症:每日大量饮酒可产生高甘油三酯血症,严重者可伴疹状黄色瘤、脂血性视网膜病,甚至胰腺炎。
(6) 口服避孕药继发高脂蛋白血症:含雌激素的口服避孕药可增加肝脏分泌VLDL,大多数妇女因同时也伴有VLDL降解增加,一般血脂变化不大。少数妇女可出现血清TG水平明显增高,停药后增高的TG可恢复。
4. 临界高胆固醇血症的诊断 其主要病因特点是基础值偏高,可能是由于人体内胆固醇转化为胆汁酸延缓,肝内胆固醇含量升高,继而抑制LDL受体活性;高胆固醇摄入,可能与肝脏胆固醇含量增加、LDL受体合成减少有关;高饱和脂肪酸摄入确切的机制尚不清楚,可能与饱和脂肪酸抑制LDL受体活性有关;体重增加可致胆固醇升高,肥胖促进肝脏输出含Apo B的脂蛋白,继而使LDL生成增加;肥胖使全身的胆固醇合成增加,抑制LDL—R的合成;年龄效应,老年人的LDL—R活性减退,LDL分解代谢率降低;女性更年期影响,雌激素能增加LDL—R的活性,由于绝经后体内雌激素减少导致胆固醇水平升高。
5. 轻度高胆固醇血症的诊断 指血浆胆固醇浓度为6.21 ~ 7.49 mmol/L(240 ~ 289 mg/dl) 或LDL—C为4.15 ~ 5.41 mmol/L (160 ~ 209 mg/dl)。大多数轻度高胆固醇血症的患者,可能是由于上述临界高胆固醇血症的原因所致,同时合并有遗传基因的异常。使体内LDL分解代谢速率降低,LDL合成增加或LDL结构改变。
6. 重度高胆固醇血症的诊断 指血浆胆固醇浓度超过7.51 mmol/L (290 mg/dl)或LDL—C>5.44 mmol/L(210 mg/dl)。重度高胆固醇血症的最好例子是杂合子型家族性高胆固醇血症(FH)。在一般人群中,杂合子型FH的发病率为1/500,而重度高胆固醇血症在成人中则为5/100。重度高胆固醇血症是下列多种因素共同所致:LDL分解代谢减低,LDL产生增加,LDL—Apo B代谢缺陷,LDL颗粒富含胆固醇酯。另外还有上述引起临界高胆固醇血症的原因。大多数重度高胆固醇血症很可能是多基因缺陷与环境因素共同作用所致。
7. 高甘油三酯血症的诊断 凡引起血浆中CM和(或)VLDL升高的原因均可导致高甘油三酯血症。许多代谢性疾病、某些疾病状态、激素和药物等都可引起高甘油三酯血症,这些一般称为继发性高甘油三酯血症。进食高糖,可致血糖升高,刺激胰岛素分泌增加,出现高胰岛素血症。后者可促进肝脏合成TG和VLDL增加,因而引起血浆TG浓度升高。此外,高糖膳食还可诱发Apo CⅢ基因表达增加,使血浆Apo CⅢ浓度增高。已知Apo CⅢ是LPL的抑制因子,血浆中Apo CⅢ增高可造成LPL的活性降低,继而影响CM和VLDL中TG的水解,引起高甘油三酯血症。饮酒可增加体内脂质的合成率,减少氧化脂肪酸的比例,并增加酯化脂肪酸的比例。此外,酒精还可降低LPL的活性,而使TG分解代谢减慢。吸烟也可使血浆TG水平升高9.1%。然而戒烟后多数人有暂时性体重增加,可能与脂肪组织中LPL活性短暂上升有关,此时应注意控制体重,以防体重增加而造成TG浓度升高。缺乏体育锻炼可使血浆TG水平升高。因为锻炼可增高LPL活性,升高HDL水平特别是HDL2的水平,并增高HL活性。长期坚持锻炼,还可使外源性TG从血浆中清除增加。
基因异常所致血浆TG水平升高,包括以下情况:① CM和VLDL装配的基因异常:由于Apo B在剪接过程中有基因缺陷,造成CM和VLDL的装配异常,由此而引这两种脂蛋白的代谢异常。② LPL和Apo CⅡ基因异常:血浆CM和VLDL中的TG有效地水解需要LPL和其辅因子Apo CⅡ参与。LPL和Apo CⅡ的基因缺陷将导致TG水解障碍,因而引起严重的高甘油三酯血症。③ Apo E基因异常:Apo E2与LDL—R、LRP两种受体的结合力都差,因而造成CM和VLDL残粒的分解代谢障碍。所以ε2等位基因携带者血浆中CM和VLDL残粒浓度增加,因而常有高甘油三酯血症。
诊断应注意的问题
脂代谢紊乱诊断时必须要注意血脂项目的合理选择与应用,临床常规(包括体检)血脂检查应至少选择TC、TG、HDL—C及LDL—C这四项,只测定TC、TG不能反映患者基本血脂情况。
1. 考虑加测Apo AⅠ、Apo B的情况 ①未确定有危险因素的心脑血管病患者,常规血脂项目正常者。②中青年心脑血管病患者。③早发动脉粥样硬化家族史者。④家族成员中有低Apo AⅠ或高Apo B者。⑤高甘油三酯患者。
2. 考虑测定Lp(a)的情况 ①未确定有危险因素的心脑血管病患者,常规血脂项目正常者。②中青年心脑血管病患者。③早发动脉粥样硬化家族史者。④家族成员中有高Lp(a)者。
