线性免疫印迹法
线性免疫印迹法(line immunoassay,LIA)是目前实验室常用的检测ANA谱方法,可实现同时检测样本中的多种自身抗体。
(一)靶抗原及质控带的包被原理
1.靶抗原的包被·商品化LIA试剂盒内的单人份膜条,通常依据靶抗原的特性,将不同的靶抗原包被在合适材质的载体膜上,以保证膜条检测的敏感性和特异性,完成患者样本内多种不同自身抗体的检测。通常情况下,包被的抗原可分为天然抗原和重组抗原。
(1)天然抗原:采用物理和化学方法裂解动物组织,从裂解液中提取并经亲和层析纯化制备相应的天然抗原。此种方法获得的抗原容易保持蛋白(抗原)构象和天然修饰(磷酸化、甲基化、糖基化等)。
(2)重组抗原:采用基因工程技术反转录获得相应的cDNA,用杆状病毒系统在昆虫或动物细胞中表达,克隆出特定蛋白(抗原)。
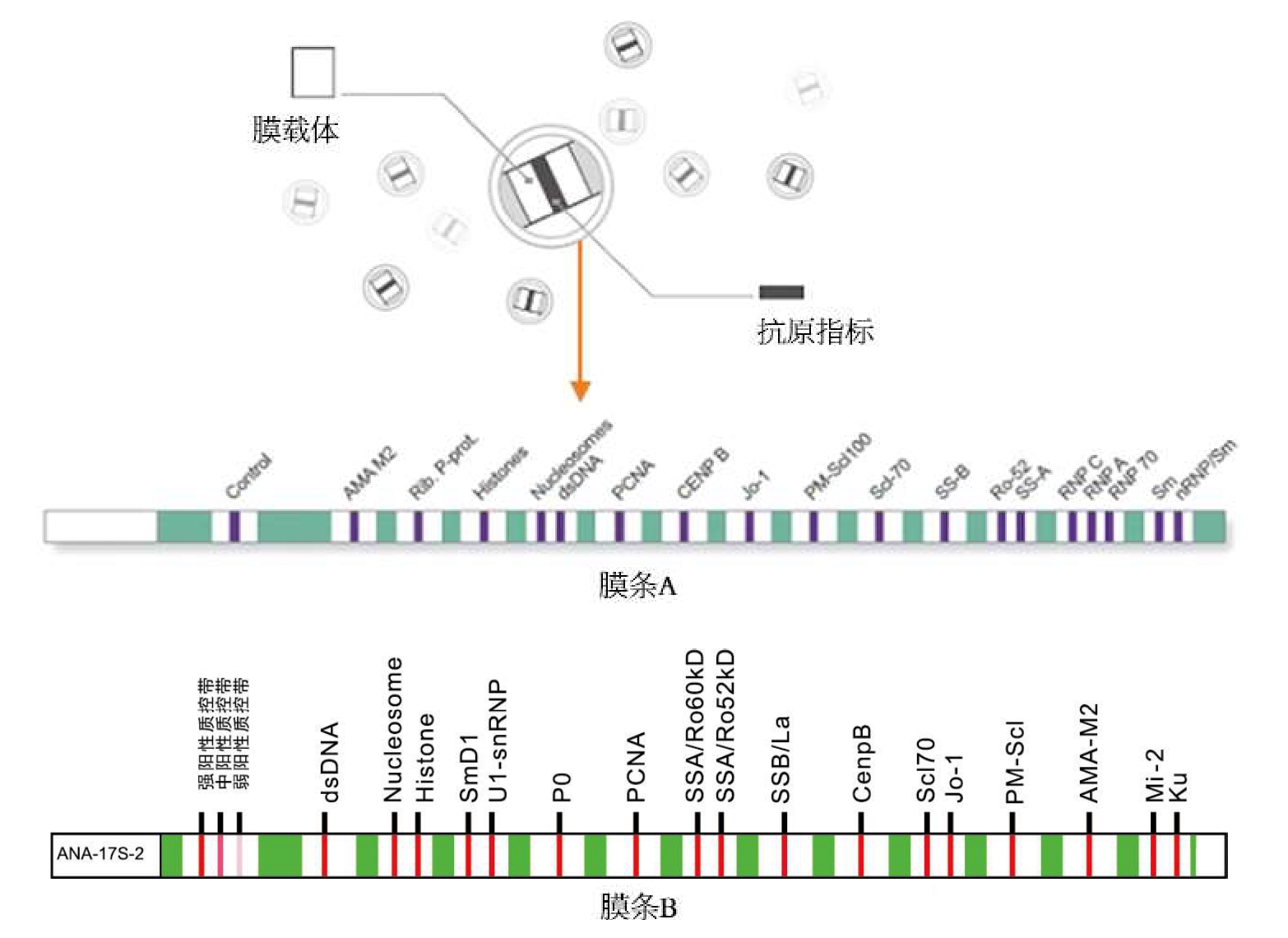
采用喷涂技术将抗原包被在适宜的载体膜上,然后将不同的模块组合在不同的膜条上,形成不同种类的检测膜条(图1—2—5)。
2.质控带的包被·每个检测膜条均包含一个质控带检测模块,用以监控该膜条的整个实验过程是否正常。目前LIA商品化试剂盒质控带主要有2种(图1—2—5),其包被的质控物以及质控物的判读标准有所不同。
(1)质控带包被物:①包被多克隆抗人IgG抗体(如欧蒙印迹法),在加入血清样本后,质控带中的多克隆抗人IgG抗体与血清中的IgG结合,所形成的复合物再与酶标记二抗结合,在底物液温育后出现颜色反应。若漏加样本、酶标记二抗或底物中任何一种,则无颜色反应。②包被人血清IgG(如亚辉龙印迹法),在加入酶标记二抗后,质控带中的人血清IgG与酶标记二抗结合,在底物液温育后出现颜色反应。若漏加酶标记二抗或底物,则无颜色反应。
(2)质控带判读标准:①单质控带,如图1—2—5膜条A。若实验过程正常,质控带的着色等级应为3+,说明该膜条的靶抗原结果均可信;其他结果如无质控带、质控带着色等级为1+或2+等均说明实验结果异常,膜条的靶抗原结果均不可信,应重复实验或检测样本IgG的含量是否正常。②多质控带,如图1—2—5膜条B。若实验正常,强阳性质控带的着色等级应为3+,中阳性质控带的着色等级应为2+,弱阳性质控带的着色等级应为1+,说明膜条的靶抗原结果均可信;其他结果如无质控带、三条质控带着色等级不满足强阳性>中阳性>弱阳性等都表示实验结果异常,此时膜条靶抗原结果均不可信,应重复实验。(https://www.daowen.com)
(二)检测原理
检测时,样本中特定抗体与相应靶抗原结合形成抗原抗体复合物,再加入碱性磷酸酶标记的抗人IgG(或IgM)抗体,结合后形成抗原抗体—酶标记二抗免疫复合物,最后加入底物液(5—溴—4—氯—3—吲哚基磷酸盐/四唑硝基蓝),产生灰色颜色反应(图1—2—6A)。因样本中不同抗体含量不同,与载体膜上相应靶抗原结合程度不同,可得到颜色深浅不一的条带,通过专业软件分析,可得到不同数值的着色强度,对应不同的着色等级[0,(±),1+,2+,3+],实现对结果的半定量判读。
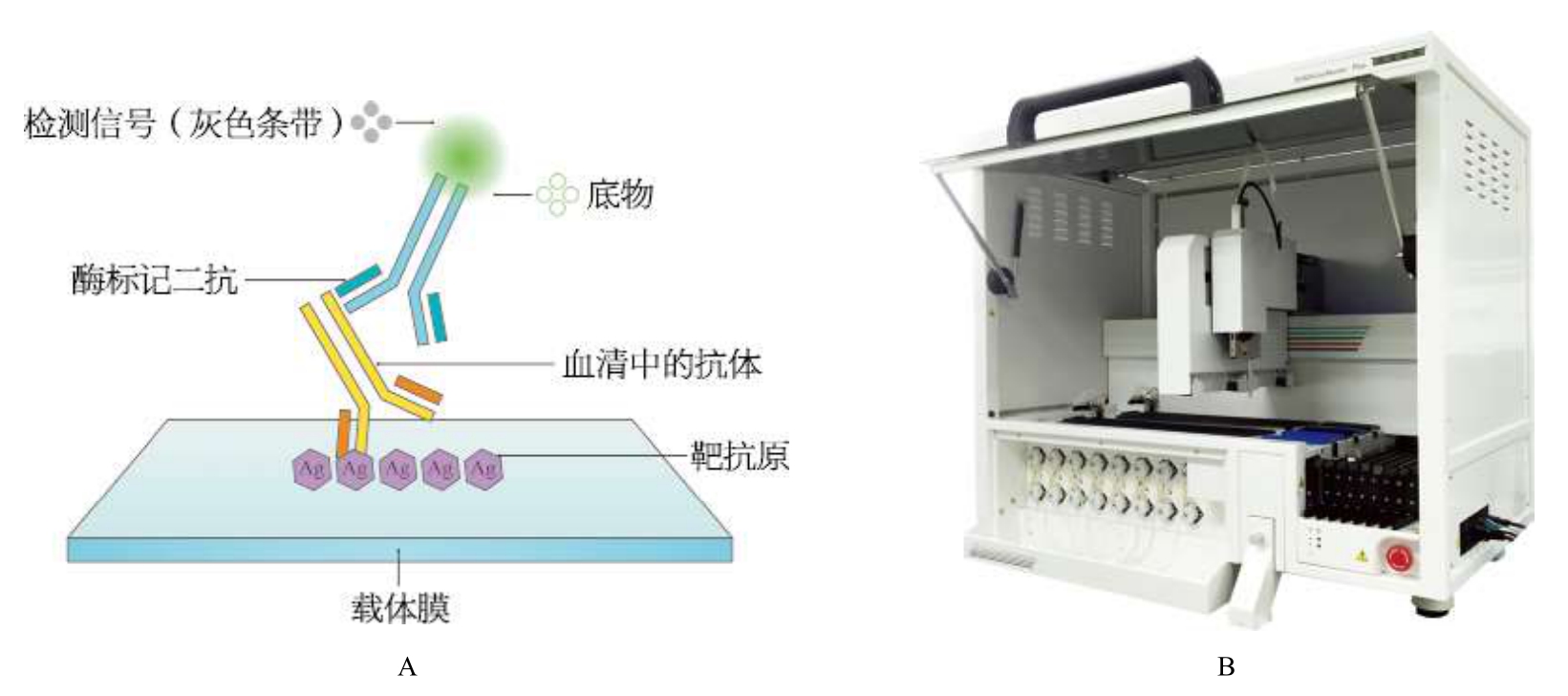
图1—2—6 免疫印迹法检测抗核抗体反应原理图及全自动免疫印迹仪
A.免疫印迹法检测抗核抗体反应原理;B.ELMP全自动免疫印迹仪[来源于欧蒙医学诊断(中国)有限公司]
目前,免疫印迹法已实现整个实验过程的自动化,如欧蒙全自动免疫印迹仪(EURO Line Master Plus,ELMP)可完成从加样、检测、判读到数据上传全自动化,减少人为操作和结果判读误差(图1—2—6B)。