补肾软坚方药调节内皮细胞通透性的机制研究
动脉粥样硬化是一种脂质代谢失衡性疾病,也是一种进程缓慢的、机制复杂的血管炎症性疾病。疾病产生初期由于炎症反应激活造成了内皮细胞损伤,单核细胞黏附于受损内皮表面,并迁移到内皮下形成巨噬细胞,巨噬细胞吞噬修饰的脂质形成泡沫细胞。血管内皮通透性正常对维持循环系统的稳定及各器官生理功能起着十分重要的作用,生理条件下受机械力和生物信号的精确调节,其中,RhoA/ROCK通路在心血管疾病中的作用越来越受到重视。本实验探讨补肾软坚方药保护内皮细胞屏障功能的分子机制,补肾软坚方药是否通过RhoA/ROCK通路调节细胞通透性。
(一)材料与方法
1.细胞株 人脐静脉细胞融合细胞株EA.hy926(No.CRL-2922)购自美国标准生物品中心(American Type Culture Collection,ATCC)。
2.主要试剂 FITC-Phalloidin,ROCK1,P-MLC,HRP-goatanti-mouseIgG,HRPgoatanti-rabbit IgG,总RNA提取试剂盒。
3.方法
(1)EA.hy926细胞的培养 同第四章第四节。
(2)补肾软坚方药含药血清的制备 同第二章第三节。
(3)免疫荧光染色 同第四章第三节。
(4)Western blotting检测 ROCK1、P-MLC将各实验分组细胞弃细胞上清液后加入100μL裂解液反复吹打后,收集裂解液置于高速冷冻离心机中得待测样品。将待测样品做BCA蛋白定量及SDS-PAGE电泳实验,得各组细胞ROCK1、P-MLC的蛋白条带。
(5)Rt-PCR检测RhoA、ROCK1基因水平的表达 同第四章第二节。(见表4-4)
表4-4 目的基因及内参引物序列

本实验选择△△CT法进行数据分析:计算实验每组每个基因的平均CT值;每个样品待测基因的平均CT值减去同一样品内参的平均CT值,得到矫正CT值,即△CT;待测基因的△CT值减去基准样品的相对基因的校正CT值,得到比较结果,即△△CT;假设基因的PCR扩增效率一致且等于1时,可用2-△△CT表示待测基因的表达量与基准样品中表达量的倍数关系。
4.统计方法 Western blotting检测结果利用Image J软件处理,分析各条带面积灰度值,目的条带与内参条带的比值代表目的蛋白的表达水平,重复实验结果取得平均值。采用SPSS 18.0版本,单因素方差分析,对各组均值进行统计学处理。
(二)结果
1.补肾软坚方药对LPA诱导的细胞骨架的作用 本实验主要为了明确补肾软坚方药含药血清保护内皮细胞屏障功能是否伴随细胞形态学的变化。实验分组为:空白对照组(Control)、模型组(LPA20μM)、补肾软坚方药组(BSKS),使用荧光双重标记法,异硫氰酸荧光素(FITC)-鬼笔环肽标记细胞骨架F-actin,DAPI标记细胞核,观察各组细胞骨架F-actin的表达及分布情况。结果显示(见附录,图4-15),未经处理的空白对照组细胞膜周边表达有序的束状F-actin,而细胞质区未见明显呈极性分布的张力丝(应力纤维)形成;经LPA刺激后,诱导细胞质区形成张力丝,密集、紊乱排布,应力纤维附着于细胞膜上,外周F-actin逐渐断裂,甚至消散。LPA刺激能够促进EA.hy926细胞骨架重构,这与其他研究报道相符。补肾软坚方药(BSKS)组预干预可以明显减弱细胞重构。
为阐明补肾软坚方药调节F-actin骨架重排的分子机制,EA.hy926细胞经LPA20μM刺激后,可诱导P-MLC蛋白的表达上调,而补肾软坚方药含药血清作用后可以明显降低P-MLC蛋白表达水平(P<0.05)。与Control组相比,LPA刺激后ROCK1蛋白水平升高(P<0.05);补肾软坚方药(10%)预处理组与模型组相比较,ROCK蛋白水平受到抑制,具有统计学意义(P<0.05)。(见图4-16)
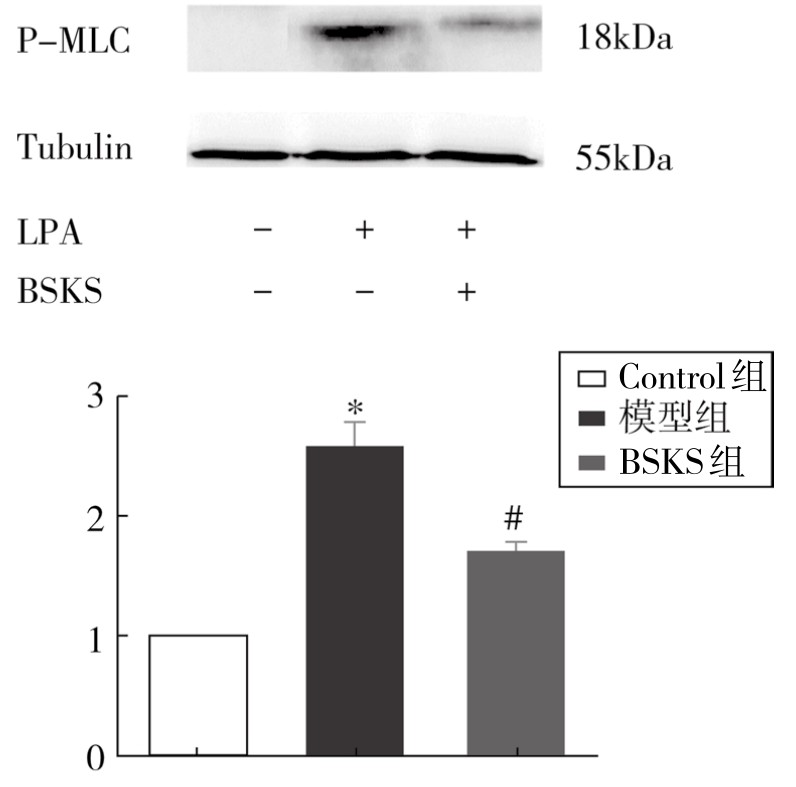
图4-16 不同组处理EA.hy926P-MLC蛋白相对表达量
注:*与Control组比较,P<0.05;#与模型组比较,P<0.05。
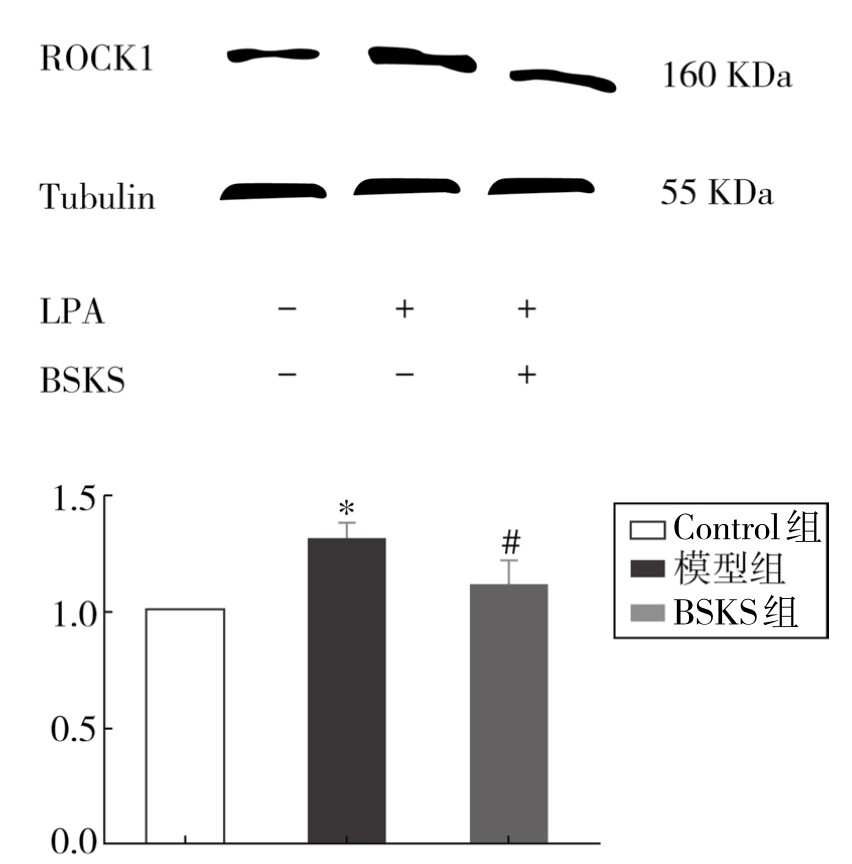
图 4-17 不同组处理EA.hy926ROCK1蛋白相对表达量
注:*与Control组比较,P<0.05;#与模型组比较,P<0.05。
2.Rt-PCR检测RhoA、ROCK1 mRNA表达的影响 与Control组相比,LPA干预24h后未见RhoAmRNA相对表达量升高,但先给以补肾软坚方药含药血清预孵育24h处理后,RhoAmRNA表达升高幅度明显降低(基因相对表达量为模型组的0.404倍),差异具有统计学意义(P<0.05)。与蛋白水平变化相一致,LPA刺激后,ROCK1 mRNA相对表达量显著升高,而补肾软坚方药作用后,明显降低ROCKmRNA表达水平(基因相对表达量为模型组的0.579倍),差异具有显著性(P<0.05)。(见图4-18)
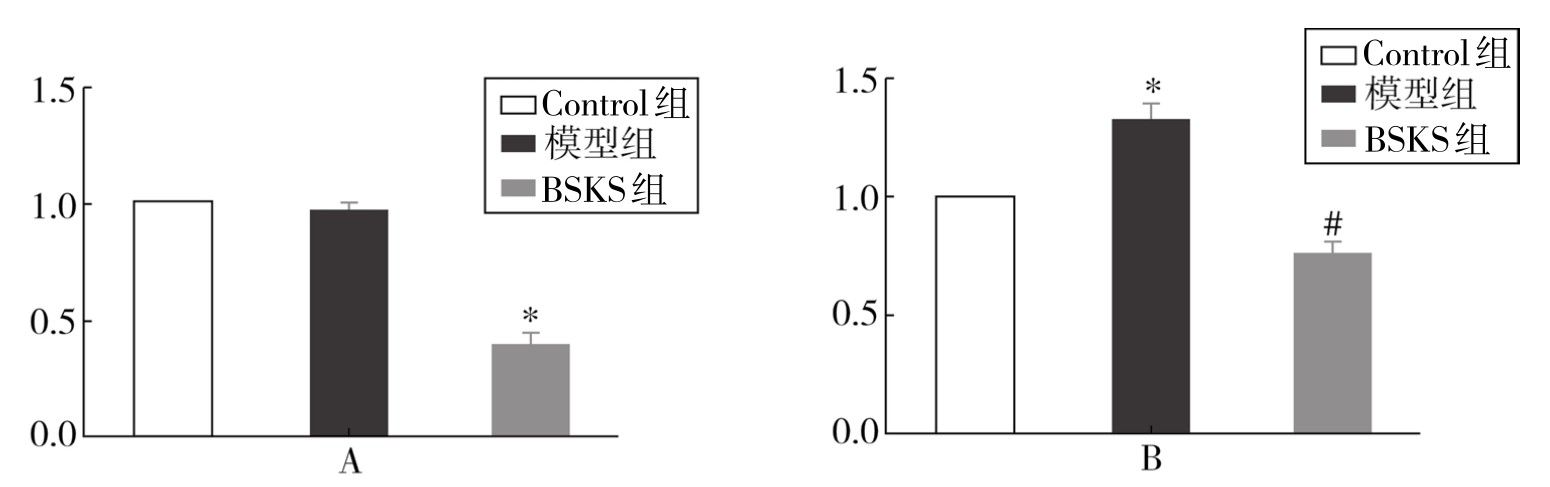
图4-18 补肾软坚方药对LPA诱导的EA.hy926RhoA、ROCK1 mRNA基因表达的影响
注:*与Control组比较,P<0.05;#与模型组比较,P<0.05;BSKS组,可明显降低RhoA、ROCK1 mRNA表达。
(三)讨论
通过对细胞骨架的研究发现,LPA刺激能够引起血管内皮细胞骨架重构,细胞内应力纤维形成增加。应力纤维的形成则有利于细胞收缩,造成细胞间隙增大,这些结果最终都会导致细胞通透性增加,这与实验中所观察到的LPA能引起FITC-葡聚糖透过率增加结果相一致。而补肾软坚方药干预则能抑制LPA介导的细胞骨架重构,从而改善内皮屏障功能。Western blotting和RT-PCR结果显示,LPA处理组RhoA、ROCK1表达明显升高,MLC磷酸化水平升高,细胞收缩与MLC磷酸化水平密切相关,MLC磷酸化水平升高,细胞收缩增强,内皮通透性增加。LPA的刺激可能通过上调RhoA和ROCK的表达,从而增加RhoA/ROCK/p-MLC通路活性,导致血管内皮高通透性。补肾软坚方药干预能下调RhoA、ROCK表达,减少MLC的磷酸化,提示补肾软坚方药可能通过该通路抑制LPA介导的内皮高通透性,保护内皮功能。
