受体类型及调节
常见受体的命名兼用药理学和分子生物学的命名方法。对已知内源性配体的受体,按特异性的内源性配体命名;对受体及其亚型的分子结构已了解的受体,按受体结构类型命名;在药物研究过程中发现,尚不知内源性配体受体的,则以药物名命名以及根据受体存在的标准命名。由于实验技术发展,特别是分子生物学技术在受体研究中的广泛应用,科学家已成功克隆出数以千计的特定受体,同时发现了许多受体亚型(受体亚型以字母及阿拉伯数字表示)。为进一步统一规范,国际药理学联合会(International Union of)(Pharmacology,IUPHAR)成立了专门的受体命名和药物分类委员会(简称NC-IUPHAR),于1998年印发了《受体特征和分类纲要》,使受体命名更为科学可信、简易可行。
受体是一个“感觉器”,是细胞膜上或细胞内能特异识别生物活性分子并与之结合,进而引起生物学效应的特殊蛋白质。大多数药物与特异性受体相互作用,通过作用改变细胞的生理生化功能而产生药理效应。目前已确定的受体有30余种,位于细胞质和细胞核中的受体称为胞内受体,可分为胞质受体及胞核受体,如肾上腺皮质激素受体、性激素受体是胞质受体,甲状腺素受体存在于胞质内或细胞核内;位于靶细胞膜上的受体,如胆碱受体、肾上腺素受体、多巴胺受体等称为膜受体,根据结构组成,膜受体又可分为G蛋白偶联受体、离子通道受体和受体酪氨酸激酶三个亚型。
(一)G蛋白偶联受体(G-protein coupled receptor,GPCR)
此类受体是人体内最大的膜受体蛋白家族,因能结合和调节G蛋白活性而得名,介导许多细胞外信号的传导,包括激素、局部介质和神经递质等,如M乙酰胆碱受体、肾上腺素受体、多巴胺受体、5-羟色胺受体、前列腺素受体以及一些多肽类受体等。这类受体在结构上都很相似,为七螺旋跨膜蛋白受体,其肽链由7个α-螺旋的跨膜区段、3个胞外环及3~4个胞内环组成(图3-5)。序列分析发现,不同GPCR跨膜螺旋区域的氨基酸比较保守,而C、N末端和回环区域氨基酸的区别较大,可能与其相应配体的广泛性及功能多样性有关。
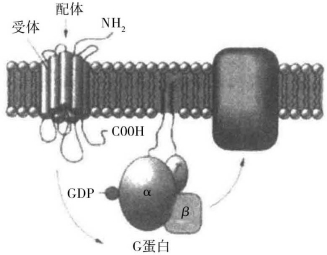
图3-5 G蛋白偶联受体示意图
(二)离子通道受体(channel-linked receptor)
离子通道受体又称离子带受体(ionotropic)(receptor),受体激动时,离子通道开放使细胞膜去极化或超极化,产生兴奋或抑制效应。离子通道有Na+、K+、Ca2+等通道。如N乙酰胆碱受体含有Na+通道,脑中的γ-氯基丁酸(GABA)受体、谷氨酸受体含有多种离子通道。此类受体由单一肽环往返4次穿透细胞膜形成1个亚基,并由4~5个亚基组成跨膜离子通道。
(三)酪氨酸激酶活性受体(tyrosine kinase-linked receptor)(https://www.daowen.com)
酪氨酸激酶活性受体为一类具有内源性酪氨酸蛋白激酶活性的单次跨膜受体,目前已发现约60种,按照受体与配体特征将其分为20个亚家族。如胰岛素受体、胰岛素样生长因子、表皮生长因子受体、血小板生长因子受体、集落刺激因子-1受体、成纤维细胞生长因子受体等都属于这类受体。
(四)核受体(nuclear receptor)
核受体是配体依赖性转录因子超家族,与机体生长发育、细胞分化等过程中的基因表达调控密切相关。配体与相应核受体结合,诱导受体的二聚化并增强其与特定的DNA序列(激素反应元件)的结合,进而导致特定靶基因表达上调(图3-6)。目前核受体超家族已有150多个成员,包括糖皮质激素受体、雌激素受体、孕激素受体、雄激素受体、维甲酸受体、甲状腺激素受体以及维生素D受体等。过氧化物酶体增殖物激活受体(PPAR)是该家族的新成员,PPAR激活后对体内脂肪与糖类代谢以及细胞生长、分化和凋亡有重要的影响。
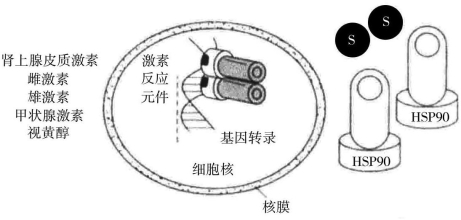
图3-6 核受体示意图
(五)其他受体
孤儿受体(orphan receptor)是一类序列已知而配体未知的蛋白受体,配体未知的GPCR称为孤儿GPCR。此外,还有孤核受体(orphan nuclear receptor)等。已发现配体的孤核受体有视磺酸X受体、视磺酸Z受体、法尼酸X受体等。通常采用反向药理学方法发现并确定其配体,即以获取受体cDNA为起点,结合功能测试,寻找相关的新配体,然后用配体和受体筛选新化合物进行新药研究,一旦找到孤儿受体的相关配体,则可能从中筛选出新的药物靶点,从而发现疗效优异的新药。
有些细胞具有多种受体,如心肌细胞具有M胆碱受体,β1、β2肾上腺素受体,H2受体等。有时一种阻断剂还可阻断多种受体,如氯丙嗪可阻断多巴胺受体、α肾上腺素受体,对胆碱受体、组胺受体和5-羟色胺受体也有较弱的阻断作用。受体除分布于突出后膜外,有些也分布于突触前膜。激动突触前膜受体可引起反馈作用,促进神经末梢释放递质,在局部调节功能平衡。
