稽查跟进和关闭
纠正措施和预防措施(CAPA)是质量管理体系中的一部分,在稽查发现的回复过程中非常重要,纠正措施是为了纠正现有违规、错误所采取的措施,其目的是防止该类事件的再次发生。预防措施是为了消除潜在造成违规、错误的原因所采取的措施,其目的是预防此类事件的发生。
稽查结束后,被稽查方应针对在稽查过程中发现的和潜在的违规问题,向稽查员提交CAPA计划。用来改正在稽查中发现的违规和潜在违规的问题。稽查方和纠正措施的执行方是相互独立的,各司其职。因此,监督纠正措施的最终执行不是稽查员的职责,CAPA是由被稽查方,如CRO公司、研究中心等来执行和完成。CAPA至少应包含:①导致稽查发现的根本原因分析。②CAPA对解决稽查发现的必要性。③CAPA计划。④已完成时间和(或)计划完成的时间。
1.启动CAPA 当被稽查方接收到正式的稽查发现时,CAPA流程即开始启动。被稽查方通过以下行动完成CAPA流程:①被稽查方通过对每个问题进行根本原因分析(root cause analysis,RCA),确定稽查发现发生的根本原因。②被稽查方基于根本原因分别确定纠正措施和预防措施。③被稽查方确定预期的CAPA关闭时间。④稽查员和被稽查方双方沟通以确认CAPA是否可被接受、是否需要进行有效性验证以及认可CAPA可以关闭。
2.根本原因和根本原因分析方法 被稽查方在回复稽查所发现的问题时,需要对重大的不依从问题进行根本原因分析,以书面的形式做好稽查回复,说明造成稽查发现的根本原因。根本原因(root cause)是指发生任何非期望的情况或出现这些问题最基本的起因,消除或减轻这些问题将预防或显著减少其所产生的影响。根本原因的分析(root cause analysis)是一种解决问题的方法,用于识别问题的根本原因。这种分析根本原因的方法是基于这样一种理念,也就是通过尝试纠正或消除根本原因来解决问题,而不是仅仅解决表面问题。通过根本原因指导CAPA,可以最大限度地减少此类问题再次发生的可能性。以下是协助被稽查方找到根本原因的常用的方法。
(1)“5个为什么”法:这是一个探索特定问题背后因果关系的提问方法。这种方法可以有效地逐步找出导致单一事件或不太复杂问题的根本原因。运用“5个为什么”方法的目标是为了确定某一个缺陷或问题的根本原因。使用的时候可能需要提问6个为什么,也可能只问3个为什么,重要的是使用这种寻找特定问题背后因果关系的提问方法,来剥离那些包含问题在内的任何外部层面。
例如,从研究中心运送到中心实验室的冰冻样本有62%在运达前已解冻。
问:为什么样本在抵达中心实验室时已不在冷冻的状态?
答:因为在运输过程中已经解冻了。
问:为什么样本会在运输过程中解冻?
答:因为运输时间超过了预期时间。
问:为什么运输时间超过了预期时间样本就会解冻?
答:因为使用的运输容器的规格是确保1~2日标本处在冰冻状态,而到达中心实验室实际需要2~4日。
问:为什么要使用规格仅确保1~2日冰冻状态的运输容器?
答:因为原项目计划是要使用中心实验室A,后来项目组决定使用中心实验室B,但是在决定更换更远的中心实验室B后并没有变更运输容器规格。(https://www.daowen.com)
问:为什么不对运输容器规格做相应变更?
答:因为当时申办方没有批准额外的费用来变更已经设计好的运输容器规格。
(2)鱼骨分析法:多用于评估和分析复杂情况下,尤其是多因素导致的不依从性。运用鱼骨图和鱼骨分析法(cause&effect/fishbone diagram)通过开会讨论,大家集思广益,按照功能类别将想法进行分类,从多种可能的原因中,找到原因。假设有一批冰冻样本在冰冻状态下,要从研究中心原封不动地运送到中心实验室,但是在实际工作中,有62%的冰冻样本在运送到中心实验室前意外地解冻了,现在要找出解冻的原因。首先将可能的原因进行分类,如图8-1所示,列出一些可能的因素:①运输因素:冰冻样本交付延迟?冰冻样本收件延迟?或者是运输途中其他未知的因素?②材料因素:是否选择了正确的运输容器?是否正确的使用了干冰?③工作人员因素:开箱时间的延迟?还是操作有误?④冰冻设备的原因:温度设定是否正确?设备校验是否正确?用鱼骨分析法将多种可能的因素一一展开,逐个分析。
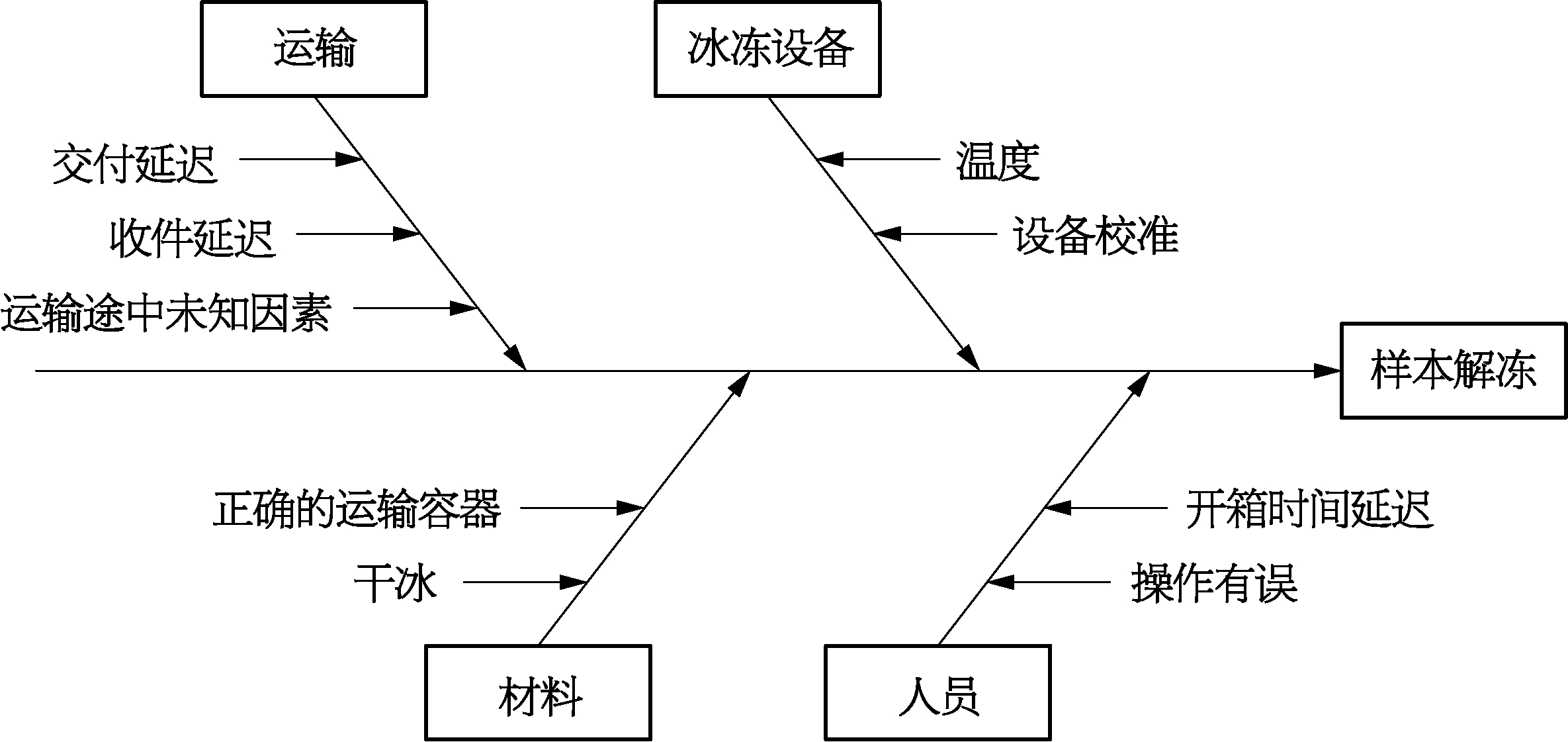
图8-1 鱼骨图和鱼骨分析法
3.CAPA具体措施 一旦确定了稽查所发现问题的原因后,被稽查方便进入到下一个环节,即描述如何制定、实施纠正和(或)预防措施的环节,以解决稽查所发现的问题。值得注意的是,并非所有的稽查问题都同时需要采取纠正和预防措施。如果一个在稽查中被发现的不依从性问题情有可原,而且无法纠正(如距离问题发生的时间已过去了太久),那么仅可以实施预防措施。同理,如果有一个不依从性问题,仅为单个孤立存在的问题(如在病例报告表中的一个单次录入错误),那么可以认为只需实施纠正措施就可以关闭这个稽查发现。当确定了CAPA回复的内容,被稽查方应提出一个切实可行的时间表。
4.有效性验证 对于解决不依从性问题,当稽查员和被稽查方双方都认可CAPA的内容和其完成的时间表,CAPA就进入稽查周期的最后阶段——有效性验证(effectiveness verification)。有效性验证是指需要有详细记录的系统化的流程来验证纠正和(或)预防措施实施的有效性。
可接受的有效性验证包括被稽查方应提供文件证明已经完成了解决稽查问题所需采取的步骤,例如,提供合理的文件来证明被稽查方所采取的行动已有效解决了稽查发现的问题,而且此类问题不会再次出现。
5.CAPA管理和跟进 为确保所有CAPA得到跟进直至关闭,质量保证部门/依从性部门应制定并实施CAPA跟进系统。在许多企业,该系统与他们的稽查管理或依从性部门的系统是有关联的。它确保在任何时候都可以明确获知CAPA内容及其状态是开放还是关闭,以满足公司管理层和(或)药品监管部门的要求。如果公司内部尚未建立CAPA追踪系统,也可以按照公司内部SOP手动记录及追踪CAPA的内容及状态。
6.CAPA的关闭 通过稽查员或稽查员所在公司与被稽查方的文字沟通记录(如通过依从性部门的文件控制和管理系统),双方对CAPA流程的所有阶段无异议,并且确认了CAPA流程和CAPA的有效性,那么就可以关闭CAPA了。稽查员所在公司和被稽查方双方应当在他们的正式文档中保留所有记录,如实地记录他们在CAPA全过程中所做的工作。对于CAPA的相关记录不应保存于药政监管当局直接可见的文档中。
7.稽查完成 当被稽查方提交了对根本原因及CAPA的初步答复,稽查可视为完成。是否继续追踪CAPA的完成情况应视稽查问题的严重程度和影响范围而定。稽查的完成并不意味着CAPA的关闭,对CAPA的跟进和CAPA的有效性验证需通过稽查员与被稽查方的持续沟通,直到双方达成共识确认CAPA完成。
如申办者或合同研究组织内部SOP中有相关要求,稽查员将提供稽查证明,以书面形式确认某项稽查的发生,根据国际临床试验质量管理规范ICH-GCP E2 8.4.4规定,稽查证明应存在研究重要文档中。稽查证明建议包含如下信息:①临床试验相关信息,如试验题目、方案编号。②稽查证明的出具日期。③稽查相关信息,如稽查对象、稽查日期、报告日期等。④稽查方法,如远程稽查、实地稽查。⑤稽查员姓名、职位和地址。⑥被稽查方姓名和工作地址。
稽查记录应根据申办者或合同研究组织的标准操作规程(SOP)进行存档。该SOP应明确稽查相关记录的保存或销毁流程、保存的地点、名称及保存期限。
