我国国家药品监督管理局(NMPA)对药物临床试验的数据核查
2026年01月16日
一、我国国家药品监督
管理局(NMPA)对药物临床试验的数据核查

2015年7月,国家食品药品监督管理总局启动了药物临床试验数据核查,坚持自查纠错从宽、被查处理从严、严惩故意造假、允许规范补正的原则,对临床试验项目实施情况进行检查,以确认试验符合药物临床试验质量管理规范(GCP)和试验方案的要求,确保受试者的安全和权益。为加强信息公开,提高工作的透明度,核查中心每个月在网站公开核查工作完成情况,设置核查进度查询,并于2016年和2017年分别发布了药物临床试验数据核查情况和药物临床试验数据工作阶段性报告。根据数据统计,截止到2018年4月,核查中心共完成480个药品注册申请的现场核查,涉及被核查机构1 390家。其中,2015年、2016年和2017年完成的核查数量分别为42、158和229个,核查进度不断加快。2017年临床试验核查工作统计结果表明,平均每个临床试验机构发现缺陷5.6条,每个生物样本分析单位发现缺陷4.0条,4个药品注册申请的临床试验数据存在真实性问题,占2017年核查总数的1.7%。图8-2列出了临床部分高频次缺陷条款分布情况(王佳楠等,2018)。
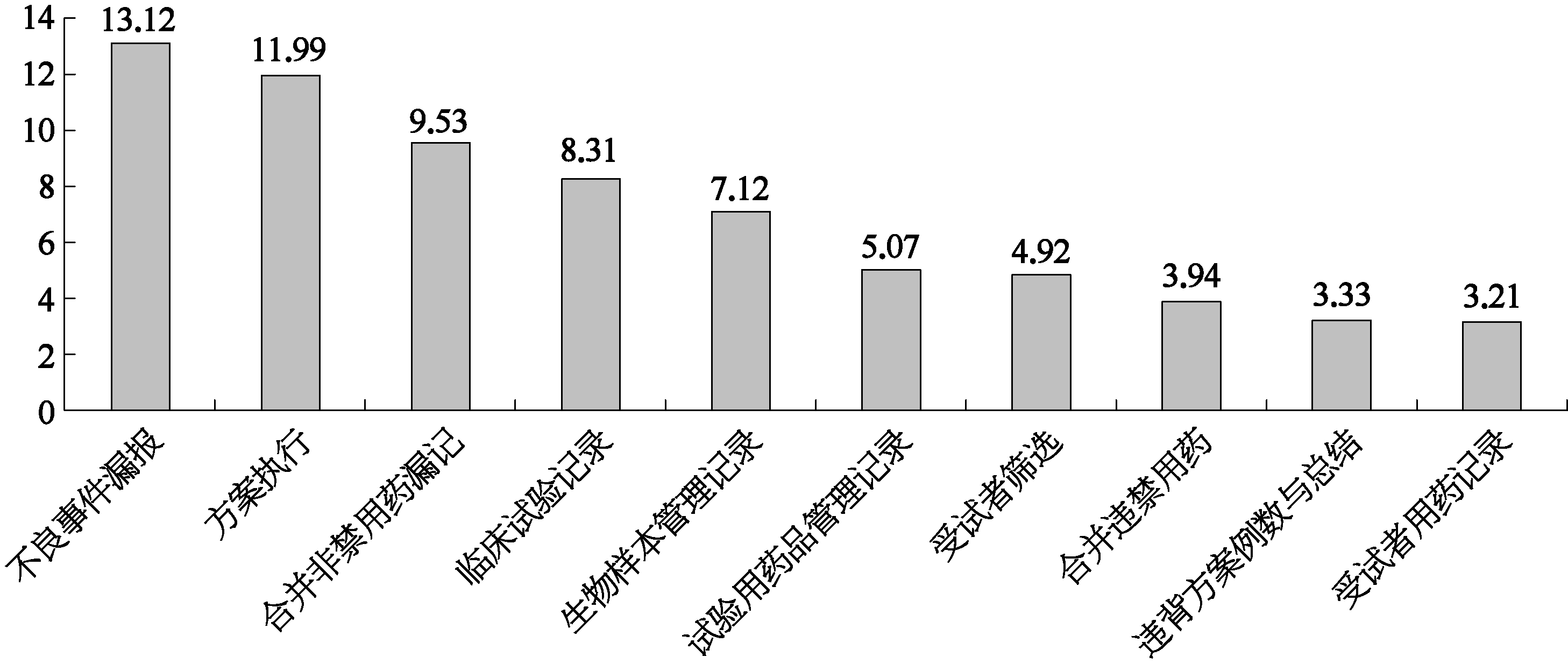
图8-2 临床部分高频次缺陷条款分布情况(https://www.daowen.com)
