《监管活动医学词典》
2026年01月16日
二、《监管活动
医学词典》

《监管活动医学词典》(Medical Dictionary for Regulatory Activities,MedDRA)是在ICH的主办下编制的医学标准术语集,用于整个监管过程(上市前至上市后)包括数据的录入、检索、评价和呈现,其用户包括监管机构和工业界。MedDRA可用于信号检测和临床症状监测,其症状包括多系统或器官,使用其多轴层次结构或通过标准MedDRA分析查询(SMQ)的特殊功能。
MedDRA约含80 000个术语,每个术语均有一个唯一的8位阿拉伯数字代码,共包含5个层次:低位语(LLT)、优选术语(PT)、高位语(HLT)、高位组语(HLGT)及系统器官分类(SOC)。MedDRA的宗旨是:①提供全球使用的国际标准。②为用户提供一个内容丰富、详细的医学标准术语。③利用其纵向结构和标准MedDRA分析查询(SMQ)帮助用户发掘、分析信号。④促进人用医疗产品国际监管信息的共享和信息沟通。MedDRA每半年更新1次,截至2018年底,来自120个国家的约5 500个组织订阅了MedDRA。MedDRA是一种多语言术语,目前有11种语言版本(包括中文版),允许大多数用户使用其母语进行操作。表12-2显示每种语言首次颁发的版本。
表12-2 MedDRA不同语言首发版本
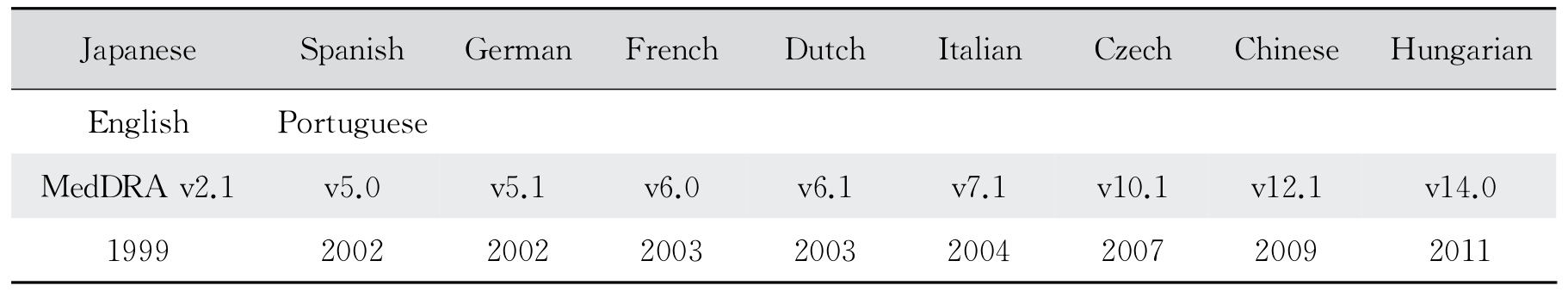
在开发和持续维护MedDRA时,ICH致力于提供统一的标准化国际医学术语,用于与人用医疗产品相关的监管沟通和数据评估。因此,MedDRA旨在用于开发周期各个阶段(如从临床试验到上市后监管)药品的注册、记录及安全监控。此外,MedDRA是ICH的电子通用技术文档(eCTD)和E2B个例安全报告电子报告表不可缺少的一部分。
