3.3.1 聚三唑非催化反应动力学
将真空处理的BAMO-r-THF共聚醚和琥珀酸二丙炔酯(BPS)按炔基/叠氮基等摩尔比混合均匀,取样品(100±15)mg,在室温至430 K温度范围内,分别采用0.1 K·min-1、0.2 K·min-1、0.4 K·min-1和0.6 K·min-1升温速率进行非等温微量热固化试验。根据BPS酯挥发特性,选取333.15 K、343.15 K、353.15 K和363.15 K四个温度进行等温试验,样品池采用膜混合反应池[42]。
1.非等温固化特征参数
在四个不同升温速率下,BAMO-r-THF共聚醚/BPS混合体系微量热曲线如图3-30所示。可以看出,实验过程中升温速率越快,BAMO-r-THF共聚醚/BPS混合体系峰温越高、峰越窄,说明固化反应所需时间与实验升温速率成正比。混合体系随着实验升温速率增加,单位时间产生的热效应变大,导致固化反应向高温方向移动、时间变短。根据图3-30微量热曲线特征,借助CALISTO PROCESSING软件获得BAMO-r-THF共聚醚/BPS混合体系固化反应数据,结果如表3-9所示。
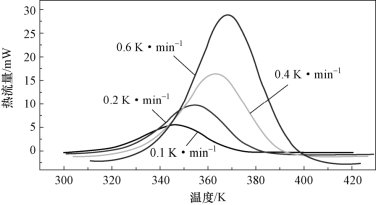
图3-30 BAMO-r-THF/BPS混合体系微量热曲线
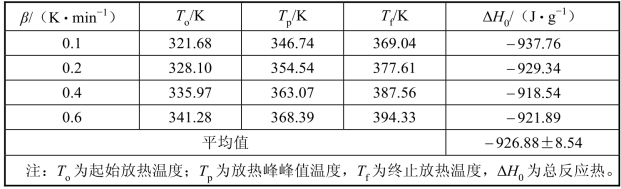
表3-9 BAMO-r-THF/BPS体系固化反应的特征参数
将图3-30量热曲线中的纵坐标对温度求积分,可以得到BAMO-r-THF/BPS黏结剂体系不同升温速率下固化进度与温度的关系,如图3-31所示。由图3-31可知,升温速率越慢,黏结剂体系完全固化的温度越低;相同温度下,升温速率越快,固化进度越低;黏结剂体系完全固化时,升温速率快则所对应的温度高,这是因为升温速率越快,达到相同温度所需时间就越短,BAMO-r-THF分子链上叠氮基与炔基的反应时间也较短,因此固化程度就会降低,黏结剂体系完全固化所需温度就会增加。
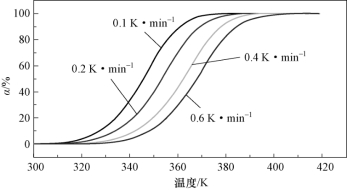
图3-31 BAMO-r-THF/BPS在不同升温速率下固化进度与温度的关系曲线
2.固化反应活化能
根据升温速率β 和固化反应峰温Tp,利用Kissinger法可直接求出表观活化能Eα和指前因子A值;与利用反应机理函数求活化能相比,该法可避免因反应机理函数不准引发的误差。Kissinger方程如式(3-11)所示[43]。
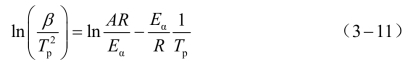
式中,β 为动态升温速率,K·min-1;Tp为放热峰峰值温度,K;A为指前因子,s-1;Eα为表观活化能,kJ·mol-1;R为气体常数,8.314 5 J·mol-1·K-1。
ln![]() 对1/Tp进行拟合所得曲线如图3-32所示。由图3-32可计算得到曲线的斜率和截距,根据Kissinger方程计算获得表观活化能Eα和指前因子A分别为81.94 kJ·mol-1和108.48 s-1,相关系数rk为0.999。
对1/Tp进行拟合所得曲线如图3-32所示。由图3-32可计算得到曲线的斜率和截距,根据Kissinger方程计算获得表观活化能Eα和指前因子A分别为81.94 kJ·mol-1和108.48 s-1,相关系数rk为0.999。
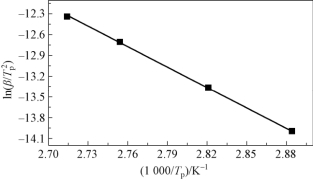
图3-32 ln(β/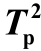 )-1/Tp曲线
)-1/Tp曲线
3.固化反应级数
利用Kissinger法获得的BAMO-r-THF/BPS反应表观活化能,通过Crane法可直接计算该黏结剂体系固化反应的反应级数n,Crane方程如式(3-12)所示[44]:
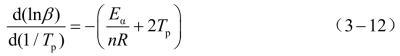
由于Eα/(nR)远大于2Tp,因此可将式(3-12)简化为式(3-13)。

式中,Eα为Kissinger法计算获得的表观活化能,kJ·mol-1;n为反应级数。
lnβ 与1/Tp关系曲线如图3-33所示。通过拟合可得到斜率为-1.06 × 104 K,相关系数rc为0.999 9,由式(3-13)计算获得BAMO-r-THF/BPS黏结剂体系固化反应的反应级数为0.93。BAMO-r-THF/BPS混合体系固化反应级数为非整数,说明该固化反应是一个复杂反应,根据n级反应动力学模型可获得BAMO-r-THF/BPS混合体系固化反应动力学方程式为:
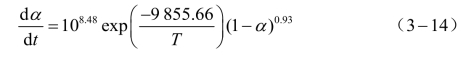
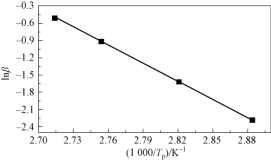
图3-33 lnβ-1/Tp曲线
