新药Ⅱ期临床试验设计
Ⅱ期研究是治疗作用的摸索阶段。其目的是摸索药物对目标适应证的疗效和药物安全性,也为Ⅲ期临床试验的研究设计和给药剂量方案提供依据。此阶段的研究设计可以根据具体的研究目的,一般采用严格的随机双盲对照试验,以平行对照为主。通常应该与标准疗法进行比较,也可以使用安慰剂对照。需注意诊断标准、疗效标准的科学性、权威性和统一性。要根据试验目的选择恰当的终点指标,包括诊断指标、疗效指标、安全性指标。选择指标时,应注意其客观性、可靠性、灵敏度、特异性、相关性和可操作性。参照临床前实验和Ⅰ期临床试验的实际情况制定药物的剂量研究方案。应有符合伦理学要求的中止试验的标准和个别受试对象退出试验的标准。对不良事件、不良反应的观测、判断和及时处理都应做出具体规定。应有严格的观测、记录及数据管理制度。试验结束后,对数据进行统计分析,由有关人员对药物的安全性、有效性、使用剂量等做出初步评价和结论。
设计案例
一项针对2型糖尿病血糖控制不佳的受试者多中心、随机、双盲、安慰剂对照Ⅱ期临床试验,以评价DPP-4I的疗效和安全性。
【目的】评价2型糖尿病患者DPP-4I不同剂量在12周治疗后疗效指标糖化血红蛋白基线变化的趋势。
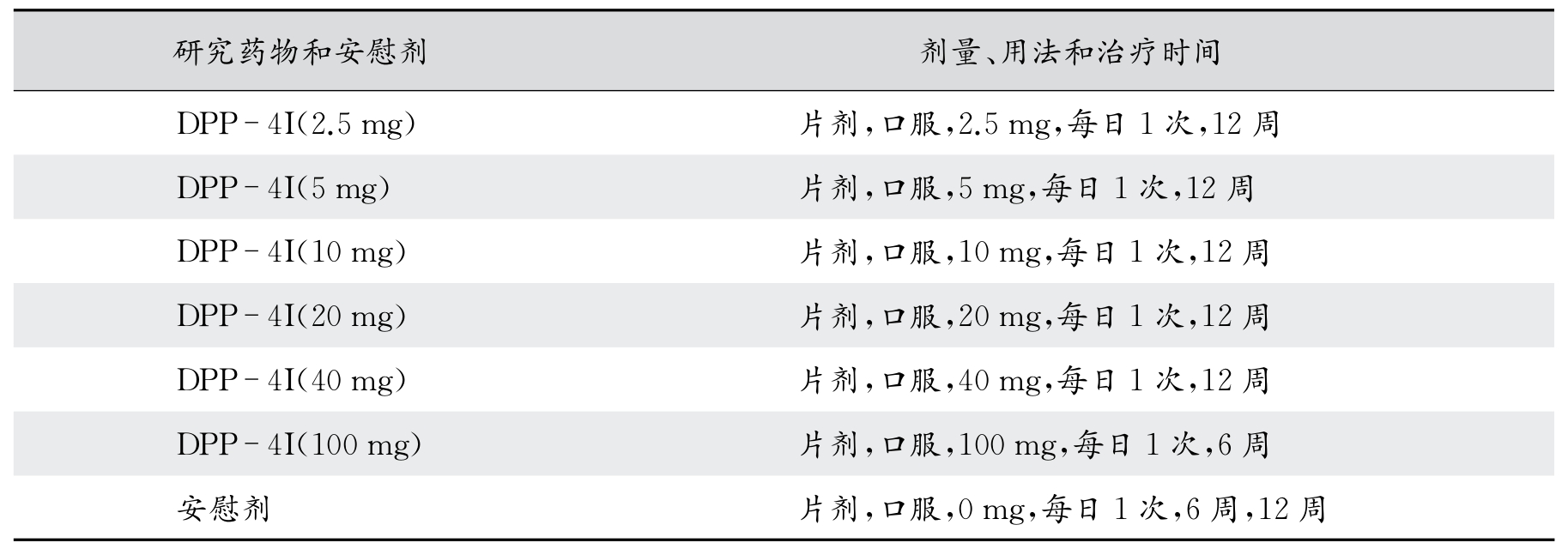
【受试者人数】423人。分组用药情况如表4-9。
表4-9 分组用药情况
【主要终点指标】评估糖化血红蛋白在2.5~40 mg各队列组从基线到用药12周的变化(注:基线的平均值变化,以百分比来评价。分析糖化血红蛋白在2.5~40 mg各队列组与安慰剂从基线到用药12周的变化)。
【次要终点指标】糖化血红蛋白在2.5~40 mg各队列组,100 mg组与安慰剂组从基线到用药6周的变化趋势。
空腹血糖在2.5~40 mg各队列组,100 mg组与安慰剂组从基线到用药6周的变化。
空腹血糖在2.5~40 mg各队列组,100 mg组与安慰剂组从基线到用药12周的变化。
果糖胺在2.5~40 mg各队列组,100 mg组与安慰剂组从基线到用药6周的变化。
果糖胺在2.5~40 mg各队列组,100 mg组与安慰剂组从基线到用药12周的变化。
胰岛素在2.5~40 mg各队列组,100 mg组与安慰剂组从基线到用药6周的变化。(https://www.daowen.com)
胰岛素在2.5~40 mg各队列组,100 mg组与安慰剂组从基线到用药12周的变化。
C肽在2.5~40 mg各队列组,100 mg组与安慰剂组从基线到用药6周的变化。
C肽在2.5~40 mg各队列组,100 mg组与安慰剂组从基线到用药12周的变化。
在2.5~40 mg各队列组,100 mg组与安慰剂组基线和第6周,餐后0~60分钟葡萄糖曲线下面积的变化。
在2.5~40 mg各队列组,100 mg组与安慰剂组基线和第12周,餐后0~60分钟葡萄糖曲线下面积的变化。
在2.5~40 mg各队列组,100 mg组与安慰剂组基线和第6、第12周,餐后15分钟、30分钟、60分钟血糖的变化。
在2.5~40 mg各队列组,100 mg组与安慰剂组基线和第6、第12周,餐后15分钟、30分钟、60分钟胰岛素的变化。
在2.5~40 mg各队列组,100 mg组与安慰剂组基线和第6、第12周,餐后15分钟、30分钟、60分钟C肽的变化。
所有队列组在治疗期12周内AE、SAE以及死亡和退出试验的受试者的百分比(AE必须在12周内采集,在治疗结束后的30日内发生的SAE和退出试验也均必须采集)。
【入选标准】21~70岁。男性或女性。未接受治疗过的2型糖尿病患者。筛选时糖化血红蛋白≥6.8%和≤9.7%。筛查禁食C肽>0.5 ng/ml。血清谷氨酸脱羧酶抗体阴性。体重指数<35 kg/m2。
【排除条件】糖尿病控制不良的症状。糖尿病酮症酸中毒史,高渗性非酮症昏迷,在筛查1年内使用过胰岛素治疗。自确诊以来,口服降糖药物超过6个月。重大心血管病史。
