1.2.1 蒸气压
2025年09月17日
1.2.1 蒸气压
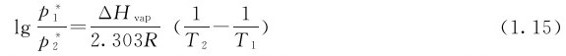
1.液体的蒸气压 将液体置于密闭容器中,它将蒸发,液面上方的空间被液体分子占据。随着上方空间液体分子个数的增加,蒸气密度增加,当蒸气分子与液面撞击时,重新进入液体中,这个过程叫凝聚。当凝聚速度和蒸发速度相等时,上方空间的蒸气密度不再改变,体系达到一种动态平衡。此时蒸气压强不再变化,这时的蒸气压为该温度下的饱和蒸气压,简称蒸气压(vapor pressure),用P*表示
同一种液体的饱和蒸气压,与液体的体积、蒸气体积无关,只与温度有关,所以蒸气压仅与液体的本质和温度有关。克劳修斯-克拉贝龙(Clausius-Clapeyron)在大量实验的基础上,得到饱和蒸气压与蒸发热的关系如下:
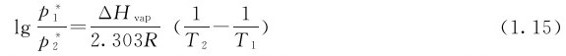
该式称为克劳修斯-克拉贝龙方程式。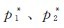 分别是液体在T1、T2时的饱和蒸气压。
分别是液体在T1、T2时的饱和蒸气压。
2.溶液的蒸气压 溶液的蒸气压指一定温度下溶液挥发或蒸发的蒸气在溶液液面以上产生的气体压强。通常的溶液都是以水为溶剂,当水与易挥发性物质(乙醇、丙酮等)形成溶液时,蒸气压会大于水的饱和蒸气压;当水与难挥发物质形成溶液时,蒸气压小于水的饱和蒸气压。
