10.1.4 单质的物理性质和化学性质
10.1.4 单质的物理性质和化学性质
10.1.4.1 物理性质
过渡元素的金属外观多呈银白色或灰白色,有光泽。除钪和钛属轻金属外,其余均属重金属,其中以重铂组元素最重。
过渡元素的原子半径较小而彼此堆积很紧密,同时由于过渡元素的最外层s电子和次外层d电子都可以参加成键,从而增加了金属键的强度,因此过渡金属单质具有高熔点、高沸点、高密度及高硬度等特点。
许多过渡金属及其化合物都有未成对的电子,因此具有顺磁性。
过渡元素的单质有较好的延展性和机械加工性能,彼此间以及与非过渡金属可以形成具有多种特征的合金。过渡金属都是电和热的良导体,它们在工程材料方面有着广泛的应用。
10.1.4.2 化学性质
过渡元素化学活泼性差别明显。第一过渡系元素的单质比第二、第三过渡系元素单质化学性质活泼。Ti、V、Cr、Mn、Fe、Co、Ni、Zn等属于活泼金属,能与稀酸(盐酸或硫酸)作用;而第二、第三过渡系的单质较难发生类似反应,金、铂仅能溶于王水中,铌、钽、钌、铑、锇、铱不溶于王水,主要原因是第二、第三过渡系元素具有较大的电离能和升华焓,有些金属表面易形成氧化膜,使金属钝化,降低了它们的活泼性。
尽管过渡金属的活泼性相差很大,但仍有某些规律可循。过渡金属在水溶液中的活泼性,可根据标准电极电势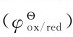 来判断,表10.2为第一过渡系金属的标准电极电势。
来判断,表10.2为第一过渡系金属的标准电极电势。
表10.2 第一过渡系金属的标准电极电势
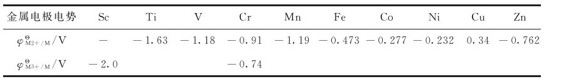
第一过渡系金属,除铜外,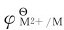 均为负值,其金属单质可从非氧化性酸中置换出氢。同一周期元素从左向右,总的变化趋势是
均为负值,其金属单质可从非氧化性酸中置换出氢。同一周期元素从左向右,总的变化趋势是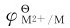 值逐渐变大,其活泼性逐渐减弱。表10.2中
值逐渐变大,其活泼性逐渐减弱。表10.2中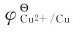 的代数值最大,原因是其第二电离能最大,要破坏3d10全充满稳定结构使之变为3d9需要较高的能量。尽管Cu2+的离子半径较小,水合能较大,但不能完全抵消第二电离能的影响,所以总的能量变化增大。
的代数值最大,原因是其第二电离能最大,要破坏3d10全充满稳定结构使之变为3d9需要较高的能量。尽管Cu2+的离子半径较小,水合能较大,但不能完全抵消第二电离能的影响,所以总的能量变化增大。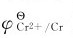 的增大也可以同样解释,因为
的增大也可以同样解释,因为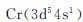 的第二电离能也较大。而Zn(3d104s2)的2个4s电子很容易失去,使
的第二电离能也较大。而Zn(3d104s2)的2个4s电子很容易失去,使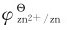 又有较大幅度的降低。
又有较大幅度的降低。
第二、三过渡系元素的金属单质非常稳定,一般不和强酸反应,但可以和浓碱或熔碱发生反应。
