3.3.2 多重平衡规则
2025年09月17日
3.3.2 多重平衡规则
通常见到的化学平衡系统,往往同时包含多个相互有关的平衡,系统内有些物质同时参加了多个反应,达到了多个平衡,此种平衡系统称为多重平衡系统。
例如在同一个容器中发生下面的反应:
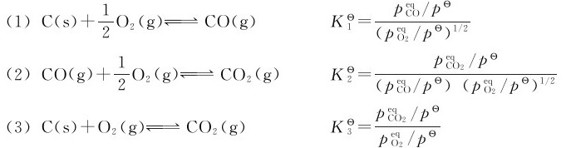
在这个平衡系统中,O2参与了三个反应,体系达到平衡以后,同一反应系统中的各个化学反应都同时达到平衡,O2的平衡浓度或分压必定同时满足每一个化学反应的标准平衡常数表达式。所以在三个标准平衡常数公式中,O2的平衡分压相等。同理,CO、CO2的平衡分压也相等。此时,反应(3)=反应(1)+反应(2),三个平衡常数满足下列关系:
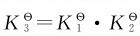
由此可以推出,反应(2)=反应(1)-反应(3)时,三个平衡常数满足下列关系:
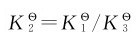
实际上,在上述反应中,只有两个反应是独立的。因此无论选择其中哪两个,第三个反应都可以根据它们的组合而得到,而且第三个反应的平衡常数与两个独立反应的平衡常数存在一定的关系,这就是多重平衡规则。
掌握和利用多重平衡规则,不论对实际生产还是对平衡问题的理论研究,都具有重要的意义。尤其对那些难以直接测定或不易从文献中查得的平衡常数的反应,可根据此规则间接计算它们的平衡常数。
