微生物限度检查法
对于口服药和外用药,不必要求达到无菌状态,但要保证药物的卫生质量,这就要求进行微生物限度检查。微生物限度检查法系指检查非规定灭菌制剂及其原料、辅料受微生物污染程度的方法。微生物限度检查法包括微生物计数法和控制菌检查法。
(一)微生物计数法
微生物计数法系用于能在有氧条件下生长的嗜温细菌和真菌的计数,包括平皿法、薄膜过滤法和最可能数法(MPN法)。供试品检查时,应根据供试品理化特性和微生物限度标准等因素选择计数方法,检测的样品量应能保证获得的实验结果能够判断供试品是否符合规定,选择方法的适用性必须经确认。除另有规定外,本法不适用于活菌制剂的检查。
微生物计数试验环境应符合微生物限度检查的要求。检验全过程必须严格遵守无菌操作,防止再污染,防止污染的措施不得影响供试品中微生物的检出。单向流空气区域、工作台面及环境应定期进行监测。
1.计数培养基适用性检查和供试品计数方法适用性试验
(1)计数培养基适用性检查:微生物计数法所用的培养基很多,如胰酪大豆胨液体培养基、胰酪大豆胨琼脂培养基、沙氏葡萄糖琼脂培养基、沙氏葡萄糖液体培养基等。供试品微生物计数中所使用的培养基应进行适用性检查。具体方法:
1)菌液制备:取金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌的新鲜培养物,用pH=7.0无菌氯化钠-蛋白胨缓冲液或0.9%无菌氯化钠溶液制成适宜浓度的菌悬液;取黑曲霉的新鲜培养物加入3~5 mL含0.05%(mL/mL)聚山梨酯80的pH=7.0无菌氯化钠-蛋白胨缓冲液或0.9%无菌氯化钠溶液,将孢子洗脱。然后,采用适宜的方法吸出孢子悬液至无菌试管内,用含0.05%(mL/mL)聚山梨酯80的pH=7.0无菌氯化钠-蛋白胨缓冲液或0.9%无菌氯化钠溶液制成适宜浓度的黑曲霉孢子悬液。菌液制备后若在室温下放置,应在2 h内使用;若保存在2~8℃,可在24 h内使用。黑曲霉孢子悬液可保存在2~8℃,在验证过的储存期内使用。
2)阴性对照:为确认试验条件是否符合要求,应进行阴性对照试验,阴性对照试验应无菌生长。如阴性对照有菌生长,应进行偏差调查。
3)培养基适用性检查:按照《中国药典》规定接种不大于100 cfu的菌液至胰酪大豆胨液体培养基管或胰酪大豆胨琼脂培养基管或沙氏葡萄糖琼脂培养基平板,按规定条件培养。每一试验菌株平行制备2管或2个平皿,同时用相应的对照培养基替代被检培养基进行对照试验。被检固体培养基上的菌落平均数与对照培养基上的菌落平均数的比值应在0.5~2范围内,且菌落形态大小应与对照培养基上的菌落一致;被检液体培养基管与对照培养基管比较,试验菌应生长良好。
(2)计数方法适用性试验:为确认所采用的方法适合于供试品的微生物计数,对供试品的微生物计数法应进行方法适用性试验。具体方法:
1)供试液的制备:根据供试品的理化性质与生物学特征,按照《中国药典》的要求,采用适宜的方法制备供试液。
2)微生物回收试验用供试液的制备:对供试液进行接种和稀释,制备试验组、供试品对照组和菌液对照组微生物回收试验用供试液。
A.试验组:取制备好的供试液,加入试验菌液,混匀,使每1 mL供试液或每张滤膜所滤过的供试液中含菌量不大于100 cfu。
B.供试品对照组:取制备好的供试液,以稀释液(pH=7.0无菌氯化钠-蛋白胨缓冲液、pH=6.8无菌磷酸盐缓冲液、pH=7.2无菌磷酸盐缓冲液、pH=7.6无菌磷酸盐缓冲液或0.9%无菌氯化钠溶液)代替菌液,操作同试验组。
C.菌液对照组:取不含中和剂及灭活剂的相应稀释液替代供试液,按试验组操作加入试验菌液并进行微生物回收试验。
D.制备微生物回收试验用供试液时,所加供试液的体积应不超过供试液体积的1%。为确认供试品中的微生物能被充分检出,首先应选择最低稀释级的供试液进行计数方法适用性试验。若因供试品抗菌活性或溶解性较差的原因导致无法选择最低稀释级的供试液进行方法适用性试验时,应采用适宜的方法对供试液进行进一步的处理。
3)供试品中微生物的回收:计数方法适用性试验所用的各试验菌,采用平皿法,或薄膜过滤法,或MPN法逐一进行微生物回收试验。试验时若试验组菌落数减去供试品对照组菌落数的值小于菌液对照组菌液数值的50%,则需通过增加稀释液或培养基的体积、加入适宜的中和剂或灭活剂,并采用薄膜过滤法,或联合使用这三种方法消除供试品的抑菌活性后再依法进行试验。
A.平皿法:包括倾注法和涂布法。试验时,每株试验菌每种培养基至少制备2个平皿,以算术平均值作为计数结果。①倾注法是取按照上述“供试液的制备”“接种和稀释”和“抗菌活性的去除或灭活”制备的供试液1 mL,置直径90 mm的无菌平皿中,注入15~20 mL温度不超过45℃熔化的胰酪大豆胨琼脂或沙氏葡萄糖琼脂培养基,混匀,凝固,倒置培养。按规定条件培养、计数。同法测定供试品对照组及菌液对照组菌数。计算各试验组的平均菌落数。②涂布法是取15~20 mL温度不超过45℃的胰酪大豆胨琼脂培养基或沙氏葡萄糖琼脂培养基,注入直径90 mm的无菌平皿,凝固,制成平板,采用适宜的方法使培养基表面干燥。每一平板表面接种上述照“供试液的制备”“接种和稀释”和“抗菌活性的去除或灭活”制备的供试液不少于0.1 mL。按《中国药典》规定的条件培养、计数。同法测定供试品对照组及菌液对照组菌数。计算各试验组的平均菌落数。
B.薄膜过滤法:薄膜过滤法所采用的滤膜孔径应不大于0.45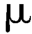 m,直径一般为50 mm。取按照上述“供试液的制备”“接种和稀释”和“抗菌活性的去除或灭活”制备的供试液适量(一般取相当于1 g,1 mL或10 cm2的供试品,若供试品中所含的菌数较多时,供试液可酌情减量),加至适量的稀释液中,混匀,过滤。用适量的冲洗液冲洗滤膜。若测定需氧菌总数,转移滤膜菌面朝上贴于胰酪大豆胨琼脂培养基平板上;若测定霉菌和酵母总数,转移滤膜菌面朝上贴于沙氏葡萄糖琼脂培养基平板上按《中国药典》规定条件培养、计数。每株试验菌每种培养基至少制备一张滤膜。同法测定供试品对照组及菌液对照组菌数。
m,直径一般为50 mm。取按照上述“供试液的制备”“接种和稀释”和“抗菌活性的去除或灭活”制备的供试液适量(一般取相当于1 g,1 mL或10 cm2的供试品,若供试品中所含的菌数较多时,供试液可酌情减量),加至适量的稀释液中,混匀,过滤。用适量的冲洗液冲洗滤膜。若测定需氧菌总数,转移滤膜菌面朝上贴于胰酪大豆胨琼脂培养基平板上;若测定霉菌和酵母总数,转移滤膜菌面朝上贴于沙氏葡萄糖琼脂培养基平板上按《中国药典》规定条件培养、计数。每株试验菌每种培养基至少制备一张滤膜。同法测定供试品对照组及菌液对照组菌数。
C.MPN法:该法的精密度和准确度较差,仅在供试品需氧菌总数没有适宜计数方法的情况下使用,不适用于霉菌的计数。具体方法是取照上述“供试液的制备”“接种和稀释”和“抗菌活性的去除或灭活”制备的供试液至少3个连续稀释级,每一稀释级取3份1 mL分别接种至3管装有9~10 mL胰酪大豆胨液体培养基中,同法测定菌液对照组菌数。接种管置30~35℃培养3 d,逐日观察各管微生物生长情况。如果由于供试品的原因使得结果难以判断,可将该管培养物转种至胰酪大豆胨液体培养基或胰酪大豆胨琼脂培养基,在相同条件下培养1~2 d,观察是否有微生物生长。根据微生物生长的管数从《中国药典》四部通则非无菌产品微生物限度检查:微生物计数法“微生物最可能数检索表”(详见《中国药典》四部)中查出被测供试品每1 g或1 mL中需氧菌总数的最可能数。
4)结果判断:计数方法适用性试验中采用平皿法或薄膜过滤法时,试验组菌落数减去供试品对照组菌落数的值与菌液对照组菌落数的比值应在0.5~2范围内;采用MPN法时,试验组菌数应在菌液对照组菌数的95%置信限内。
2.供试品检查
(1)检验量:检验量即一次试验所用的供试品量(g、mL或cm2)。一般应随机抽取不少于2个最小包装的供试品,混合,取规定量供试品进行检验。除另有规定外,一般供试品的检验量为10 g或10 mL;膜剂为100 cm2;贵重药品、微量包装药品的检验量可以酌减。检验时,应从2个以上最小包装单位中抽取供试品,大蜜丸还不得少于4丸,膜剂还不得少于4片。
(2)供试品的检查:按计数方法适用性试验确认的计数方法进行检查。同时还需要进行阴性对照试验,即以稀释液代替供试液同法进行试验。阴性对照试验应无菌生长,若有菌生长,应进行偏差调查。胰酪大豆胨琼脂培养基或胰酪大豆胨液体培养基用于测定需氧菌总数;沙氏葡萄糖琼脂培养基用于测定霉菌和酵母菌总数。
1)平皿法:除另有规定外,每稀释级每种培养基至少制备2个平板。
A.培养和计数:除另有规定外,胰酪大豆胨琼脂培养基平板在30~35℃培养3~5 d,沙氏葡萄糖琼脂培养基平板在20~25℃培养5~7 d,观察菌落生长情况,点计平板上生长的所有菌落数,计数并报告。菌落蔓延生长成片的平板不宜计数。点计菌落数后,计算各稀释级供试液的平均菌落数,按菌数报告规则报告菌数。若同稀释级两个平板的菌落数平均值不小于15 cfu,则两个平板的菌落数不能相差1倍或以上。(https://www.daowen.com)
B.菌数报告规则:需氧菌总数测定宜选取平均菌落数小于300 cfu的稀释级、霉菌和酵母菌总数测定宜选取平均菌落数小于100 cfu的稀释级,作为菌数报告的依据。取最高的平均菌落数,计算1 g、1 mL或10 cm2供试品中所含的微生物数,取两位有效数字报告。如各稀释级的平板均无菌落生长,或仅最低稀释级的平板有菌落生长,但平均菌落数小于1时,以<1乘以最低稀释倍数的值报告菌数。
2)薄膜过滤法:除另有规定外,按计数方法适用性试验确认的方法进行供试液制备。取相当于1 g、1 mL或10 cm2供试品的供试液,若供试品所含的菌数较多时,可取适宜稀释级的供试液,按照适用性试验确认的方法加至适量稀释液中,立即过滤,冲洗,冲洗后取出滤膜,菌面朝上贴于胰酪大豆胨琼脂培养基或沙氏葡萄糖琼脂培养基上培养。
A.培养和计数:培养条件和计数方法同平皿法,每张滤膜上的菌落数应不超过100 cfu。
B.菌数报告规则:以相当于1 g、1 mL或10 cm2供试品的菌落数报告菌数。若滤膜上无菌落生长,以<1报告菌数(每张滤膜过滤1 g、1 mL或10 cm2供试品),或<1乘以最低稀释倍数的值报告菌数。
3)MPN法:取规定量供试品,按照适用性试验确认的方法进行供试液制备和供试品接种,所有试验管在30~35℃培养3~5 d,如果需要确认是否有微生物生长,按照适用性试验确定的方法进行。记录每一稀释级微生物生长的管数,从“微生物最可能数检索表”查每1 g或1 mL供试品中需氧菌总数的最可能数。
3.结果判断 需氧菌总数是指胰酪大豆胨琼脂培养基上生长的总菌落数(包括真菌菌落数);霉菌和酵母菌总数是指沙氏葡萄糖琼脂培养基上生长的总菌落数(包括细菌菌落数);若采用MPN法,测定结果为需氧菌总数。若供试品的需氧菌总数、霉菌和酵母菌总数的检查结果均符合该品种项下的规定,判供试品符合规定;若其中任何一项不符合该品种项下的规定,判供试品不符合规定。
(二)控制菌检查法
控制菌检查法系用于在规定的试验条件下,检查供试品中是否存在特定的微生物,主要是耐胆盐革兰阴性菌、大肠埃希菌、沙门菌、铜绿假单胞菌、金黄色葡萄球菌、梭菌、白色念珠菌的检查。
1.菌液制备 将金黄色葡萄球菌、铜绿假单胞菌、大肠埃希菌、沙门菌分别接种于胰酪大豆胨液体培养基中或在胰酪大豆胨琼脂培养基上,30~35℃培养18~24 h;将白色念珠菌接种于沙氏葡萄糖琼脂培养基上或沙氏葡萄糖液体培养基中,20~25℃培养2~3 d,将生孢梭菌接种于梭菌增菌培养基中置厌氧条件下30~35℃培养24~48 h或接种于硫乙醇酸盐流体培养基中30~35℃培养18~24 h。上述培养物用pH=7.0无菌氯化钠-蛋白胨缓冲液或0.9%无菌氯化钠溶液制成适宜浓度的菌悬液。为确认试验条件是否符合要求,还应进行阴性对照试验,阴性对照试验应无菌生长,如有菌生长,应进行偏差调查。
2.培养基适用性检查 控制菌检查用的成品培养基、由脱水培养基或按处方配制的培养基均应进行培养基的适用性检查。检查项目包括促生长能力、抑制能力及指示特性的检查。不同培养基的检查项目及所用试验菌株不同,《中国药典》对其均有规定。
(1)促生长能力的检查:固体培养基和液体培养基促生长能力的检查方法不同。①液体培养基促生长能力检查方法是:分别接种不大于100 cfu的试验菌于被检培养基和对照培养基中,在相应控制菌检查规定的培养温度及不大于规定的最短培养时间下培养,与对照培养基管比较,被检培养基管试验菌应生长良好。②固体培养基促生长能力检查的方法是:用涂布法分别接种不大于100 cfu的试验菌于被检培养基和对照培养基平板上,在相应控制菌检查规定的培养温度及不大于规定的最短培养时间下培养,被检培养基与对照培养基上生长的菌落大小、形态特征应一致。
(2)培养基抑制能力检查:接种不少于100 cfu的试验菌于被检培养基和对照培养基中,在相应控制菌检查规定的培养温度及不小于规定的最长培养时间下培养,试验菌应不得生长。
(3)培养基指示特性检查:用涂布法分别接种不大于100 cfu的试验菌于被检培养基和对照培养基平板上,在相应控制菌检查规定的培养温度及不大于规定的最短培养时间下培养,被检培养基上试验菌生长的菌落大小、形态特征、指示剂反应情况等应与对照培养基一致。
3.控制菌检查方法适用性试验 按照《中国药典》规定配制供试品溶液和选定试验菌株,按控制菌检查法取规定量的供试液及不大于100 cfu的试验菌接入规定的培养基中,依相应的控制菌检查法,在规定的温度和最短时间下培养,应能检出所加试验菌相应的反应特征。若能检出试验菌,则方法可用;若未检出试验菌,应消除供试品的抑菌活性后再重新进行方法适用性试验。
4.阳性对照试验和阴性对照试验 方法验证后,进行供试品控制菌检查时,还需进行试验菌的阳性对照试验和稀释液的阴性对照试验,阳性对照应检出相应的控制菌,阴性对照应无菌生长。
5.控制菌的检查 不同的控制菌检查方法各不相同,本书只介绍大肠埃希菌和沙门菌。
(1)大肠埃希菌:大肠埃希菌即大肠杆菌,属肠杆菌科埃希菌属,是人和温血动物肠道内的栖居菌,可随粪便排出体外,是粪便污染指示菌。致病性大肠埃希菌,可引起婴幼儿、成人暴发性腹泻、化脓或败血症,口服药品必须检查大肠埃希菌。
检查方法:取相当于1 g或1 mL供试品的供试液,接种至适宜体积的胰酪大豆胨液体培养基中,混匀,30~35℃培养18~24 h。取培养物1 mL接种至100 mL麦康凯液体培养基中,42~44℃培养24~48 h。取麦康凯液体培养物划线接种于麦康凯琼脂培养基平板上,30~35℃培养18~72 h。若麦康凯琼脂培养基平板上有菌落生长,应进行分离、纯化及适宜的鉴定试验,确证是否为大肠埃希菌;若麦康凯琼脂培养基平板上没有菌落生长,或虽有菌落生长但鉴定结果为阴性,判供试品未检出大肠埃希菌。
(2)沙门菌:沙门菌属肠杆菌科沙门菌属,是人畜共患的肠道病原菌,可引起伤寒、肠炎、肠热病和食物中毒。
检查方法:取10 g或10 mL供试品直接或处理后接种至适宜体积的胰酪大豆胨液体培养基中,混匀,30~35℃培养18~24 h。取培养物0.1 mL接种至10 mLRV沙门菌增菌液体培养基中,30~35℃培养18~24 h。取少量RV沙门菌增菌液体培养物划线接种于木糖赖氨酸脱氧胆酸盐琼脂培养基平板上,30~35℃培养18~48 h。沙门菌在木糖赖氨酸脱氧胆酸盐琼脂培养基平板上生长良好,菌落为淡红色或无色、透明或半透明、中心有或无黑色。用接种针挑选疑似菌落于三糖铁琼脂培养基高层斜面上进行斜面和高层穿刺接种,培养18~24 h,或采用其他适宜方法进一步鉴定。若木糖赖氨酸脱氧胆酸盐琼脂培养基平板上有疑似菌落生长,且三糖铁琼脂培养基的斜面为红色、底层为黄色,或斜面黄色、底层黄色或黑色,应进一步进行鉴定试验,确证是否为沙门菌。如果平板上没有菌落生长,或虽有菌落生长但鉴定结果为阴性,或三糖铁琼脂培养基的斜面未见红色、底层未见黄色;或斜面黄色、底层未见黄色或黑色,判供试品未检出沙门菌。
(三)注意事项
(1)供试品检出控制菌或其他致病菌时,按一次检出结果为准,不再复试。
(2)药品在检验前,应保持原包装状态,不得开启,以免污染。同时药物需放置于阴凉干燥处,防止微生物繁殖,以免影响检验结果。凡原包装已被开启者,应另行取样。
(3)供试品检验全过程必须符合无菌技术要求。使用灭菌用具时,不能接触可能污染的任何器物,灭菌吸管不得吹吸。
(4)培养基的分装量不得超过容器的2/3,以免灭菌时溢出。包装时,塞子必须塞紧,塞入2/3,以免松动脱落或造成染菌。
