二、脂溶性维生素
脂溶性维生素是指在油脂中的溶解度较大,在水中几乎不溶的维生素,包括维生素A、维生素D、维生素E、维生素K等,下面重点介绍维生素A和维生素E。
(一)维生素A的分析
维生素A包括维生素A1(视黄醇)、维生素A2(去氢维生素A)、和维生素A3(去水维生素A)等,其中维生素A1的活性最高,因此通常所说的维生素A指维生素A1,它是一种不饱和的脂肪醇,其天然产品主要源于鱼肝油,目前药用维生素A主要采用人工合成的方法制取。《中国药典》收载的有维生素A、维生素A软胶囊、维生素AD软胶囊及维生素AD滴剂。其中的维生素A是人工合成的维生素A1醋酸酯与精制植物油制成的油溶液。
1.药物的结构与性质
(1)结构:维生素A的结构为具有一个共轭多烯醇(酯)侧链的环己烯,有多种立体异构体。基本结构为
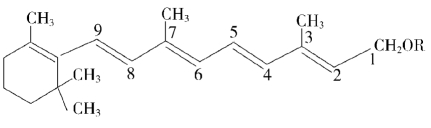
根据维生素A取代基R的不同,可分为维生素A醇和维生素A酯。取代基不同,其外观性状及熔点不同(表6-12)。
表6-12 维生素A的分类(纯品)
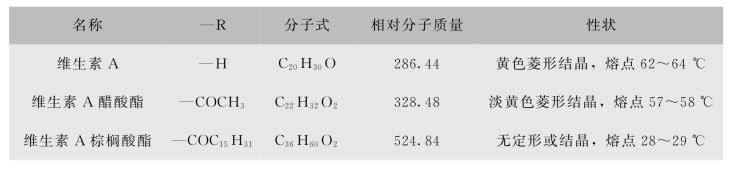
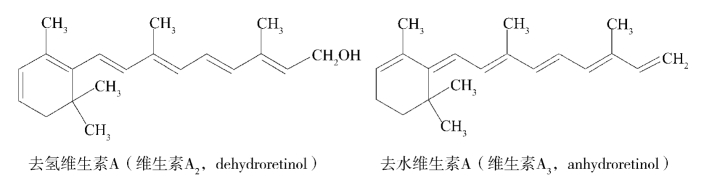
维生素A的异构体与维生素A具有相似的化学性质,但其光谱特性及生物效价不同。去氢维生素A、脱水维生素A及维生素A顺反异构体效价均低于维生素A1,鲸醇(维生素A醇的二聚体)无生物活性,但这些物质在310~340 nm波长处均有紫外吸收,并能与显色试剂产生相近颜色。所以测定维生素A含量时应考虑这些干扰因素。
(2)性质:
1)溶解性:维生素A与三氯甲烷、乙醚、环己烷或石油醚能任意比例混溶,易溶于异丙醇、脂肪和植物油,在乙醇中微溶,在水中不溶。
2)易氧化变质:维生素A分子结构中有共轭多烯醇侧链,性质不稳定,易被空气中的氧或氧化剂氧化,遇光易变质,尤其在受热或金属离子存在时,更易氧化变质。其氧化产物为环氧化合物、维生素A醛或维生素A酸,均无生物活性。
3)脱水反应:维生素A对酸不稳定,在一定条件下(如无水氯化氢乙醇液中)可发生脱水反应,生成脱水维生素A。
4)与三氯化锑呈色:维生素A的三氯甲烷溶液与三氯化锑作用显色,可作为维生素A定性、定量分析的依据。
5)具紫外吸收:维生素A分子中具有共轭多烯醇的侧链结构,且与环己烯环共轭,在325~328 nm波长处有最大吸收,此特性可用于鉴别和含量测定。应注意其最大吸收峰的位置随溶剂的不同而异。表6-13为维生素A在不同溶剂中的紫外吸收数据。
表6-13 维生素A在不同溶剂中的紫外吸收数据
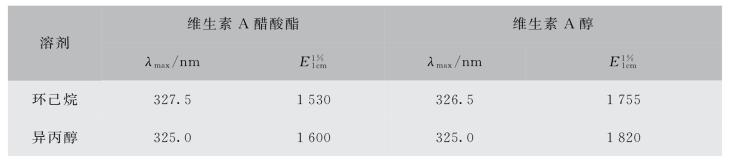
2.维生素A的分析
(1)性状:本品为淡黄色油溶液或结晶与油的混合物(加热至60℃,为澄清溶液);无臭;在空气中易氧化,遇光易变质。
(2)鉴别:
1)三氯化锑反应:《中国药典》收载的维生素A及其软胶囊、维生素AD软胶囊及维生素AD滴剂均采用三氯化锑的显色反应进行鉴别。《美国药典》和《日本药局方》也采用该法鉴别本品。
A.方法:取维生素A1滴,加三氯甲烷10 mL,振摇使其溶解;取出2滴,加三氯甲烷2 mL与25%三氯化锑的三氯甲烷溶液0.5 mL,即显蓝色,渐变为紫红色。
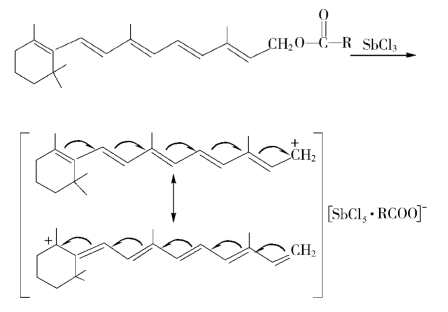
B.原理:维生素A在三氯甲烷溶液中,与饱和无水三氯化锑试剂中的氯化高锑作用形成正碳离子,而产生不稳定的蓝色,渐变成紫红色。反应式为
C.注释:①由于水可使三氯化锑水解成氯化氧锑(Sb OCl),乙醇可使碳正离子的正电荷消失,所以该反应须在无水无醇条件下进行。②在本反应中,实际起作用的可能是三氯化锑试剂中的氯化高锑。③本反应专属性差,显色极不稳定。
2)紫外分光光度法:《英国药典》曾用该法鉴别浓缩维生素A酯类药物(天然品)。
A.方法:取约相当于10 IU的维生素A供试品,加无水乙醇-盐酸(100∶1)溶液溶解,立即用紫外-可见分光光度计在300~400 nm的波长范围内进行扫描,应仅在326 nm的波长处有单一的吸收峰。将此溶液置水浴上加热30 s,迅速使冷却,照上法进行扫描,则应在348 nm、367 nm和389 nm的波长处有3个尖锐的吸收峰,且在332 nm的波长处有肩峰或拐点。如图6-2所示。
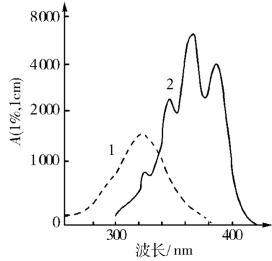
图6-2 维生素A和脱水维生素A的紫外吸收光谱图
1.维生素 2.脱水维生素A
B.原理:维生素A分子中含有5个共轭双键,其无水乙醇溶液在326 nm的波长处有最大吸收峰。当在盐酸催化下加热,则发生脱水反应而生成去水维生素A。后者比维生素A多一个共轭双键,故其最大吸收峰向长波长位移(红移,即向长波方向移动),同时在332 nm附近有曲折,在348 nm、367 nm、389 nm附近有吸收峰。
3)薄层色谱法:BP和USP曾用薄层色谱法对维生素A进行鉴别,但方法不完全相同。
A.BP鉴别法:以硅胶G为吸附剂,环己烷-乙醚(80∶20)为流动相。分别取供试品与对照品(不同维生素A酯类)的环己烷溶液(5 IU/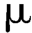 L)各2
L)各2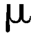 L,点于薄层板上,不必挥散溶剂,立即展开。取出薄层板后,置空气中挥干,喷以三氯化锑溶液,比较供试品溶液和对照品溶液所显蓝色斑点位置,即可鉴别。
L,点于薄层板上,不必挥散溶剂,立即展开。取出薄层板后,置空气中挥干,喷以三氯化锑溶液,比较供试品溶液和对照品溶液所显蓝色斑点位置,即可鉴别。
B.USP鉴别法:以硅胶为吸附剂,环己烷-乙醚(80∶20)为流动相,以维生素A的三氯甲烷溶液(约1 500 IU/mL)点样0.01 mL,展开10 cm,空气中挥干,以磷钼酸为显色剂显色。维生素A醇及其醋酸酯、棕榈酸酯均显蓝绿色,其Rf值分别为0.1、0.45和0.7。此为《美国药典》的鉴别方法。
注释:BP鉴别法可用作鉴别浓缩合成品维生素A的各种酯类(油剂);由于维生素A与三氯化锑所显蓝色不稳定,故应立即比色。
(3)检查:《中国药典》规定对维生素A进行酸值和过氧化值检查。
1)酸值:维生素A在制备过程中酯化不完全或贮藏过程中水解,均可生成醋酸。酸度大,不利于维生素A的稳定,因此应控制酸度。
A.检查方法:取乙醇与乙醚各15 mL,置锥形瓶中,加酚酞指示液5滴,滴加氢氧化钠滴定液(0.1 mol/L)至微显粉红色,再加维生素A2.0 g,振摇使溶解,用氢氧化钠滴定液(0.1 mol/L)滴定至粉红色30 s不褪,酸值不得过2.0(通则0713)。
B.原理:本法检查的是游离醋酸,可被氢氧化钠中和。
C.注释:①酸值系指中和1 g的脂肪、脂肪油或其他类似物质中含有的游离酸所需氢氧化钾的质量(mg),测定时可用氢氧化钠滴定液(0.1 mol/L)进行滴定。②酸值计算公式,如所用氢氧化钠滴定液(0.1 mo L/L)的浓度不恰为0.100 0 mol/L时,应乘以滴定液浓度校正因子F值。③酸值在10以下时,用10 mL的半微量的滴定管;测定酸值小于10的油脂时,溶解供试品所用的醇醚混合液中的乙醇宜改用无水乙醇,防止供试品溶液可能出现的析出问题。
2)过氧化值:维生素A结构中的共轭双键,易被氧化成过氧化物,因此应控制此类杂质。
A.检查方法:取本品1.0 g,加冰醋酸-三氯甲烷(6∶4)30 mL,振摇使溶解,加碘化钾的饱和溶液1 mL,振摇1 min,加水l00 mL与淀粉指示液1 mL,用硫代硫酸钠滴定液(0.01 mol/L)滴定至紫蓝色消失,并将滴定的结果用空白试验校正。消耗硫代硫酸钠滴定液(0.01 mol/L)不得过1.5 mL。
B.注释:利用维生素A中的过氧化物可将碘化钾氧化为碘,碘可以与硫代硫酸钠定量反应,通过硫代硫酸钠滴定液消耗的量,计算出本品的过氧化值。过氧化值指每1 000 g供试品中含有的其氧化能力与一定量的氧相当的过氧化物量。
(4)含量测定:维生素A及其制剂含量测定的方法,最初采用生物学方法测定其生物活性。因该法操作烦琐、费时,准确度与重现性较差,后来采用三氯化锑比色法。但由于三氯化锑反应专属性差,呈色极不稳定,测定结果受水分、温度影响较大,但由于本法较简便、快速,现仍用于食品和饲料中维生素A的含量测定。目前,各国药典均采用紫外分光光度法测维生素A及其制剂的含量。《中国药典》规定维生素A醋酸酯原料及制剂中维生素A的含量用“维生素A测定法”中的高效液相色谱法测定,维生素A及其软胶囊采用“维生素A测定法”中的紫外-可见分光光度法。本法能快速、准确地测定结果,并能较正确地反映出维生素A的生物效价。
下面主要介绍《中国药典》收载的紫外分光光度法,并简要介绍三氯化锑比色法。
1)紫外-可见分光光度法(三点校正法):测定原理:利用维生素A在325~328 nm波长范围内有最大吸收峰进行含量测定,由于维生素A制剂中含有稀释用油,维生素A原料中混有其他杂质,这些杂质在325~328 nm波长处有吸收,对维生素A的测定有干扰。《中国药典》用三点校正法消除干扰物质吸收所引入的误差,以便提高测定结果的准确性。
三点校正法又称三波长校正法,其校正原理主要基于以下两点:①物质对光吸收呈加和性,即在供试品的吸收曲线上,各波长的吸光度是维生素A与干扰杂质吸光度的代数和,其吸收曲线也是二者吸收的叠加。②干扰物质的吸收在310~340 nm波长范围内呈线性,且随波长的增大而吸光度变小。
三波长的选择:分别选在维生素A的最大吸收波长处(λ1),及该波长的两侧各一点(λ2、λ3)。《中国药典》规定维生素A醋酸酯的三波长分别是316 nm、328 nm和340 nm(符合![]() Δλ=12 nm,等波长差法,又叫直接测定法)。维生素A醇的三波长分别是310 nm、325 nm、334 nm(符合Aλ2=Aλ3=6/7Aλ1,等吸收比法,又叫皂化法)。其做法是在3个波长处测得吸光度后,在规定的条件下以校正公式进行校正、判断,然后再进行计算,就可以得到维生素A的真实含量。
Δλ=12 nm,等波长差法,又叫直接测定法)。维生素A醇的三波长分别是310 nm、325 nm、334 nm(符合Aλ2=Aλ3=6/7Aλ1,等吸收比法,又叫皂化法)。其做法是在3个波长处测得吸光度后,在规定的条件下以校正公式进行校正、判断,然后再进行计算,就可以得到维生素A的真实含量。
维生素A的含量以国际单位表示,每国际单位相当于全反式维生素A醋酸酯0.344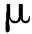 g或全反式维生素A醇0.300
g或全反式维生素A醇0.300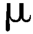 g。维生素A的性质不稳定,含量测定应在半暗室中尽快进行,注意避光。
g。维生素A的性质不稳定,含量测定应在半暗室中尽快进行,注意避光。
合成维生素A和天然鱼肝油中的维生素A主要是维生素A醋酸酯,如果供试品的纯度较高,干扰测定的杂质较少,且符合第一法测定的条件时,可直接用溶剂溶解供试品后进行测定;如果杂质较多或者供试品为维生素A醇时应采用第二法,即经皂化提取后再测定。
A.测定方法一(直接测定酯式维生素A):取供试品适量,精密称定,加环己烷溶解并定量稀释制成每1 mL中含9~15单位的溶液,照紫外-可见分光光度法测定其吸收峰的波长(应为328 nm),并分别在300 nm、316 nm、328 nm、340 nm、360 nm5个波长处分别测其吸光度,计算各吸光度与波长328 nm处吸光度的比值(Ai/A328),并与表6-14规定的理论值比较。
表6-14 维生素A各波长处吸光度的比值(Ai/A328)
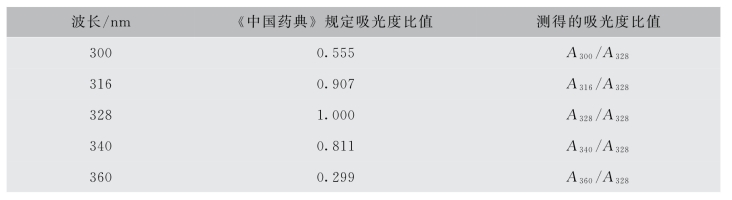
根据以下方法判断计算含量时所选用的A值:
如果吸收峰波长在326~329 nm之间,且所测得的各波长吸光度比值不超过表6-14中规定的±0.02,计算含量时用未校正吸光度(A328);
如果最大吸收波长在326~329 nm之间,但所测得各波长的吸光度比值有一个或几个超过表6-14中规定值的±0.02,应按公式![]() 求出校正后的吸光度,然后再计算含量。未校正吸光度(A328)和校正吸光度(A328校正)的应用,应按下法选择:
求出校正后的吸光度,然后再计算含量。未校正吸光度(A328)和校正吸光度(A328校正)的应用,应按下法选择:
a.328 nm处的校正吸光度与未校正吸光度相差不超过±3.0%(计算方法: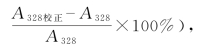 则仍用未校正吸光度(A328)计算含量。
则仍用未校正吸光度(A328)计算含量。
b.如果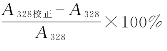 在-15%~-3%之间,应以校正吸光度(A328校正)计算含量。
在-15%~-3%之间,应以校正吸光度(A328校正)计算含量。
c.如果![]() 超出-15%~-3%的范围,或者吸收峰波长不在326~329 nm之间,则供试品应按第二法(皂化法)测定。
超出-15%~-3%的范围,或者吸收峰波长不在326~329 nm之间,则供试品应按第二法(皂化法)测定。
上述判断方法可以用图6-3进行示意:
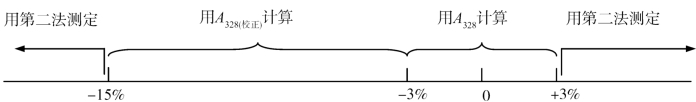
图6-3 直接测定法判断示意图
有关计算:
①求指定波长328 nm处的吸收系数![]()
![]()
式中,A可为A325,也可为A325校正。C为维生素A供试液的浓度,g/100 mL。L为比色池的厚度。
②求维生素A(醋酸酯)的效价:
效价![]()
③维生素A醋酸酯占标示量的百分含量:

式中,A可为A328或A328校正。D为供试品溶液的稀释倍数,如果多次稀释,应为多次稀释倍数之积。W为供试品的取用量,g。![]() 为单位制剂中用于测定部分的平均质量,g。L为比色池的厚度,cm。1 900为维生素A醋酸酯的效价换算因素。标示量是指规定的每一粒胶丸中含维生素A醋酸酯的国际单位。
为单位制剂中用于测定部分的平均质量,g。L为比色池的厚度,cm。1 900为维生素A醋酸酯的效价换算因素。标示量是指规定的每一粒胶丸中含维生素A醋酸酯的国际单位。
B.测定方法二(皂化法。经皂化提取,除去干扰后,测定维生素A醇):精密称取供试品适量(约相当于维生素A总量500单位以上,质量不多于2 g),置皂化瓶中,加乙醇30 mL与50%(g/g)氢氧化钾溶液3 mL,置水浴中煮沸回流30 min,冷却后,自冷凝管顶端加水10 mL冲洗冷凝管内部管壁,将皂化液移至分液漏斗中(分液漏斗活塞涂以甘油淀粉润滑剂),皂化瓶用水60~100 mL分数次洗涤,洗液并入分液漏斗中,用不含过氧化物的乙醚振摇提取4次,每次振摇约5 min,第一次60 mL,以后各次40 mL,合并乙醚液,用水洗涤数次,每次约100 mL,洗涤应缓缓旋动,避免乳化,直至水层遇酚酞指示液不再显红色,乙醚液用铺有脱脂棉与无水硫酸钠的滤器滤过,滤器用乙醚洗涤,洗液与乙醚液合并,放入250 mL容量瓶中,用乙醚稀释至刻度,摇匀;精密量取适量,置蒸发皿内,在水浴上低温蒸发至5 mL后,置减压干燥器中,抽干,迅速加异丙醇溶解并定量稀释制成每1 mL中含维生素A 9~15单位,照紫外-可见分光光度法,在300 nm、310 nm、325 nm与334 nm4个波长处测定吸光度,并测定吸收峰的波长。吸收峰的波长应在323~327 nm之间,计算300 nm波长处的吸光度与325 nm波长处的吸光度的比值(A300/A325)。
根据以下方法判断计算含量时所选用的A值:
a.如果最大吸收波长在323~327 nm之间,且300 nm波长处的吸光度与325 nm波长处的吸光度之比值(A300/A325)不超过0.73,则用公式![]()
![]() 计算校正吸光度。
计算校正吸光度。
b.如果325 nm处的校正吸光度与未校正吸光度相差不超过±3.0%(计算方法:![]() 则仍用未校正吸光度(A325)计算含量;若超过±3.0%,用A325校正计算含量。如图6-4所示。
则仍用未校正吸光度(A325)计算含量;若超过±3.0%,用A325校正计算含量。如图6-4所示。
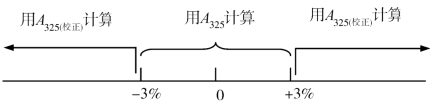
图6-4 皂化法判断示意图
c.如果最大吸收波长不在323~327 nm之间,或300 nm波长处的吸光度与325 nm波长处的吸光度的比值超过0.73,说明供试品中杂质含量过高,应采用色谱法将未皂化部分纯化后再进行测定。
含量计算方法:
维生素A醇占标示量的百分比按下列公式计算:
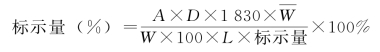
式中,1 830为维生素A醇的效价换算因素。其余有关符号及常数和第一法公式下的含义相同。
注释:①采用三点校正法,328 nm为维生素A的最大吸收波长,其余两点均在最大吸收峰的两侧。因此在测定前应对仪器的波长及比色池在各测定波长的配对性进行校正,否则会产生较大误差。②测定应在半暗室中尽快进行,所用试药不得含有氧化性物质,以防止维生素A被紫外线及氧化性物质破坏。③皂化提取时用水洗醚提取,若强烈振摇可引起乳化,因此应小心缓缓旋动,若产生乳化,可加入少量异丙醇或水破坏之。④实验所用不含过氧化物的乙醚应照麻醉乙醚项下的过氧化物检查,如不符合规定可用5%硫代硫酸钠溶液振摇,静置,分取乙醚层,再用水振摇洗涤1次,重蒸,弃去首尾5%部分,馏出的乙醚再检查过氧化物,应符合规定。⑤换算因素的计算:
维生素A的国际单位规定如下:(https://www.daowen.com)
因为1 IU=0.344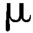 g维生素醋酸酯,1 IU=0.300
g维生素醋酸酯,1 IU=0.300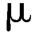 g维生素A醇。故1 g维生素A醋酸酯相当的国际单位为
g维生素A醇。故1 g维生素A醋酸酯相当的国际单位为
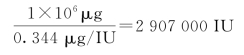
1 g维生素A醇相当的国际单位为
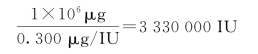
因为换算因素=![]() 故维生素A醋酸酯及维生素A的百分吸收系数
故维生素A醋酸酯及维生素A的百分吸收系数![]() 分别为1 530和1 820。有
分别为1 530和1 820。有

2)高效液相色谱法:《中国药典》用高效液相色谱法测定维生素AD软胶囊和滴剂中的维生素A的组分。下面以维生素AD软胶囊为例介绍。
测定方法:
A.色谱条件:用硅胶为填充剂,以正己-异丙醇(997∶3)为流动相,检测波长为325 nm。
B.对照品溶液的制备:精密称定维生素A对照品适量(约相当于15 mg维生素A醋酸酯),置100 mL量瓶中,加正己烷稀释至刻度,摇匀,再精密量取5 mL,置50 mL容量瓶中,加正己烷稀释至刻度,摇匀。
C.供试品溶液的制备:取装量差异项下的内容物,精密称取适量(约相当于15 mg维生素A醋酸酯),置100 mL量瓶中,加正己烷稀释至刻度,摇匀,再精密量取5 mL,置50 mL容量瓶中,加正己烷稀释至刻度,摇匀。
D.系统适用性溶液的制备:取维生素A对照品适量(约相当于维生素A醋酸酯300 mg),置烧杯中,加入碘试液0.2 mL,混匀,放置约10 min,定量转移至200 mL容量瓶中,加正己烷稀释至刻度,摇匀,再精密量取1 mL,置100 mL容量瓶中,加正己烷稀释至刻度。
E.系统适用性试验:取系统适用性溶液10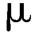 L,注入液相色谱仪,调整色谱系统维生素A醋酸酯主峰与其顺式异构体主峰分离度应大于3.0。精密量取对照品溶液10
L,注入液相色谱仪,调整色谱系统维生素A醋酸酯主峰与其顺式异构体主峰分离度应大于3.0。精密量取对照品溶液10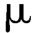 L,注入液相色谱仪,连续进样5次,主成分峰面积的相对标准偏差不得过3.0%。
L,注入液相色谱仪,连续进样5次,主成分峰面积的相对标准偏差不得过3.0%。
F.含量测定:精密量供试品溶液和对照品溶液各10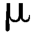 L注入液相色谱仪,记录色谱图,按外标法以峰面积计算含量。
L注入液相色谱仪,记录色谱图,按外标法以峰面积计算含量。
注释:本法适用于维生素A醋酸酯原料及其制剂中维生素A的含量测定。
3)三氯化锑比色法:
A.测定方法:取维生素A对照品,加三氯甲烷溶解并定量稀释成系列浓度的标准溶液,精密量取各液适量,分别加入一定量的三氯化锑-三氯甲烷溶液,在5~10 s内,于620 nm波长处测定吸光度,绘制标准曲线(工作曲线),同法测定供试品溶液的吸光度,根据标准曲线计算供试品含量。
B.原理:维生素A可与三氯化锑的无水三氯甲烷溶液反应产生蓝色,在618~620 nm波长处有最大吸收,符合Beer定律,可用于比色测定。
C.注释:①反应产生的蓝色不稳定,要求操作迅速,加入显色剂后5~10 s内完成测定。②温度对反应显色强度影响较大,要求供试品溶液的测定温度与标准曲线绘制时温度相差应在±1℃以内。③反应介质要求无水,原因是三氯化锑在水中可水解产生氯化氧锑,而使溶液混浊,影响比色结果。④维生素A中的有关物质在相同条件下也可与三氯化锑显色,而非维生素A专属,常使测定结果偏高,应加以注意。⑤三氯化锑可腐蚀皮肤、仪器,应用时应小心。
(二)维生素E的分析
维生素E(Vitamin E)为α-生育酚的醋酸酯,《中国药典》收载的是维生素E粉、片剂、软胶囊和注射剂。
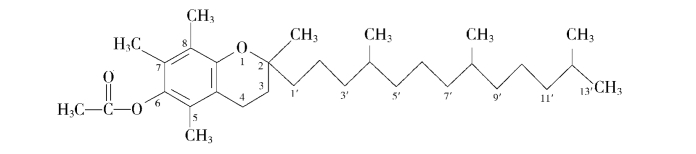
1.结构 维生素E为苯并二氢吡喃醇(色满醇)的衍生物,主要有α、β、γ和δ等多种异构体,其中以α-生育酚生理活性最强。结构中苯并二氢吡喃环上的第2位碳原子(C2)和侧链上2个碳原子(4′、8′)为手性碳原子,具有旋光性,天然品为右旋体,合成品为消旋体。苯环上有一个乙酰化的酚羟基。结构式为
2.性质
(1)还原性:维生素E在无氧条件下对热稳定,但是对氧特别敏感,游离体若露置于空气中和日光下极易氧化变色,其酯相对稳定,但遇光也可变色。其氧化产物可能是醌式化合物或聚合物。
(2)酯的水解:维生素E为α-生育酚醋酸酯,因此在酸性或碱性溶液中加热可水解生成游离生育酚,这也是维生素E中产生游离生育酚的主要原因,故生育酚常作为特殊杂质进行检查。
(3)紫外特征吸收:维生素E分子中具有苯环和酚羟基,其无水乙醇溶液在284 nm波长处有最大吸收,其吸收系数![]() 为41.0~45.0。并且在279 nm波长处有肩峰或拐点。
为41.0~45.0。并且在279 nm波长处有肩峰或拐点。
3.维生素E的分析
(1)性状:本品为微黄色至黄色或黄绿色澄清的黏稠液体,几乎无臭;遇光色渐变深。天然维生素E放置会固化,25℃左右熔化。在无水乙醇、丙酮、乙醚或植物油中易溶,在水中不溶。
(2)鉴别:
1)硝酸反应:硝酸反应是《中国药典》收载的鉴别维生素E方法之一。
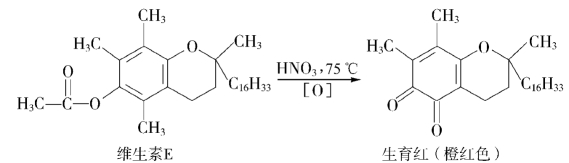
A.方法:取本品约30 mg,加无水乙醇10 mL溶解后,加硝酸2 mL,摇匀,在75℃加热约15 min,溶液应显橙红色。
B.原理:维生素E在酸性条件下,水解生成生育酚,生育酚同时被硝酸氧化生成具
邻醌结构的生育红而显橙红色。反应方程式如下:
2)三氯化铁 联吡啶反应:本反应曾被《中国药典》收载为鉴别维生素E的方法。
联吡啶反应:本反应曾被《中国药典》收载为鉴别维生素E的方法。
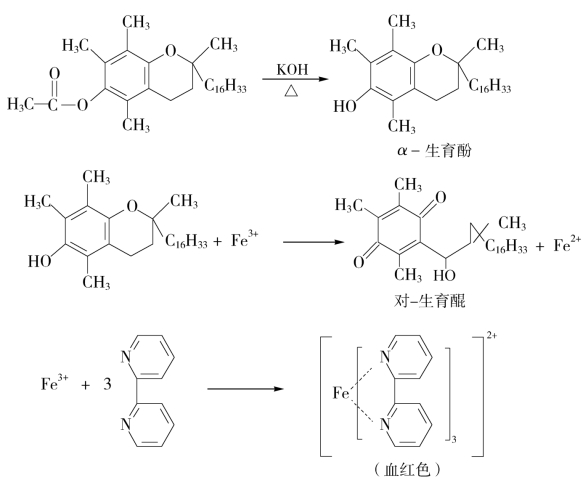
A.方法:取本品约10 mg,加乙醇制氢氧化钾试液2 mL,煮沸5 min,放冷,加水4 mL与乙醚10 mL,振摇,静置使分层;取乙醚液2 mL,加2,2′-联吡啶的乙醇溶液(0.5→100)数滴和三氯化铁的乙醇液(0.2→100)数滴,应显血红色。
B.原理:在乙醇制氢氧化钾的碱性条件下,维生素E发生水解,生成游离生育酚,生育酚被提取至乙醚层,被三氯化铁氧化生成对-生育醌,同时Fe3+被还原为Fe2+,Fe2+与2,2′-联吡啶反应,生成红色的配位化合物。
3)红外分光光度法:《中国药典》采用红外分光光度法鉴别维生素E,采用标准图谱对照法。
4)高效液相色谱法:《中国药典》对维生素E及其制剂均用该法鉴别,要求在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
5)紫外吸收光谱法:《中国药典》利用维生素E的乙醇溶液的紫外吸收特征,对其进行鉴别。取本品,精密称定,加无水乙醇溶解并定量稀释制成每1 mL中约含0.1 mg的溶液,照紫外-可见分光光度法(通则0401),在284 nm的波长处测定吸光度,吸收系数![]() 为41.0~45.0。
为41.0~45.0。
6)气相色谱法:《中国药典》曾采用气相色谱法鉴别维生素E软胶囊和维生素E粉剂。
方法:在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与维生素E对照品溶液主峰的保留时间一致。
7)薄层色谱法:《英国药典》曾采用此法鉴别α-生育酚醋酸酯,方法如下:
A.供试品溶液的制备:精密称取维生素E供试品10 mg,用2 mL环己烷溶解即得。
B.对照品溶液的制备:精密称取维生素E对照品10 mg,用2 mL环己烷溶解即得。
C.色谱条件及方法:将供试品溶液和对照品溶液分别取10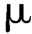 L,点样于硅胶F254板上,以环己烷-乙醚(20∶80)为展开剂,展开至薄层板的2/3处,取出,空气中挥干溶剂,在254 nm紫外灯下检测,供试品溶液所显主斑点的位置和大小应与对照品溶液相同。
L,点样于硅胶F254板上,以环己烷-乙醚(20∶80)为展开剂,展开至薄层板的2/3处,取出,空气中挥干溶剂,在254 nm紫外灯下检测,供试品溶液所显主斑点的位置和大小应与对照品溶液相同。
(3)检查:《中国药典》在维生素E的原料项下要求检查酸度、生育酚(天然型)、有关物质(合成型)及残留溶剂正己烷(天然型)。制剂均需检查有关物质。
1)酸度:检查维生素E制备过程中引入的醋酸。《中国药典》采用的是酸碱滴定法。
A.检查方法:取乙醇和乙醚各15 mL,置锥形瓶中,加酚酞指示液0.5 mL,滴加氢氧化钠滴定液(0.1 mol/L)至微显粉红色。加本品1.0 g溶解后,用氢氧化钠滴定液(0.1 mol/L)滴定,消耗氢氧化钠滴定液(0.1 mol/L)不得超过0.5 mL。
B.原理:本法检查的是维生素E醋酸酯合成时未能完全酯化的酸,在酚酞指示液的条件下,用规定浓度的氢氧化钠滴定供试品中的酸性杂质,以消耗氢氧化钠滴定液的毫升数作为限度指标,以控制本品中的含酸性物质的量。
C.注释:第一次用氢氧化钠滴定是为了消除乙醇和乙醚中的酸性杂质的干扰。
2)生育酚:《中国药典》用铈量法检查天然型维生素E中未酯化的生育酚。
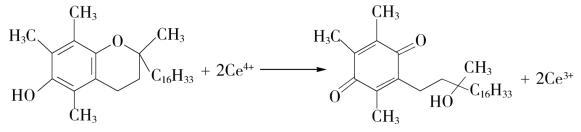
A.检查方法:取本品0.10 g,加无水乙醇5 mL,溶解后,加二苯胺试液1滴,用硫酸铈滴定液(0.01 mol/L)滴定,消耗的硫酸铈滴定液(0.01 mol/L)不得超过1.0 mL。
B.原理:生育酚具有还原性,可被硫酸铈定量氧化,通过在规定条件下,限制硫酸铈滴定液(0.01 mol/L)的限量来控制生育酚的限量。反应式为
3)有关物质:合成型维生素E制备过程复杂,中间产物、副产物等种类多,《中国药典》采用气相色谱法检查合成维生素E在制备过程中产生的有关物质。
检查方法:取本品,用正己烷稀释制成每1 mL中约含2.5 mg的溶液,作为供试品溶液;精密量取适量,用正己烷定量稀释制成每1 mL中含25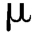 g的溶液,作为对照溶液。照含量测定项下的色谱条件,精密量取供试品溶液与对照溶液各1
g的溶液,作为对照溶液。照含量测定项下的色谱条件,精密量取供试品溶液与对照溶液各1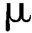 L,分别注入气相色谱仪,记录色谱图至主成分峰保留时间的2倍,供试品溶液的色谱图中如有杂质峰,α-生育酚(杂质Ⅰ)(相对保留时间约为0.87)的峰面积不得大于对照溶液主峰面积(1.0%),其他单个杂质峰面积不得大于对照溶液主峰面积的1.5倍(1.5%),各杂质峰面积的和不得大于对照溶液主峰面积的2.5倍(2.5%)。
L,分别注入气相色谱仪,记录色谱图至主成分峰保留时间的2倍,供试品溶液的色谱图中如有杂质峰,α-生育酚(杂质Ⅰ)(相对保留时间约为0.87)的峰面积不得大于对照溶液主峰面积(1.0%),其他单个杂质峰面积不得大于对照溶液主峰面积的1.5倍(1.5%),各杂质峰面积的和不得大于对照溶液主峰面积的2.5倍(2.5%)。
注释:本法为不加校正因子的主成分自身对照法。
4)残留溶剂:《中国药典》采用气相色谱法检查天然型维生素E中的残留溶剂正己烷。
药物的残留溶剂指在原料药或辅料的生产中,以及在制剂制备过程中使用的,但在工艺过程中未能完全去除的有机溶剂。《中国药典》采用气相色谱法测定残留在药物中的对人体有害的有机溶剂。
《中国药典》规定用毛细管柱顶空进样等温法(通则0861第一法),检查天然型维生素E中的有机溶剂正己烷:取对照品溶液和供试品溶液,分别连续进样不少于2次,测定待测峰的峰面积。《中国药典》规定正丁烷的限度不得过0.029%。
注释:①对照品溶液与供试品溶液必须使用相同的顶空条件。②由于静态顶空进样时,抽取的是处于气液平衡的顶部气体,所以每个顶空瓶只能取样一次。③应根据供试品中残留溶剂的沸点和溶解介质的沸点选择顶空温度。对沸点较高的残留溶剂,通常选择较高的顶空温度;但此时应兼顾供试品的热分解特性,尽量避免供试品产生的挥发性热分解产物对测定的干扰。④顶空平衡时间一般为30~45 min,以保证供试品溶液的气-液两相有足够的时间达到平衡。顶空时间通常不宜过长,如超过60 min,可能引起顶空瓶的气密性变差,导致定量准确性的降低。⑤对于有传输管的顶空进样器,传输管温度应适当,通常比进样针温度高10℃左右。
(4)含量测定:维生素E的含量测定方法很多,如铈量法(利用维生素E的水解产物生育酚的还原性)、三氯化铁与2,2-联吡啶比色法(将Fe3+还原为Fe2+,再与2,2′-联吡啶生成有色配位化合物后进行比色测定)、羟肟酸铁比色法、紫外分光光度法、荧光法、色谱法等。《中国药典》收载的维生素E及其片剂、软胶囊、注射液、粉剂均用气相色谱法测定含量,国外药典大多也采用该法测其含量。该法简便、快速、专属性强。
1)气相色谱法:维生素E测定方法如下:
A.色谱条件:以硅酮(OV-17)为固定液,涂布浓度为2%的填充柱;或用100%二甲基聚硅氧烷为固定液的毛细管柱;柱温265℃。氢火焰离子化检测器(FID)。
B.系统试用性试验:理论塔板数按维生素E计算不低于500(填充柱)或5 000(毛细管柱),维生素E峰与内标物质峰的分离度应大于1.5。
C.校正因子的测定:取正三十二烷适量,加正己烷溶解并稀释成每1 mL中含1.0 mg的溶液,摇匀,作为内标溶液。另取维生素E对照品约20 mg,精密称定,置棕色具塞锥形瓶中,精密加入内标溶液10 mL,密塞,振摇使溶解,取1~3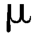 L进样,计算校正因子。
L进样,计算校正因子。
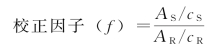
式中,AS为内标物(正三十二烷)的峰面积或峰高;AR为维生素E对照品的峰面积或峰高;cS为内标物质的浓度;cR为对照品的浓度。
D.样品的含量测定:取本品约20 mg,精密称定,置棕色具塞锥形瓶中,精密加入内标溶液10 mL,密塞,振摇使溶解;取1~3 L进样,测定,按内标法计算,即得。
L进样,测定,按内标法计算,即得。
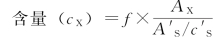
式中,AX为供试品的峰面积或峰高;cX为供试品的浓度;![]() 为内标物质的峰面积或峰高;
为内标物质的峰面积或峰高;![]() 为内标物质的浓度;f为内标法校正因子。
为内标物质的浓度;f为内标法校正因子。
注释:①本法可分离维生素E及其异构体,能选择性地测定维生素E的含量。若维生素E用酚羟基衍生化(如醋酸酯)能更好地改善维生素E的分离,同时可缩短分析时间。②本法采用内标法定量,进样量和操作条件的变化对结果无影响。③本法应用氢火焰离子化检测器,其检测器温度一般应高于柱温,并不得低于150℃,以免水汽凝结,通常250~350℃。④柱温箱控温精度应在±1℃。⑤本法采用溶液直接进样,进样口温度应高于柱温30~50℃。⑥若应用毛细管柱进样量应减少,一般应分流以免过载。
2)高效液相色谱法:《日本药局方》曾用该法测定维生素E的含量。本法可用于测定α-生育酚及其醋酸酯,现以α-生育酚的测定(外标法)介绍如下:
A.色谱条件:色谱柱为内径4 mm,柱长15~30 cm的不锈钢柱;固定相为十八烷基硅烷键合硅胶(5~10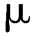 m);流动相为甲醇-水(49∶1);紫外检测器,检测波长292 nm。
m);流动相为甲醇-水(49∶1);紫外检测器,检测波长292 nm。
B.系统适用性试验:取生育酚及醋酸酯标准品各0.05 g,加无水乙醇溶解并稀释至50 mL,用此液进样20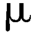 L,记录色谱图,两者的分离度应大于2.6(生育酚先出峰)。取标准溶液20
L,记录色谱图,两者的分离度应大于2.6(生育酚先出峰)。取标准溶液20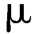 L进样,连续5次,峰高的相对标准差应小于0.8%。
L进样,连续5次,峰高的相对标准差应小于0.8%。
C.测定方法:取α-生育酚供试品和标准品各0.05 g,精密称定,以无水乙醇溶解并稀释至50.0 mL,即得供试品溶液和标准品溶液。取供试品溶液和标准品溶液各20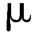 L,分别进样,测得峰高分别为HX和HR,按下式计算含量:
L,分别进样,测得峰高分别为HX和HR,按下式计算含量:
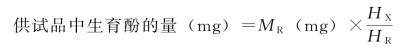
式中,HX为供试品中生育酚的峰高;HR为对照品中生育酚的峰高;MR为生育酚对照品的量。
注释:①测维生素E的含量可用正相或反相高效液相色谱法,且条件各有不同。②本法还可测食品、饲料和生物样品中维生素E的含量。
(3)铈量法:
1)方法:取本品0.2 g,精密称定,置具塞棕色锥形瓶中,加无水乙醇25 mL,使溶解,加硫酸的无水乙醇溶液(3→25)25 mL,加热回流3 h,放冷,转移至100 mL棕色容量瓶中,用少量无水乙醇洗涤容器,洗液并入容量瓶中,加无水乙醇稀释至刻度,摇匀,精密量取5 mL,加乙醇20 mL、水10 mL与二苯胺指示液2滴,用硫酸铈滴定液(0.01 mol/l)滴定,滴定速度以每10 s 25滴为宜,至溶液由亮黄色转变为灰紫色,持续10 s即为终点,并将滴定结果用空白试验校正,即得。每1 mL的硫酸铈滴定液(0.01 mol/L)相当于2.36 mg的H31H52O3。
2)原理:维生素E在酸性条件下加热回流,即水解生成游离生育酚,后者可被硫酸铈定量氧化为对-生育醌,稍过量的硫酸铈氧化二苯胺指示剂,使其颜色发生改变而指示滴定终点。
注释:维生素E以在硫酸酸性条件下水解为宜,因为在碱性溶液中游离生育酚易被空气中的氧气氧化,而且硫酸铈在酸性溶液中稳定,否则会因水解而影响测定。
