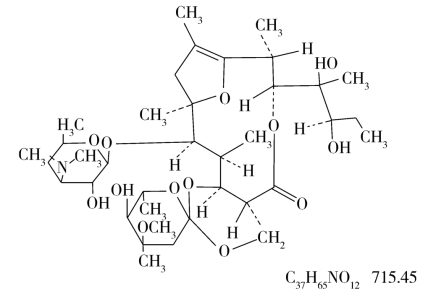
大环内酯类抗生素的分析
大环内酯类抗生素仅次于β-内酰胺类抗生素及氨基糖苷类抗生素,是由链霉素产生的一类弱碱性抗生素,其结构特征为分子中含有1个内酯结构的十四元、十五元或十六元大环。通过内酯环上的羟基和去氧氨基糖或6-去氧糖缩合成碱性苷。这类药物主要有红霉素、麦迪霉素、螺旋霉素、乙酰螺旋霉素和乙酰麦迪霉素等。
(一)化学结构与性质
1.典型药物 大环内酯类抗生素结构中含有1个十四元、十五元或十六元大环内酯结构,并通过内酯环上的羟基和去氧氨基糖或6-去氧糖缩合成碱性苷。代表药物结构如下:

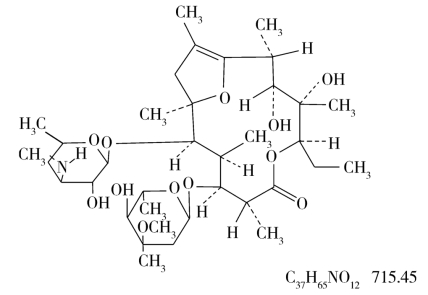
红霉素
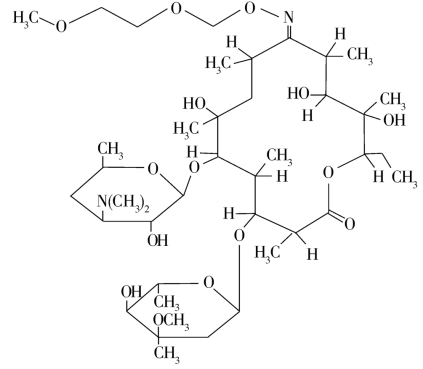
罗红霉素
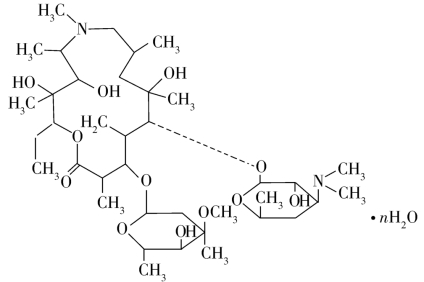
阿奇霉素
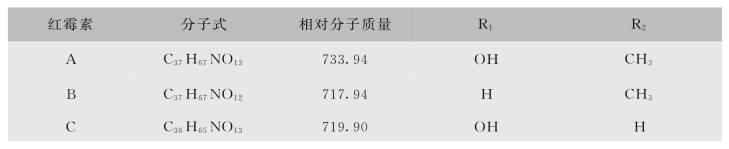
红霉素是由红霉内酯、去氧氨基糖和红霉糖缩合而成的碱性苷。红霉素在生物发酵过程中,同时产生红霉素A、红霉素B、红霉素C三种类似物(表6-18)及红霉素D生物合成中间体,其中以红霉素A的活性最高,为红霉素药物的有效成分。国产红霉素为红霉素A和红霉素C,红霉素C的理化性质和抗菌谱与红霉素A相似,但其抗菌活性只有红霉素A的30%~60%,故《中国药典》规定需进行红霉素A、红霉素B、红霉素C组分及有关物质的检查,采用的是高效液相色谱法。
表6-18 红霉素类药物
2.性质
(1)溶解性:大环内酯类抗生素中含有氨基,一般均为无色的碱性化合物,易溶于有机溶剂。可与酸成盐,其盐易溶于水。
(2)稳定性:大环内酯类抗生素中含有内酯与苷键,化学性质不稳定,在酸性条件下易发生苷键水解,在碱性条件下发生内酯环开环破裂及脱酰基反应,导致药物的抗菌作用降低或消失。
(3)还原性:红霉素分子中含有脱氧氨基己糖和红霉糖,具有还原糖的性质,能将斐林试液还原,生成红色氧化亚铜;与氨制硝酸银试液发生银镜反应;与浓H2SO4作用显色等,可用于鉴别。
(4)旋光性:红霉素具有旋光性,其无水乙醇溶液的![]() 为-71°~-78°;在紫外光区有吸收,λmax=280 nm,可用于鉴别及含量测定。
为-71°~-78°;在紫外光区有吸收,λmax=280 nm,可用于鉴别及含量测定。
(二)红霉素的分析
本品按无水物计算,每1 mg的效价不得少于920红霉素单位。
1.性状 本品为白色或类白色的结晶或粉末;无臭;微有引湿性。本品在甲醇、乙醇或丙酮中易溶,在水中极微溶解。比旋度测定,取本品,精密称定,加无水乙醇溶解并定量稀释制成每1 mL中约含20 mg的溶液,放置30 min后依法测定,比旋度为-71°~-78°。
2.鉴别
(1)高效液相色谱法:在红霉素组分项下记录的色谱图中,供试品溶液主峰的保留时间应与标准品溶液主峰的保留时间一致。
原理:红霉素中含有多种组分,其药物成分以红霉素A组分为主,标准品中含有红霉素A、红霉素B、红霉素C和红霉素烯醇醚成分,采用高效液相色谱法可将各组分先分离再分析。色谱条件:固定相为十八烷基硅烷键合硅胶;流动相为磷酸盐溶液(取磷酸氢二钾8.7 g,加水1 000 mL,用20%磷酸调节pH值至8.2)-乙腈(40∶60),流速为0.8~1.0 mL/min;检测波长为215 nm。标准品中各组分色谱峰出峰顺序为红霉素C峰、红霉素A峰、红霉素B峰和红霉素烯醇醚峰。
(2)红外光谱法:本品的红外光吸收图谱应与对照的图谱一致。如不一致,取本品与标准品适量,加少量三氯甲烷溶解后,水浴蒸干,置五氧化二磷干燥器中减压干燥后测定,除2 050~1 980 cm-1波长范围外,应与标准品的图谱一致。
(3)薄层色谱法:取本品细粉适量,加甲醇制成每1 mL中约含红霉素2.5 mg的溶液,滤过,取续滤液作为供试品溶液。另取红霉素标准品适量,加甲醇制成每1 mL,约含红霉素2.5 mg的溶液,作为标准品溶液。照薄层色谱法试验,吸取上述两种溶液各10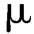 L,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇(85∶15)为展开剂,展开,晾干,喷以乙醇-对甲氨基苯甲醛-硫酸(90∶5∶5)的混合溶液,置100℃加热约数分钟,至出现黑色或红紫色斑点。供试品溶液所显主斑点的位置和颜色应与标准品溶液主斑点的位置和颜色相同。
L,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇(85∶15)为展开剂,展开,晾干,喷以乙醇-对甲氨基苯甲醛-硫酸(90∶5∶5)的混合溶液,置100℃加热约数分钟,至出现黑色或红紫色斑点。供试品溶液所显主斑点的位置和颜色应与标准品溶液主斑点的位置和颜色相同。
原理:红霉素肠溶片、肠溶胶囊均采用此法进行鉴别。与高效液相色谱法同为色谱法,《中国药典》规定选做1项即可。(https://www.daowen.com)
3.检查
(1)碱度:取本品0.1 g,加水150 mL,振摇,依法测定,pH值应为8.0~10.5。
原理:大环内酯类抗生素结构中的内酯环及糖苷键,对酸、碱均不稳定;可发生开环及苷键水解等反应,导致药物的抗菌活性降低或丧失。
(2)有关物质:取本品约40 mg,置10 mL容量瓶中,加甲醇4 mL使溶解,用pH=8.0磷酸盐溶液(取磷酸氢二钾11.5 g,加水900 mL使溶解,用10%磷酸溶液调节pH值至8.0,用水稀释成1 000 mL)稀释至刻度,摇匀,作为供试品溶液;精密量取1 mL,置100 mL容量瓶中,用上述pH=8.0磷酸盐溶液-甲醇(3∶2)稀释至刻度,摇匀,作为对照溶液;精密量取对照溶液适量,用pH=8.0磷酸盐溶液-甲醇(3∶2)定量稀释制成每1 mL中约含4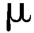 g的溶液,作为灵敏度溶液。照红霉素组分检查项下的色谱条件,量取灵敏度溶液100
g的溶液,作为灵敏度溶液。照红霉素组分检查项下的色谱条件,量取灵敏度溶液100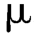 L注入液相色谱仪,记录色谱图,主成分色谱峰高的信噪比应大于10。精密量取供试品溶液和对照溶液各100
L注入液相色谱仪,记录色谱图,主成分色谱峰高的信噪比应大于10。精密量取供试品溶液和对照溶液各100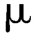 L,分别注入液相色谱仪,记录色谱图。供试品溶液色谱图中如有杂质峰,杂质C峰面积不得大于对照溶液主峰面积的3倍(3.0%),杂质E与杂质F校正后的峰面积(乘以校正因子0.08)均不得大于对照溶液主峰面积的2倍(2.0%),杂质D校正后的峰面积(乘以校正因子2)不得大于对照溶液主峰面积的2倍(2.0%),杂质A、杂质B及其他单个杂质的峰面积均不得大于对照溶液主峰面积的2倍(2.0%),各杂质校正后的峰面积之和不得大于对照溶液主峰面积的7倍(7.0%)。供试品溶液色谱图中小于灵敏度溶液主峰面积的峰忽略不计。
L,分别注入液相色谱仪,记录色谱图。供试品溶液色谱图中如有杂质峰,杂质C峰面积不得大于对照溶液主峰面积的3倍(3.0%),杂质E与杂质F校正后的峰面积(乘以校正因子0.08)均不得大于对照溶液主峰面积的2倍(2.0%),杂质D校正后的峰面积(乘以校正因子2)不得大于对照溶液主峰面积的2倍(2.0%),杂质A、杂质B及其他单个杂质的峰面积均不得大于对照溶液主峰面积的2倍(2.0%),各杂质校正后的峰面积之和不得大于对照溶液主峰面积的7倍(7.0%)。供试品溶液色谱图中小于灵敏度溶液主峰面积的峰忽略不计。
(3)红霉素组分:照高效液相色谱法测定。
1)色谱条件与系统适用性试验:用十八烷基硅烷键合硅胶为填充剂(XTerra RP C18柱,4.6 mm×250 mm,3.5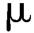 m或效能相当的色谱柱);以乙腈-0.2 mol/L磷酸氢二钾溶液(用磷酸调节pH值至7.0)-水(35∶5∶60)为流动相A,以乙腈-0.2 mol/L磷酸氢二钾溶液(用磷酸调节pH值至7.0-水(50∶5∶45)为流动相B,先以流动相A等度洗脱,待红霉素B洗脱完毕后立即按表6-19进行线性梯度洗脱,流速为1.0 mL/min,检测波长为210 nm,柱温为65℃。精密称取红霉素标准品约40 mg,置10 mL容量瓶中,加甲醇4 mL使溶解,用有关物质检查项下的pH=8.0磷酸盐溶液稀释至刻度,摇匀,量取100
m或效能相当的色谱柱);以乙腈-0.2 mol/L磷酸氢二钾溶液(用磷酸调节pH值至7.0)-水(35∶5∶60)为流动相A,以乙腈-0.2 mol/L磷酸氢二钾溶液(用磷酸调节pH值至7.0-水(50∶5∶45)为流动相B,先以流动相A等度洗脱,待红霉素B洗脱完毕后立即按表6-19进行线性梯度洗脱,流速为1.0 mL/min,检测波长为210 nm,柱温为65℃。精密称取红霉素标准品约40 mg,置10 mL容量瓶中,加甲醇4 mL使溶解,用有关物质检查项下的pH=8.0磷酸盐溶液稀释至刻度,摇匀,量取100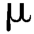 L注入液相色谱仪,记录色谱图,红霉素A峰的拖尾因子应不大于2.0。取红霉素系统适用性对照品40 mg,置10 mL容量瓶中,加甲醇4 mL使溶解,用上述pH=8.0磷酸盐溶液稀释至刻度,摇匀,量取100
L注入液相色谱仪,记录色谱图,红霉素A峰的拖尾因子应不大于2.0。取红霉素系统适用性对照品40 mg,置10 mL容量瓶中,加甲醇4 mL使溶解,用上述pH=8.0磷酸盐溶液稀释至刻度,摇匀,量取100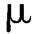 L注入色谱仪,记录色谱图,应与红霉素系统适用性对照品的标准图谱一致,红霉素A峰的保留时间约为23 min,杂质A、杂质B、杂质C、杂质D、杂质E和杂质F的相对保留时间分别约为0.4、0.5、0.9、1.6、2.3和1.8,红霉素B和红霉素C的相对保留时间分别约为1.7和0.55,杂质B峰和红霉素C峰、红霉素B峰和杂质F峰之间的分离度应不小于1.2,杂质C峰和红霉素A峰之间的分离度应符合要求。
L注入色谱仪,记录色谱图,应与红霉素系统适用性对照品的标准图谱一致,红霉素A峰的保留时间约为23 min,杂质A、杂质B、杂质C、杂质D、杂质E和杂质F的相对保留时间分别约为0.4、0.5、0.9、1.6、2.3和1.8,红霉素B和红霉素C的相对保留时间分别约为1.7和0.55,杂质B峰和红霉素C峰、红霉素B峰和杂质F峰之间的分离度应不小于1.2,杂质C峰和红霉素A峰之间的分离度应符合要求。
表6-19 线性梯度洗脱

注:tg为红霉素B的保留时间
2)测定法:精密称取本品约40 mg,置10 mL容量瓶中,加甲醇4 mL使溶解,用上述pH=8.0磷酸盐溶液稀释至刻度,摇匀,作为供试品溶液;精密称取红霉素标准品约40 mg,置10 mL容量瓶中,加甲醇4 mL使溶解,用上述pH=8.0磷酸盐溶液稀释至刻度,摇匀,作为标准品溶液(1);精密量取标准品溶液(1)1 mL,置100 mL容量瓶中,用上述pH=8.0磷酸盐溶液-甲醇(3∶2)稀释至刻度,摇匀,作为标准品溶液(2)。精密量取供试品溶液与标准品溶液(1)、标准品溶液(2)各100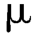 L,分别注入液相色谱仪,记录色谱图。按外标法以标准品溶液(1)中红霉素A的峰面积计算供试品中红霉素A的含量,按无水物计,不得少于93.0%;按外标法以标准品溶液(2)中红霉素A的峰面积计算供试品中红霉素B和红霉素C的含量,按无水物计,均不得过3.0%。
L,分别注入液相色谱仪,记录色谱图。按外标法以标准品溶液(1)中红霉素A的峰面积计算供试品中红霉素A的含量,按无水物计,不得少于93.0%;按外标法以标准品溶液(2)中红霉素A的峰面积计算供试品中红霉素B和红霉素C的含量,按无水物计,均不得过3.0%。
4.含量测定 精密称取本品适量,加乙醇(10 mg加乙醇1 mL)溶解后,用灭菌水定量制成每1 mL中约含1 000单位的溶液,照抗生素微生物检定法测定,可信限率不得大于7%。1 000红霉素单位相当于1 mg的C37H67N013。图6-5为红霉素杂质测定。
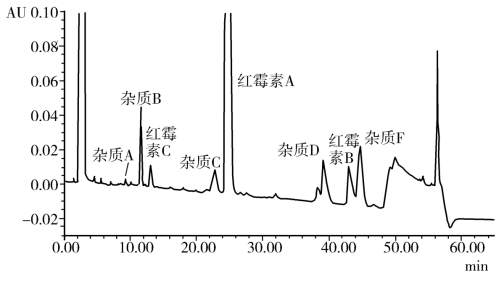
图6-5 红霉素杂质测定
5.杂质
(1)杂质A[红霉素F(erythromycin F)]:
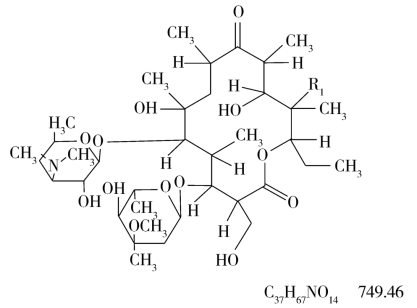
(2)杂质B[N-去甲基红霉素A(N-demethylerythromycin A)]:
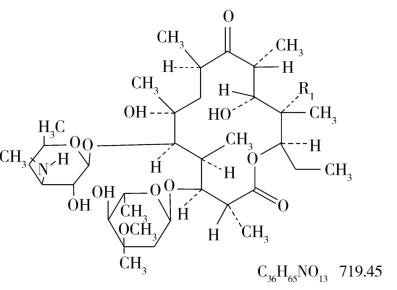
(3)杂质C[红霉素E(erythromycin E)]:

(4)杂质D[脱水红霉素A(anhydroerythromycin A)]:
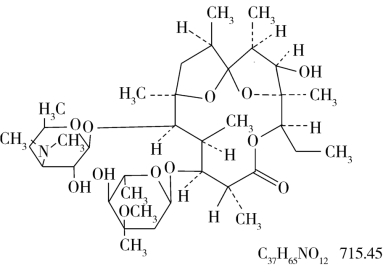
(5)杂质E[红霉素A烯醇醚(erythromycin A enol ether)]:
(6)杂质F[红霉素A烯醇醚(pseudoerythromycin A enol ether)]: