特发性间质性肺炎
特发性间质性肺炎分为七型(表2-1),所有的病例应由有经验的临床呼吸科医师、放射科医师和病理科医师共同讨论完成最后诊断,即临床-影像-病理诊断(CRP诊断)。
表2-1 2002年ATS/ERS的特发性间质性肺炎的分型

2012年美国胸科学会(ATS)和欧洲呼吸学会(ERS)又对间质性肺疾病进行了进一步的分类。主要的分类框架仍保留,但进一步将特发性间质性肺炎分为家族性和非家族性,不论家族性和非家族性均分为慢性纤维化如特发性肺纤维化和特发性非特异性间质性肺炎,急性和亚急性的肺纤维化如急性间质性肺炎和隐原性机化性肺炎,以及吸烟相关的间质性肺炎如呼吸性细支气管炎伴间质性肺炎和脱屑性间质性肺炎。还可分为常见的、少见的和不可分型的特发性间质性肺炎。常见的为特发性肺纤维化,特发性非特性异性间质性肺炎,呼吸性细支气管炎伴间质性肺炎,脱屑性间质性肺炎,隐原性机化性肺炎,急性间质性肺炎。少见的为特发性淋巴间质性肺炎和特发性胸膜肺的弹力纤维增生症。下面分述不同类型特发性间质性肺炎的特点。
(一)急性间质性肺炎
急性间质性肺炎(acute interstitial pneumonia,AIP)是一种不明原因的暴发性的疾病,常发生于既往健康的人,组织学为弥漫性的肺泡损害。
1.病理特点 AIP病理改变分为急性期(又称渗出期)和机化期(又称增殖期)。急性期的病理特点为肺泡上皮乃至上皮基底膜的损伤,炎性细胞进入肺泡腔内,在受损的肺泡壁上可见Ⅱ型上皮细胞再生并替代Ⅰ型上皮细胞,可见灶状分布的由脱落的上皮细胞和纤维蛋白所构成的透明膜充填在肺泡腔内。另可见肺泡隔的水肿和肺泡腔内出血。此期在肺泡腔内逐渐可见纤维母细胞成分,进而导致肺泡腔内纤维化。机化期的病理特点是肺泡腔内及肺泡隔内呈现纤维化并有显著的肺泡壁增厚。其特点为纤维化为活动的,主要由增生的纤维母细胞和肌纤维母细胞组成,伴有轻度胶原沉积。此外还有细支气管鳞状上皮化生。
2.诊断 AIP发病无明显性别差异,平均发病年龄49岁,年龄从7~77岁病例均有报告。无明显性别差异。起病急剧,表现为咳嗽,呼吸困难,随之很快进入呼吸衰竭,类似ARDS。多数病例AIP发病前有“感冒”样表现,半数患儿有发热。常规实验室检查无特异性。AIP病死率极高。
急性间质性肺炎的CT的表现主要为弥漫的磨玻璃影和含气腔的实变影。可见牵拉性的支气管扩张。区域性的磨玻璃改变和牵拉性的支气管扩张与疾病的病程有关。研究还发现肺磨玻璃影或肺实变合并牵拉性支气管扩张较未合并牵拉性支气管扩张者预后为差。前者肺组织病理为弥漫性肺泡损伤的纤维化期或机化的晚期,后者为弥漫性肺泡损伤的渗出期或早期纤维化期。激素在早期机化期有效。
3.治疗 AIP治疗上无特殊方法,可采用ARDS治疗方法。AIP死亡率极高12,如果除外尸检诊断的AIP病例,死亡率可达50 ~88
~88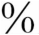 (平均62
(平均62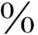 ),平均生存期限短,多在1~2个月间死亡。近年有应用大剂量的糖皮质激素冲击治疗成功的报道。北京儿童医院有3例诊断为急性间质性肺炎应用激素得到成功的治疗,尚在长期的追踪之中。
),平均生存期限短,多在1~2个月间死亡。近年有应用大剂量的糖皮质激素冲击治疗成功的报道。北京儿童医院有3例诊断为急性间质性肺炎应用激素得到成功的治疗,尚在长期的追踪之中。
(二)特发性肺纤维化
特发性肺纤维化(idiopathic pulmonary fibrosis,IPF)即普通间质性肺炎(usual interstitial pneumonia,UIP)。
1.病理特点 其病理特点为出现片状、不均一、分布多变的间质改变。每个低倍镜下都不一致,包括间质纤维化、间质炎症及蜂窝变与正常肺组织间呈灶状分布、交替出现。可见纤维母细胞灶分布于炎症区、纤维变区和蜂窝变区,为UIP诊断所必需的条件,但并不具有特异病理意义。纤维母细胞灶代表纤维化正在进行,并非既往已发生损害的结局。由此可见成纤维细胞灶、伴胶原沉积的瘢痕化和蜂窝变组成的不同时相病变共存构成诊断UIP的重要特征。
2.诊断 主要发生在成年人,男女比例约为2∶1。UIP起病过程隐袭,主要表现为干咳气短,活动时更明显。全身症状有发热、倦怠、关节痛及体重下降。50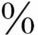 患儿体检发现杵状指(趾),大多数可闻及细小爆裂音(velcro啰音)。儿童病理证实得UIP很少,儿童仅有一例15岁患儿证实为UIP,并且与ABCA3基因的突变有关。以往儿童报道的100多例的IPF中,无纤维母细胞灶的存在,并且多数预后较好,不符合UIP/IPF的病理和临床特点。
患儿体检发现杵状指(趾),大多数可闻及细小爆裂音(velcro啰音)。儿童病理证实得UIP很少,儿童仅有一例15岁患儿证实为UIP,并且与ABCA3基因的突变有关。以往儿童报道的100多例的IPF中,无纤维母细胞灶的存在,并且多数预后较好,不符合UIP/IPF的病理和临床特点。
实验室检查常出现异常,如血沉的增快,抗核抗体阳性,冷球蛋白阳性,类风湿因子阳性等。
UIP的胸片和CT可发现肺容积缩小,呈线状、网状阴影、磨玻璃样改变及不同程度蜂窝状变。磨玻璃影所占区域<30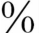 。上述病变在肺底明显。并且病变主要累及外周肺野和下肺区域。
。上述病变在肺底明显。并且病变主要累及外周肺野和下肺区域。
肺功能呈中至重度的限制性通气障碍及弥散障碍。支气管肺泡灌洗液见中性粒细胞比例升高,轻度嗜酸粒细胞增多。
3.治疗 尽管只有10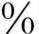 ~20
~20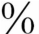 患儿可见到临床效果,应用糖皮质激素仍是主要手段;有证据表明环磷酰胺/硫唑嘌呤也有一定效果,最近有报告秋水仙碱效果与激素相近。对治疗无反应的终末期患儿可以考虑肺移植。
患儿可见到临床效果,应用糖皮质激素仍是主要手段;有证据表明环磷酰胺/硫唑嘌呤也有一定效果,最近有报告秋水仙碱效果与激素相近。对治疗无反应的终末期患儿可以考虑肺移植。
4.预后 UIP预后不良,死亡率为59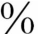 ~70
~70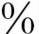 ,平均生存期为2.8~6年。极少数患儿自然缓解或稳定,多需治疗。
,平均生存期为2.8~6年。极少数患儿自然缓解或稳定,多需治疗。
(三)脱屑性间质性肺炎
1.组织学特点 脱屑性间质性肺炎(desquamative interstitial pneumoma,DIP)组织学特点为肺泡腔内肺泡巨噬细胞均匀分布,见散在的多核巨细胞。同时有轻中度肺泡间隔增厚,主要为胶原沉积而少有细胞浸润。在低倍镜下各视野外观呈单一均匀性分布,而与UIP分布的多样性形成鲜明对比。在成人多见于吸烟的人群。在小儿诊断的DIP,多为表面活性蛋白C(SP-C)和ABCA3的基因突变所致。并且比成人的DIP预后差。
2.诊断 DIP男性发病是女性的2倍。主要症状为干咳和呼吸困难,通常隐袭起病。半数患儿出现杵状指(趾)。实验室通常无特殊发现。肺生理也表现为限制性通气功能障碍,弥散功能障碍,但不如UIP明显。
DIP的主要影像学的改变在中、下肺区域,有时呈外周分布。主要为磨玻璃样改变,有时可见不规则的线状影和网状结节影。以广泛性磨玻璃状改变和轻度纤维化的改变多提示脱屑性间质性肺炎。与UIP不同,DIP通常不出现蜂窝变。
3.治疗 治疗儿童主要采用糖皮质激素治疗,成人为戒烟和激素治疗。成人患儿对糖皮质激素治疗反应较好。10年生存在70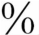 以上。小儿DIP对激素治疗反应差。(https://www.daowen.com)
以上。小儿DIP对激素治疗反应差。(https://www.daowen.com)
(四)呼吸性细支气管相关的间质性肺炎
呼吸性细支气管相关的间质性肺炎(respiratory bronchiololi-tis-associated interstitial lung disease,RBILD)与DIP极为相似,病理为呼吸性细支气管炎伴发周围的气腔内大量含色素的巨噬细胞聚积,与DIP的病理不同之处是肺泡巨噬细胞聚集只局限于这些区域而远端气腔不受累,而有明显的呼吸性细支气管炎。近年来认为DIP/RBILD可能为同一疾病的不同结果,因为这两种改变并没有明确的组织学上的区别,而且表现和病程相似。
RBILD发病平均年龄36岁,男性略多于女性,所有患儿均是吸烟者,主要症状是咳嗽气短。杵状指(趾)相对少见。影像学上2/3出现网状,网状结节影,未见磨玻璃影;胸部影像学也可以正常。BALF见含色素沉着的肺泡巨噬细胞。成人病例戒烟后病情通常可以改变或稳定;经糖皮质激素治疗的少数病例收到明显效果。可以长期稳定生存。
(五)非特异性的间质性肺炎
非特异性的间质性肺炎(nonspecific interstitial pneumonia,NSIP)是指难以分类的间质性的肺炎,随后不断加以摒除,逐渐演变为独立的临床病理概念。虽然NSIP的病因不清,但可能与下列情况相关:某些潜在的结缔组织疾病、某些药物反应、有机粉尘的吸入、急性肺损伤的缓解期等,也可见于BOOP的不典型的活检区域。这种情形类似于BOOP,既可是很多病因的继发表现,又可以是特发性的。结合临床影像和病理资料来诊断NSIP很重要。
1.病理特点 NSIP特点是肺泡壁内出现不同程度的炎症及纤维化,但缺乏诊断UIP、DIP或AIP的特异表现,或表现炎症伴轻度纤维化,或表现为炎症及纤维化的混合。病变可以是灶状,间以未受波及的肺组织,但病变在时相上是均一的,这一点与UIP形成强烈的对比。肺泡间隔内由淋巴细胞和浆细胞混合构成的慢性炎性细胞浸润是NSIP的特点。浆细胞通常很多,这种病变在细支气管周围的间质更明显。
在NSIP,近50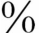 病例可见腔内机化病灶,即BOOP的特征表现,但通常病灶小而显著,仅占整个病变的10
病例可见腔内机化病灶,即BOOP的特征表现,但通常病灶小而显著,仅占整个病变的10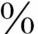 以下;30
以下;30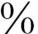 病例有片状分布的肺泡腔内炎细胞聚积,这一点容易与DIP相区别,因为NSIP有其灶性分布和明显的间质纤维化;1/4的NSIP可出现淋巴样聚合体伴发中心(所谓淋巴样增生),这些病变散在分布,为数不多;罕见的还有形成不良呈灶性分布的非坏死性肉芽肿。
病例有片状分布的肺泡腔内炎细胞聚积,这一点容易与DIP相区别,因为NSIP有其灶性分布和明显的间质纤维化;1/4的NSIP可出现淋巴样聚合体伴发中心(所谓淋巴样增生),这些病变散在分布,为数不多;罕见的还有形成不良呈灶性分布的非坏死性肉芽肿。
2.诊断 NSIP主要发生于中年人,多为非吸烟者。平均年龄49岁,男∶女=1∶1.4,也有多见于女性患儿的报道。NSIP也可发生于儿童。起病隐匿或呈亚急性经过。主要临床表现为咳嗽气短,渐进性呼吸困难,乏力。约一半有体重减轻。10 有发热。体格检查可有呼吸增快,双下肺可闻及爆裂音,杵状指(趾)少见,约占10
有发热。体格检查可有呼吸增快,双下肺可闻及爆裂音,杵状指(趾)少见,约占10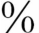 。超过2/3的患儿运动时可有低氧血症。支气管肺泡灌洗液(BALF)多见淋巴细胞增多。肺功能为限制性通气功能障碍。
。超过2/3的患儿运动时可有低氧血症。支气管肺泡灌洗液(BALF)多见淋巴细胞增多。肺功能为限制性通气功能障碍。
NISP的影像学的改变主要为广泛的磨玻璃改变和网点影,可见牵拉性支气管扩张,少数可见实变影。NISP的磨玻璃阴影主要分布于中下肺野,多对称分布。实变影常为小片实变,可对称分布。与UIP比较,NSIP以磨玻璃影为主,网点影较UIP为细小。
3.治疗 NSIP治疗上激素效果好,复发仍可以继续使用。与UIP相比,大部分NSIP患儿对糖皮质激素有较好的反应和相对较好的预后,5年内病死率为15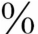 ~20
~20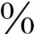 。预后取决于病变范围。
。预后取决于病变范围。
(六)隐原性机化性肺炎
1.病理特点 隐原性机化性肺炎(cryptogenic organizing pneumonia,COP)病理为闭塞性细支气管炎和机化性肺炎为主要特点的病理改变,两者在肺内均呈弥漫性分布。主要表现为终末细支气管、呼吸性细支气管、肺泡管及肺泡内均可见到疏松的结缔组织渗出物,其中可见到单核细胞、巨噬细胞、淋巴细胞及少量的嗜酸细胞、中性粒细胞、肥大细胞分布,此外尚可见到纤维母细胞浸润。在细支气管、肺泡管及肺泡内可形成肉芽组织,导致管腔阻塞,可见肺泡间隔的增厚,组织纤维化机化后,并不破坏原来的肺组织结构,因而无肺泡壁的塌陷及蜂窝状的改变。
2.诊断 COP多见于50岁以上的成年人,男女均可发病,儿童也有COP的报道,但较少见,多为感染后的BOOP。大多病史在3个月内,近期多有上感的病史。病初有流感样的症状如发热、咳嗽、乏力、周身不适和体重降低等,常可闻及吸气末的爆裂音。肺功能为限制性通气功能障碍。
COP患儿胸片最常见、最特征性的表现为游走性、斑片状肺泡浸润影,呈磨玻璃样,边缘不清。典型患儿在斑片状阴影的部位可见支气管充气征,阴影在早期多为孤立性,随着病程而呈多发性,在两肺上、中、下肺野均可见到,但以中、下肺野多见。肺CT可见胸膜下或支气管周围的斑片状阴影,其大小一般不超过小叶范围。还可见结节影。同时具有含气腔的实变、结节影和外周的分布为COP的肺CT特点。BALF见淋巴细胞的比例升高。
3.治疗 COP对激素治疗反应好,预后较好。
(七)淋巴间质性肺炎
淋巴间质性肺炎(lymphoid interstitial pneumonia,LIP)称淋巴细胞间质性肺炎。特发性淋巴间质性肺炎很少见。
1.病理特点 肉眼上间质内肺静脉和细支气管周围有大小不等黄棕色的结节,坚实如橡皮。结节有融合趋势。镜下:肺叶间隔、肺泡壁、支气管、细支气管和血管周围可见块状混合性细胞浸润,以成熟淋巴细胞为主,有时可见生发中心,未见核分裂,此外还有浆细胞、组织细胞和单核细胞等。浆细胞为多克隆,可有B细胞和T细胞,但是以一种为优势。
2.诊断 平均年龄为50~60岁,在婴儿和老人也可见到。在儿童,多与HIV、EBV感染有关。LIP的临床表现为非特异性,包括咳嗽和进行性的呼吸困难。肺外表现为体重减轻、乏力。发热、胸痛和咯血少见。从就诊到确诊往往需要1年左右的时间。肺部听诊可闻及肺底湿啰音,杵状指(趾),肺外淋巴结肿大、脾大少见。
异常丙种球蛋白血症较常见,其发生率可达80 。通常包括多克隆的高丙种球蛋白病。单克隆的高丙种球蛋白病和低丙球血症少见但也有描述。肺功能示限制性的肺功能障碍。一氧化碳弥散能力下降,氧分压下降。
。通常包括多克隆的高丙种球蛋白病。单克隆的高丙种球蛋白病和低丙球血症少见但也有描述。肺功能示限制性的肺功能障碍。一氧化碳弥散能力下降,氧分压下降。
淋巴间质性肺炎的影像学表现为网状结节状的渗出,边缘不清的小结。有时可见片状实变及大的多发结节。在小儿,可见双侧间质或网点状的渗出,通常有纵隔增宽和肺门增大。蜂窝肺在1/3成人病例中出现。胸腔渗出不常见。肺CT多示2~4mm结节或磨玻璃样阴影。病情发展可有支气管扩张、囊泡影。
3.治疗 目前尚无特效的疗法,主要为糖皮质激素治疗,有时可用细胞毒性药物。激素治疗有的病例症状改善,有的病例肺部浸润进步,不久后又恶化。用环磷酰胺和长春新碱等抗肿瘤治疗,效果不确实。
4.预后 33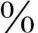 ~50
~50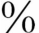 在诊断的5年内死亡,大约5
在诊断的5年内死亡,大约5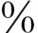 LIP转化为淋巴瘤。
LIP转化为淋巴瘤。
