10.2.4 理想气体的状态方程
2026年01月14日
10.2.4
理想气体的状态方程
一定质量理想气体的平衡状态可以用压强p、体积V、温度T三个状态参量来描述,然而这三个状态参量之间不是相互独立的,它们之间存在着一定的关系。在平衡态下,系统的状态参量p、V、T之间存在的关系称为系统的状态方程,状态方程可表示为f(p,V,T)=0,其具体形式通常由实验来确定。一定质量的化学纯理想气体的状态方程可表示为其中:p、V、T分别为气体的压强、体积和热力学温度;m和M分别为气体的质量和摩尔质量;R为普适气体常量,其值为R=8.31 J·mol-1·K-1。(https://www.daowen.com)
![]()
由状态方程可以看出,气体的状态参量只有两个是独立的,因此只需用任意两个状态便可确定系统的平衡状态:
p=p(V,T), V=V(T,p), T=(p,V)
例如,以p为纵轴,V为横轴的p-V图上的每一点给出一组确定的p、V值,因此p-V图上的每一点都表示一个平衡态。同理,也可作出T-V图等。这些图中的每一点也都表示一个平衡态。图10.2是常见的p-V图。
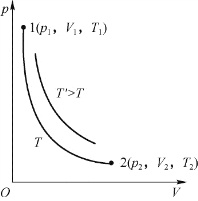
图10.2 理想气体的等温线
设系统的总分子数为N,摩尔分子数为N A,每个分子的质量为m s,则气体的总质量和摩尔质量可表示为
m=Nm s, M=N A m s
将这个关系式代入理想气体状态方程式(10.6),可得
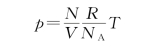
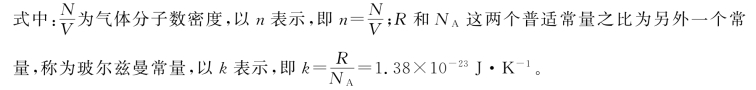
这样,理想气体状态方程的另一种形式为
![]()
式(10.7)表明,理想气体的压强与分子数密度和温度成正比。
