肠外营养途径选择
在实施肠外营养支持的过程中,正确的静脉输注途径的选择是肠外营养支持能得以顺利实施的前提。临床上肠外营养的静脉输注途径主要有中心静脉和周围静脉,在选择何种途径时应考虑以下因素:①肠外营养混合液的渗透压。②肠外营养支持输注的持续时间。③穿刺部位血管的解剖条件。④穿刺操作者的技能。⑤患者及医护人员对导管维护、护理的技能。⑥患者的疾病及凝血功能状况。
(一)中心静脉途径
1.中心静脉途径的适应证
中心静脉管径粗、血流速度快、血流量大,对渗透压的耐受性好,输入的液体可很快被稀释而不致刺激血管壁,不易产生静脉炎和静脉血栓形成。中心静脉对输注液体的浓度和酸碱度的限制小,能在单位时间内快速输入机体所需的大量液体,并可在24 h内进行持续不断地输注,因此,能最大限度地按机体的需要以较大幅度调整输入液体的量、浓度及速率,保证供给机体所需的热能和各种营养素。中心静脉穿刺置管后可供长期输液用,免遭反复静脉穿刺带来的痛苦。经中心静脉输液患者的四肢可随意活动,翻身和做护理工作也较方便,有利于防止肺部感染和压疮的发生。此外,通过留置中心静脉的双腔或三腔导管,还可供随时采取血标本,同时推注、输注其他药物,对危重患者可监测其中心静脉压以帮助了解心血管功能和全身血容量的情况,指导输液量和输液速度的调整。因此,对需较长时间肠外营养支持者或因有较多额外丢失、处于显著高代谢状态以致机体对营养物质的需求量大为增加者则宜采用中心静脉途径输液。
周围静脉输注具有应用方便、安全性高、并发症少而轻等优点,一般适用于预期只需短期(不超过2周)肠外营养支持的患者或接受部分肠外营养支持(输注营养素的量较少)的患者。
中心静脉系指上腔静脉和下腔静脉。上腔静脉和下腔静脉均可置管输液,但后者的管径比前者细,血流量少,易发生静脉炎和静脉血栓形成。而且下腔静脉置管时导管多经高位大隐静脉或股静脉插入,因导管的静脉入口邻近大腿根部,易受污染,成为病原微生物入侵通道而引起败血症。同时,因输液管道需固定于大腿,使患者活动严重受限,护理也不方便。因此,一般都尽量不采用下腔静脉置管输液的方法。在婴儿或上腔静脉置管失败,无法行上腔静脉置管时,可选择下腔静脉置管。目前临床上常用的中心静脉置管途径有:①经皮穿刺颈内静脉置管。②经锁骨下区穿刺锁骨下静脉置管。③经锁骨上区穿刺锁骨下静脉置管。④经皮穿刺颈外静脉置管或切开颈外静脉置管。⑤经头静脉或贵要静脉插入中心静脉导管(PICC)。临床上常用的中心静脉置管途径如图5-1所示。
2.中心静脉导管选择
制造静脉导管的材料有聚氯乙烯、聚乙烯、聚丙烯、聚氨酯、硅橡胶及凡纶等。理想的导管材料应具备以下条件:①优越的抗血栓性能。②质地柔软。③组织反应小。④长期应用不会变质。⑤价廉等。前三种导管经长期使用后易变僵硬,故仅适宜短期使用。后三种导管质柔软、组织反应小,内外面更光洁、管壁薄,是较理想的符合临床需求的优质导管。目前,国内、外许多厂家生产、发展了多种高质量、多功能的单腔和多腔静脉导管(图5-2)。一些新型的中心静脉导管有缓释抗生素涂层,可减少导管表面细菌定植,减少导管相关的血行感染(catheter related blood stream infections,CRBSI)。还有一种性能优良,使用方便的皮下埋藏式植入的输液港(port-cath),导管一端留置在静脉内,另一端连接一个圆形容器(药物注射盒),整个装置可长期埋藏在皮下,当需要注射药物和静脉输注时,只需经皮在药盒圆形平台上穿刺入药盒中即可(图5-3)。该装置可放置数月至数年,护理方便,一些研究者提出植入的输液港感染率低,不影响日常活动,适合于长期家庭肠外营养患者。
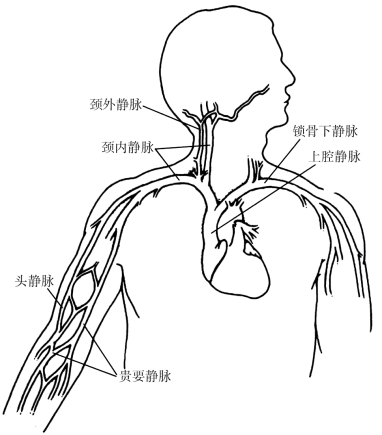
图5-1 临床上常用的中心静脉置管途径
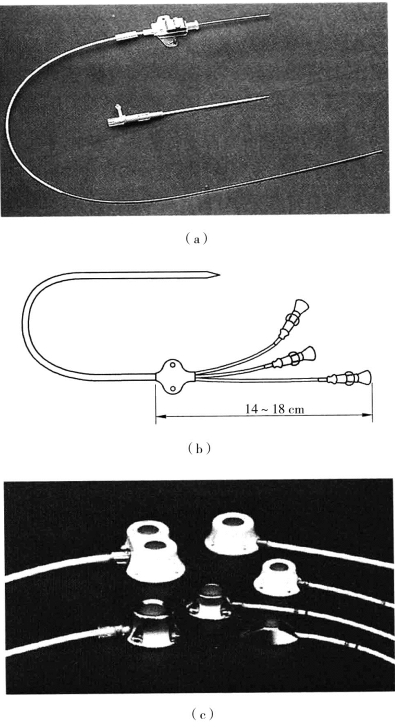
图5-2 单腔和多腔中心静脉导管
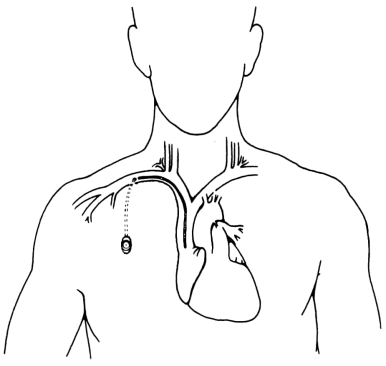
图5-3 埋藏式药物注射盒及放置示意图
3.中心静脉置管方法
(1)经锁骨下区锁骨下静脉穿刺置管:该方法临床上应用广泛,其优点为:①穿刺部位在锁骨下方胸壁,该处较平坦,便于准备术野皮肤和穿刺、置管的操作。②留置导管易于固定,也不影响患者颈部和上肢活动。③穿刺处的敷料不跨越关节,便于置管后的护理。
具体操作步骤:患者仰卧,最好取头低足高位,使静脉充盈、静脉内压升高,因而在插管时不易发生气栓。在两肩胛骨之间沿胸椎垫放一小长枕,使锁骨下静脉与肺尖分开。头转向对侧。穿刺点常选在锁骨中点下方距锁骨下缘12 cm处。整个穿刺过程严格遵循无菌操作规程,有条件者最好在手术室中进行。穿刺局部皮肤需先剃毛、去脂,然后严格消毒,铺盖无菌巾。在局部浸润麻醉后先以细针作试探性穿刺,进针方向为指向锁骨内侧头上缘,与胸壁成角为15°~30°,进针时注射器内保持轻度负压,一般进针35 cm左右常可进入静脉,进针深度与患者体型及穿刺点与锁骨下缘间的相对位置有关。随即换置管用的穿刺针按原路缓慢进针,一旦进入静脉即可抽得大量回血,再轻稳地进针12 mm,使整个针尖斜面位于静脉腔内,再次抽回血以确定针尖位置。嘱患者吸气后屏息,以一手固定穿刺针后迅速取下注射器,用手指按压针尾插孔以免发生气栓,再将导管(或导引钢丝)从插孔送入,使管顶端达到上腔静脉(在成人,从穿刺入口至到达上腔静脉内的导管长度约16 cm)。退出穿刺针,抽吸与导管联结的注射器,如回血通畅,表明管端在静脉内,即可卸下注射器和穿刺针,将导管与输液管联结。用皮肤缝线和胶布固定导管,穿刺口覆盖无菌敷料。经锁骨下区锁骨下静脉穿刺置管具体操作步骤如(图5-4)所示。
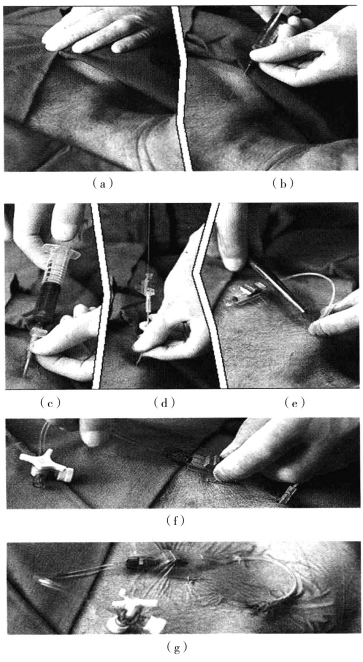
图5-4 经锁骨下区锁骨下静脉穿刺操作步骤
(2)经锁骨上区锁骨下静脉穿刺置管:采用该方法应首选右侧穿刺置管,左侧穿刺有可能损伤胸导管。患者体位和穿刺区的皮肤准备同经锁骨下区穿刺,术者位于患者头部的一侧。患者的头要尽量转向对侧并挺露锁骨上窝。穿刺点选在胸锁乳突肌胸骨头外侧缘与锁骨上缘所构成夹角的平分线上,距角顶约1.5 cm。穿刺方向为指向胸锁关节下缘,与水平面呈30°角,和矢状面呈45°角。在成人刺入2.5~3.5 cm即能进入锁骨下静脉,比经锁骨下途径的距离短。经锁骨上区锁骨下静脉穿刺置管示意图如图5-5所示。
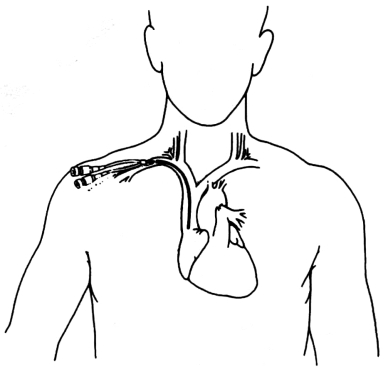
图5-5 经锁骨上区锁骨下静脉穿刺置管示意图
由于导管从锁骨上窝引出体外,该处伤口敷料难以与局部皮肤紧密接触,并易蓄积汗液等分泌物。为克服此弊端,常由穿刺点越过锁骨向前胸壁做一皮下隧道,使导管通过皮下隧道从前胸壁引出,并在该处固定于皮肤。做皮下隧道、引出导管的方法随置管类型而异,一般均先沿选定的隧道部位做局部浸润麻醉,切开原先做静脉穿刺的进皮点皮肤。然而用一只粗针从隧道远端的皮肤刺入,并在皮下推进,最后针尖从原静脉穿刺处已扩大的皮肤伤口穿出。将导管(或导引钢丝)末端从针尖孔插入针腔内,退出粗针,导管(或导引钢丝)即经皮下隧道引出体外(导管套在导引钢丝外插入静脉,当管端达上腔静脉后抽出导引钢丝)。缝合切开的皮肤伤口以完全埋藏导管于皮下。用皮肤缝线固定导管,伤口覆盖无菌敷料(图5-6)。
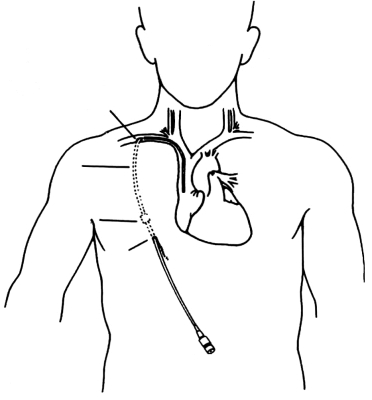
图5-6 皮下隧道置管示意图
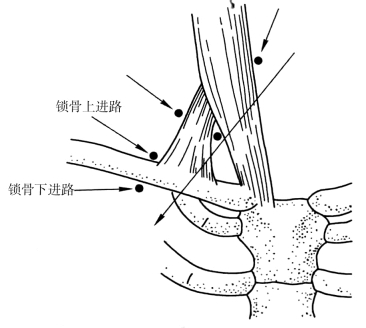
(3)颈内静脉穿刺置管:患者体位穿刺区的皮肤准备及操作步骤同锁骨下静脉穿刺置管,穿刺点可选择下列3个部位(图5-7)。①高位穿刺点:患者头尽量后仰并转向对侧。穿刺点在大约相当于甲状软骨上缘水平的胸锁乳突肌前缘稍内侧,可用左手中示指触摸颈总动脉搏动外0.5~1.0 cm,为进针点,针杆与水平面呈30°~40°角,针尖指向锁骨中、内1/3交界处。当抽得回血后即插管至上腔静脉水平。此法成功率较高、并发症发生率低,但由于插管部位高,导管和敷料均不易固定,导管难以长期保留。②低位前路穿刺点:在胸锁乳突肌下段胸骨头和锁骨头内侧缘所构成夹角的平分线上,距角顶约1 cm,针杆与水平面约成30°角,针尖指向同侧乳头、胸锁乳头肌锁骨头内侧缘的深面,一般进针23 cm即可刺入静脉。③低位后路穿刺点:在胸锁乳头肌外侧缘的中、下1/3交点或锁骨上5 cm左右(颈外静脉与胸锁乳头肌后缘交界处),针保持接近呈水平位,在胸锁乳突肌深面、向胸骨柄上窝方向缓慢推进。一般进针2.5~3.5 cm可刺入静脉。
 (https://www.daowen.com)
(https://www.daowen.com)
图5-7 颈内静脉穿刺置管穿刺点
(4)颈外静脉置管:颈外静脉与颈内静脉汇合后进入锁骨下静脉,汇合部形成一向外的锐角,常造成插管困难(尤其在左侧)。置管时患者仰卧,头低足高位,肩背部垫高,头转向对侧,术野皮肤清洁后按常规消毒、铺无菌巾。如颈外静脉充盈明显,可在直视下穿刺静脉后插管。如颈外静脉不清楚,则需做切开插管。皮肤切口可选择在锁骨上缘上方约35 cm。切开皮肤、皮下组织及颈阔肌后显露颈外静脉,用弯血管钳游离静脉约15 cm。在已游离的静脉后面绕过两根丝线。以远侧丝线绳索扎静脉,牵引结扎线使静脉紧张。斜行剪开静脉一小口,插入导管,导管位置安放妥当后结扎近侧丝线以固定导管。缝合皮肤切口,皮肤缝线在结扎后再用于固定导管。
(5)经周围静脉插入中心静脉导管(PICC):经外周静脉置入中心静脉导管是指通过肘部静脉将导管置入上腔静脉。最常选用的静脉是肘部头静脉、贵要静脉或正中静脉。PICC的优点主要是可以避免多数中心静脉导管的并发症,可以较长时间留置和较少的感染发生。具体操作步骤如下:患者仰卧,两肩胛骨间区垫一长薄枕,头转向对侧,上臂外展90°。先测量置入导管的长度(由穿刺点到右侧锁骨头距离再垂直向下到胸骨右侧缘第3肋间隙的长度),严格遵循无菌原则消毒前臂中段到上臂中段,上臂上止血带。选择贵要静脉或肘正中静脉作为穿刺点,在局部浸润麻醉后先用外引套管做穿刺,抽到回血后拔出针芯,插入选择好的导管并插至预定长度,如遇阻力可外展上臂以改变头静脉进入锁骨下静脉的角度,拨出引导套管,掰开并去掉引导套管,拨出金属导丝。用含肝素的生理盐水冲洗导管,观察导管是否通畅,用固定翼或胶布固定导管(图5-8)。
PICC在临床上应用越来越广泛,如外周静脉条件很差的患者、需连续应用抗生素2周以上患者、输入高渗性溶液、输入刺激性强的化疗药物或毒性药物及长期卧床形成深静脉血栓患者等。如何提高穿刺置管成功率是临床面临的一个新的课题。在使用超声做引导工具以前,经外周静脉穿刺中心静脉置管成功率主要取决于操作者的经验及患者的血管状况。穿刺前的精确定位是手术成功的关键。超声显像具有实时、动态的特点,可在穿刺前对血管做初步选择、评估,确定最佳穿刺部位。操作者可以在超声引导下准确地将穿刺针送入血管腔,大大提高了操作者一次穿刺置管的成功率。
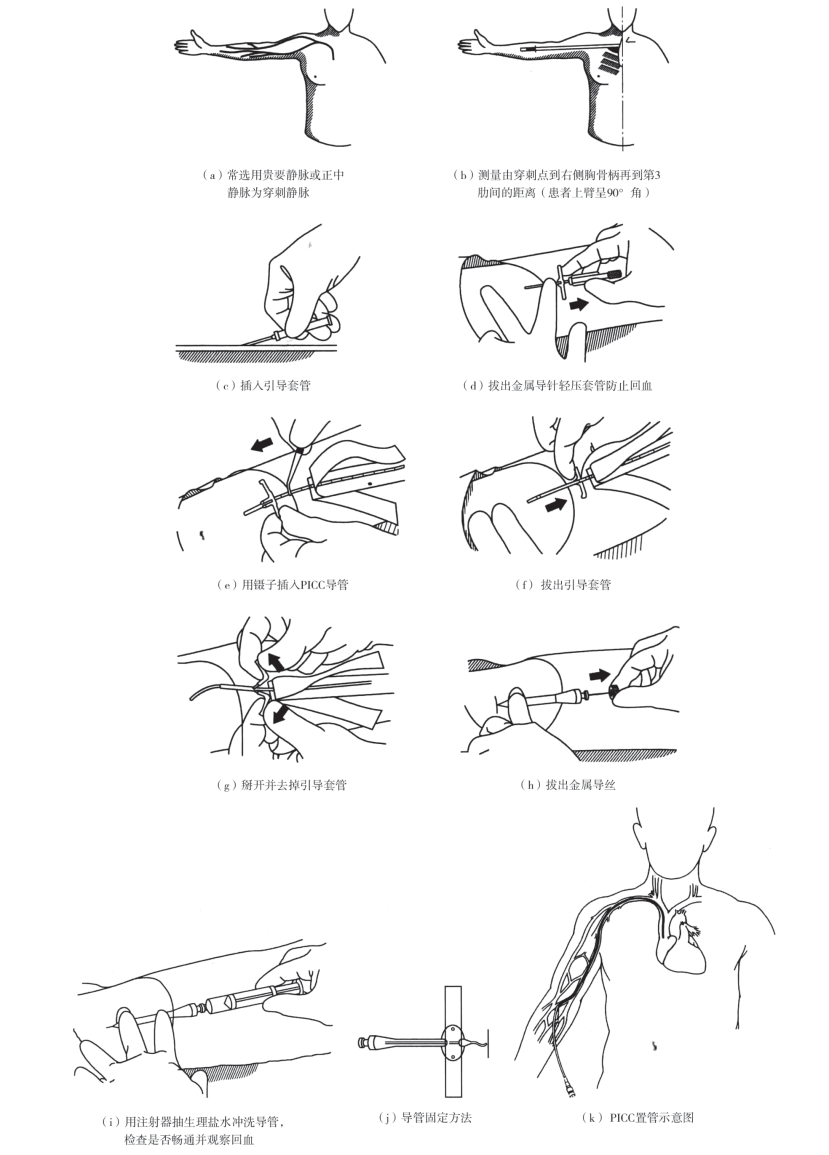
图5-8 PICC置管操作步骤及示意图
PICC可选择的途径很多,如锁骨下静脉、颈内静脉、贵要静脉等。通常情况下,应首选贵要静脉做血管穿刺,因贵要静脉位于肘前,操作范围较大。贵要静脉入路可能是中心静脉置管创伤最小、并发症最少的方法,可以明显降低气胸、血胸、空气栓塞及神经损伤等并发症的概率。超声设备引入PICC置管是PICC发展史上的一个划时代的事件,在超声直视下,能够清晰地看见预置部位周围的静脉、动脉、神经,这不仅有利于选择合适的血管进行穿刺,而且极大地避免了盲插时出现的误伤动脉、神经等。高频彩色多普勒超声的出现使中心静脉置管取得突破性进展,在超声引导监测下,操作者可以顺利完成穿刺、置管等操作。
(6)超声引导经中心静脉置管:目前,临床上对行中心静脉置管患者的血管选择方法有肉眼观察解剖标志定位法和超声引导法。凭解剖标志定位法进行经验性盲穿置管,对患者局部血管条件及操作者经验要求高,否则穿刺成功率较低且并发症多。当遇到解剖异常、肥胖、颈短、有过穿刺并发症的患者或在困难体位下穿刺时,用解剖标志定位法做颈内静脉穿刺十分困难,操作风险大。失败率和并发症发病率相当高,影响患者的治疗和康复,并加重经济负担,严重的甚至死亡。
超声具有无损伤、易操作的优点,20世纪80年代起逐渐用于辅助引导中心静脉置管,彩色多普勒超声成像,直观显示血管壁、管腔及周围的解剖结构,可以直接观察血流情况。利用超声引导技术穿刺颈内静脉在近乎直视下操作,它改变以往盲探、盲穿的方式,在其引导下的颈内中心静脉插管可提高首次穿刺成功率、减少操作时间提高工作效率,降低气胸、神经损伤、误穿动脉等并发症的发生率,保证了医疗安全。大量的临床对照研究结果显示,超声引导能够降低中心静脉置管中并发症的发生率,提高穿刺的成功率。
(图5-9)是超声引导经中心静脉置管示意图。
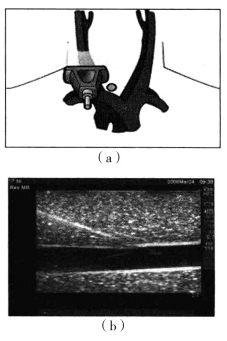
图5-9 超声引导经中心静脉置管示意图
(二)周围静脉途径
周围静脉是指浅表静脉,大多数是上肢末梢静脉。下肢周围静脉,尤其是在成人,不适合用作肠外营养,因为发生血栓性静脉炎的危险性较高,且患者需要卧床休息,活动严重受限,护理也不方便。
1.周围静脉途径适应证
周围静脉营养(peripheral parenteral nutrition,PPN)是指通过周围静脉途径输注营养液,是除中心静脉以外的另一种肠外营养方式,PPN具有应用方便、安全性高、可避免中心静脉导管相关并发症等优势,临床应用日趋广泛,已成为临床肠外营养支持的主要途径。近年来,PPN的概念日益被人们所接受,在许多发达国家已经作为短期肠外营养支持的首选途径。PPN的优点有:①静脉途径易建立,无须经特殊培训的人员操作。②避免与中心静脉导管插管相关的并发症的发生。③便于临床观察,可早期发现插管处静脉炎征象并及时处理。④减少中心静脉置管引起的并发症及风险。⑤操作简便,便于在缺乏经验的基层单位中普及。
PPN的适应证有:①短期(<14 d)肠外营养者,可避免中心静脉置管所致的危险性。②当中心静脉置管禁忌或不能进行时。③中心静脉导管感染或败血症时,拔除留置的导管数日以防止中心静脉导管细菌定殖,但又不能停止肠外营养支持者,此时应采用周围静脉途径。
PPN的禁忌证有:①需要长期肠外营养支持或已经放置中心静脉导管者。②能量及营养底物需求量高(如高分解代谢状态、高流量肠瘘等),超过了周围静脉营养所能供给的确能力。③周围静脉局部条件差,无法建立静脉通路者。④肠外营养液渗透压过高(如需要限制液体量患者),超过周围静脉耐受能力者。
2.周围静脉及静脉导管的选择
PPN时的周围静脉大多数选择上肢的末梢静脉,如前臂近端或肘前窝的周围静脉。下肢周围静脉由于容易发生血栓性静脉炎,而且不利于患者活动,因而不适合用作肠外营养。无论选择何处静脉,为减少血栓性静脉炎的发生,应尽量选择直径较粗的静脉。
PPN时为使患者免受频繁穿刺静脉的痛苦和减少穿刺针机械刺激所致的静脉炎和静脉血栓形成,可应用塑料套式静脉留置套管针。具体操作如下:首先选择显露良好的周围静脉,较理想的是前臂静脉,用止血带扎住穿刺点近端,穿刺部位备皮、去脂、消毒,套管穿刺静脉成功后解开止血带,将外套管推入静脉内,把内芯拔出,保留在静脉内的塑料套管与输液装置连接,套管出处用无菌纱布或特殊薄膜覆盖(图5-10)。目前,临床上有多种静脉留置式套管针使用,如预计通过同一输液导管输注时间超过24 h,最好选用尖端较细、材质为聚亚氨酯或硅胶的导管,同时尽量选择直径较粗的静脉,这样对静脉内壁的机械性损伤较小,并有利于血液及时稀释输入的营养液。穿刺置管时,静脉导管尖端与皮肤穿刺点应保持一段距离,以减少细菌定植的机会。有研究发现,导管的尖端越细,越有利于血流及时稀释输入的营养液。导管的尖端距离皮肤进针口越远,细菌定植的机会越小。
由此可见,在实施PPN时应尽量选择直径较粗的静脉,输液的静脉留置导管应较细,以避免对血管内壁的机械性刺激,并有利于血液及时稀释输入的营养液,静脉导管尖端与皮肤穿刺点应保持一段距离,以减少细菌定植的机会。
3.周围静脉营养组分及输注
周围静脉营养支持能否耐受,除了与所选择静脉的通畅程度、导管材料与导管内径外,还与营养液的渗透压、pH和输注速度有关。一般来说,血流通畅的周围静脉能够耐受<900 mOsm/L渗透压的营养液10~14 d,高渗溶液会刺激静脉、引起疼痛、静脉炎和血栓形成。添加脂肪乳剂和增加容量可降低渗透压。此外,脂肪乳剂还有保护血管内皮的作用。因此,周围静脉营养支持时,应当含有相当量的脂肪乳剂作为能量物质,或采用适合周围静脉的营养制剂。此外,采用全合一方式配制营养液和提倡低热量营养支持均有利于PPN的实施。
周围静脉营养支持输注方式有交替式输注和持续性输注两种,前者为每日在输注完毕后拔除静脉穿刺针,次日在对侧前臂重新穿刺。后者留置到治疗结束或出现静脉炎征象时,才拔除留置的静脉导管。短时间(12~24 h)中断输液时可用封闭塞或肝素帽(又称为注射塞)密封塑料套管尾端,但需使套管腔内充满肝素液(1 mg肝素/1 mL等渗盐水)。取下封闭塞后可继续输液。如需长时间(如24 h以上)中断输液,可将实心的针芯插入套管腔内。针芯的直径与塑料套管内径相适应,其顶端比套管前端的锥形口长1 mm,两者紧密接触,可防止套管内凝血。拔除针芯后又可继续输液。由于目前使用的导管质地较柔软,内、外壁表面十分光滑,材料本身与组织的生物相容性好,留置在静脉内对血管壁刺激性小,也不会因患者肢体活动而损伤血管,静脉血栓形成的可能性小。一般来说,材质良好的静脉留置式套管针可留置2~3 d,较少发生血栓性静脉炎。
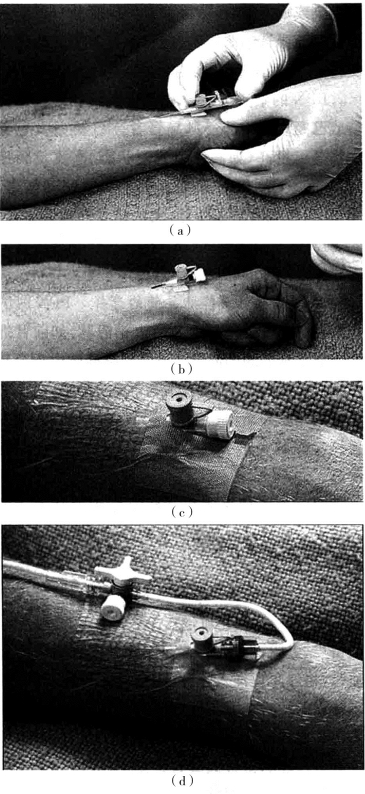
图5-10 周围静脉穿刺、留置操作示意图
