五、心输出量监测
心输出量是反映心脏泵功能的重要指标。可判断心力衰竭和低排综合征,评估患者预后。根据Startling曲线,临床上能指导输血、补液和应用心血管药物治疗。
(一)监测方法
1. 有创心输出量监测方法
(1)Fick法:Fick于1870年首先提出,由于肺循环与体循环的血流量相等,故测定单位时间内流经肺循环的血量可确定心输出量。某种物质注入流动液体后的分布等于流速乘以物质近端与远端的浓度差。直接Fick法是用氧耗量和动、静脉氧含量差来计算CO的,具体公式为:
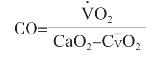
其中V˙O2为氧耗量,CO2为混合静脉血氧含量,CaO2为动脉血氧含量。直接Fick法测定CO需要用设备测定氧耗量,同时通过肺动脉导管采集混合静脉血测定CO2,采集动脉血测定CaO2。
直接Fick法被认为是CO监测的金标准。在实际应用中,直接Fick法也有一定的误差。如导管尖端的位置不当,或者是左向右分流时肺动脉采血的氧含量不能完全代替实际的混合静脉血氧含量。机体正常情况下有一部分静脉血流绕过肺泡经支气管静脉和心内最小静脉直接流入左心室,进入体循环(即右向左分流)。这部分血流占CO的20%。故肺循环血量不能完全代替体循环血量。研究表明,采用这种方法测出的CO,平均误差范围为2.6%~8.5%。
(2)温度稀释法:利用肺动脉导管,通过测定注射冷0.9%氯化钠溶液导致的温差及传导时间计算CO的方法为温度稀释法,是常用的有创心血管功能监测方法。
①温度稀释法:利用Swan-Ganz导管施行温度稀释法测量心输出量,是进行创伤性心血管功能监测的方法,结果准确可靠,操作简便,并发症少。适用于心血管和急诊危重患者。测量时,将2~10℃冷0.9%氯化钠溶液作为指示剂,经Swan-Ganz导管置入右心房,随血流进入肺动脉,由温度探头和导管前端热敏电阻分别测出指示剂在右心房和肺动脉的温差及传导时间,经心输出量计算机描记时间温度曲线的面积,自动计算心输出量,并显示和记录其数字及波形。注射应尽可能快速和均匀,理想速度为10mL/4~5s(2mL/s)。连续注射和测量3次,取平均值。
②连续温度稀释法:采用物理加温作为指示剂来测定心输出量,可以连续监测CO。连续温度稀释法采用与Swan-Ganz导管相似的导管(CCOmbo),导管置于肺动脉内,在心房及心室这一段(10cm)有一加温系统,可使周围血液温度升高,然后由热敏电阻测定血液温度变化,加热是间断进行的,每30秒一次,故可获得温度-时间曲线来测定心输出量。开机后3~5分钟即可报出心输出量,以后每30秒报出以前所采集的3~6分钟的平均数据,连续监测。该仪器不需定标,加温系统是反馈自控的,温度恒定,导管加温部位表面温度为44℃,功率为7.5W,仅有一薄层血液与之接触,至热敏电阻处血液温度仅高于体温0.05℃(这种微小温差用常规热敏电阻是无法测出的)。血液和心内膜长时间暴露在44℃未发现有任何问题。目前导管增加了混合静脉血氧饱和度(SO2)测定。
(3)脉搏轮廓分析连续心输出量测定(PiCCO):采用成熟的温度稀释法测量单次心输出量,并通过分析动脉压力波型曲线下面积与CO存在的相关关系,获取连续CO。PiCCO技术从中心静脉导管注射室温水或冰水,在大动脉(通常是主动脉)内测量温度-时间变化曲线,因而可测量全心的相关参数;更为重要的是其所测量的全心舒张末期容积(GEDV)、胸腔内血容积(ITBV)能更充分反映心脏前负荷的变化,弥补了以往以中心静脉压(CVP)、肺动脉阻塞压(PAOP)等压力代容积的缺陷。根据温度稀释法可受肺间质液体量(即血管外肺水,EVLW)影响的特点(染料稀释法则无此特点),目前应用单指示剂(热稀释)法还可测量EVLW,即EVLW=胸腔总热容积(ITTV)-ITBV。
PiCCO技术测量参数包括:AP、SVR、GEDV、ITBV、不间断容量反应(SVV,PPV)、全心射血分数(GEF)、心功能指数(CFI)、EVLW、肺血管通透性指数(PVPI)。PiCCO技术还有以下优点:①损伤小,只需建立一中心静脉导管和动脉通路,不需要使用右心导管,更适合儿科患者;②各类参数更直观,不需要加以推测解释(如右心导管测量的PCWP等);③可实时测量CO,使治疗更及时;④导管放置过程简便,不需要行胸部X线定位,容易确定血管容积基线,避免了仅凭X线胸片判断是否存在肺水肿引起的争议;⑤使用简便,结果受人为因素干扰少;导管留置可达10天,有备用电池,便于患者转运。PiCCO技术禁用于股动脉移植和穿刺部位严重烧伤的患者。对存在心内分流、主动脉瘤、主动脉狭窄者及肺叶切除和体外循环等手术易出现测量偏差。当中心静脉导管置入股静脉时,测量CO偏差高过75mL/min,应予以注意。
2. 无创或微创心输出量监测法
(1)生物阻抗法心输出量监测(thoracic electrical bioimpedance,TEB)。TEB是利用心动周期中胸部电阻抗的变化来测定左心室收缩时间并通过计算获得心搏量。TEB操作简单,费用低,并能动态连续观察CO的变化趋势。但其抗干扰能力差,尤其是不能鉴别异常结果是由患者的病情变化引起的还是由仪器本身的因素所致,计算CO时忽略了肺水和外周阻力的变化,因此,在危重病和脓毒症患者与有创监测时CO相关性较差,在一定程度上限制了其在临床上的广泛使用。心阻抗血流图是利用心动周期于胸部电抗阻的变化来测定左心室收缩时间和计算出每搏量,然后再演算出一系列心功能参数。1986年,Sramek改良了Kubicek公式,应用8只电极分别安置在颈根部和剑突水平,根据生物电阻抗原理,测量胸部电阻抗变化,通过微处理机自动计算CO。(https://www.daowen.com)
(2)食管超声心动图(TEE)。TEE监测参数包括:①每搏量(SV)=舒张末期容量(EDV)-收缩末期容量(ESV)。②左室周径向心缩短速率(VCF),正常值为每秒0.92±0.15周径。③左室射血分数(EF)。④舒张末期面积(EDA),估计心脏前负荷。⑤根据局部心室壁运动异常,包括不协调运动、收缩无力、无收缩、收缩异常及室壁瘤,监测心肌缺血。TEE监测心肌缺血较ECG和肺动脉压敏感,变化出现较早。
(3)动脉脉搏波形法连续心输出量监测:通过外周动脉置管监测患者动脉波形,并根据患者的年龄、性别、身高及体重等信息计算得出每搏量(SV)。通过SV×心率得出心输出量。以FloTrac为例,SV与动脉压的标准差成正比,血管顺应性和血管阻力对SV的影响合成一个变量χ(搏动性,pulsatility),即SV=动脉压力标准差(SDAP)×搏动性。动脉压以100Hz的频率来取样,其标准差每20秒更新一次。χ通过主动脉顺应性、平均动脉压、压力波形的偏度和峰度及体表面积各参数的多元回归方程推算,不需要定标。血管张力是决定每搏输出量与动脉压力之间关系的主要因素。
用动脉脉搏波形分析法测定心输出量时,还可以显示每搏量变异性(SVV),而SVV通过(SVmax-SVmin)/SVmean计算;每搏量变异性(SVV)的分析,如机械通气时,有助于对患者进行目标导向的液体治疗。主动脉阻抗的个体差异可能导致心输出量计算的不准确性。动脉压力波形的假象或变更,如动脉瓣膜疾病、运用主动脉球囊反搏装置或体循环血管阻力大量减小,都可能影响心输出量测定的准确性。
(4)部分CO2重复吸入法心输出量监测:该技术采用的是转换的Fick公式,其以CO2消耗量为参数,而不是氧摄取量。
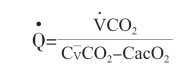
该方法通过计算机控制的气动阀门,每3分钟间歇性关闭50秒,导致部分呼出气体被重复吸入。将重复吸入引起的CO2生成量和呼气末CO2量(近似于混合静脉血CO2量)的变化代入上述方程,可计算出心输出量。
初期的临床研究表明该方法与温度稀释法有较好的一致性,但该方法仅限于机械通气且无明显肺内分流的患者,临床应用有较大局限性。
(二)临床意义
1. 血流动力学指标计算法
见表2-6。
表2-6 血流动力学指标正常值
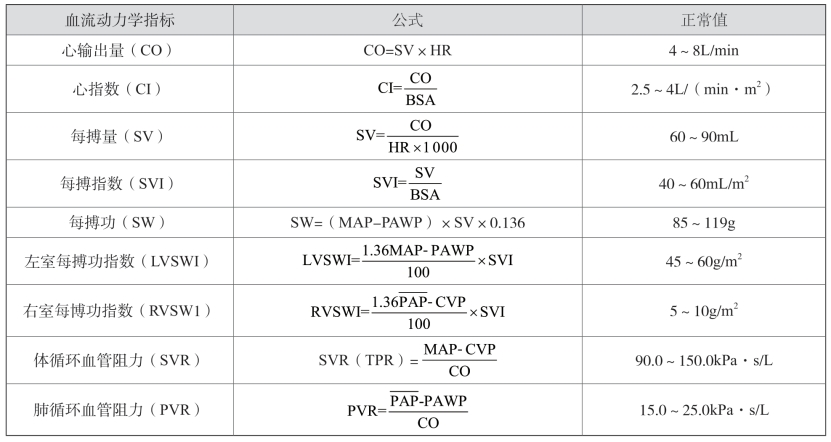
2. 判断心脏功能
①诊断心力衰竭和低心输出量综合征,估计病情预后。②绘制心功能曲线,分析CI和PAWP的关系,指导输血、补液和心血管治疗。
