静脉麻醉维持期间给药速率和计算方法
理论上静脉麻醉维持给药速率应等于药物从体内清除的总清除率(Cls)乘以血浆浓度。为了维持一个稳定的靶浓度(CT),给药速率应与药物从体内排除的速率相等:
静脉麻醉维持的给药速率=CT×Cls
此计算公式概念浅显易懂,但它不适用于多室模型的静脉麻醉药长时间持续输注时的药代动力学特征。药物的吸收和消除在以血液为代表的中央室,而药物的分布在一个或多个假定的周边室,消除和分布是同时进行的,且随着给药时间的延长,药物从中央室扩散到周边室的量逐渐减少,其给药量也应随之减少,即以指数衰减形式输注给药:
维持给药速率=CT×V1×(k10+k12e-k21t+k13e-k31t)
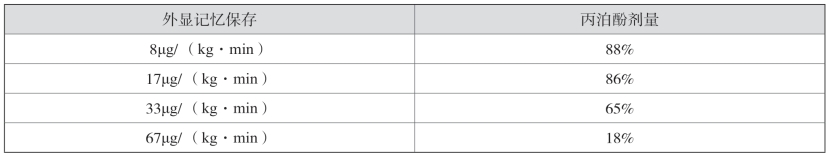
临床医师显然不会用此公式去计算给药速度。通常维持静脉麻醉的方法是参考已知的维持麻醉的给药速率,麻醉医师根据经验和观察患者的生理指标进行调节。例如,丙泊酚麻醉维持给药的速率一般为6~12mg/(kg·h)。具体到个别患者的麻醉维持,什么速率合适,需要麻醉医师来判断和决定。当然也有客观的参考标准,推荐使用的是神经电生理方法监测麻醉深度。例如,用脑电双频谱指数(BIS)监测,麻醉中调节静脉给药速率,将BIS维持在40~60。另一方面,参考来自文献的临床实验数据,例如,使群体患者意识消失的丙泊酚输注速率为6.6mg/(kg·h),也即110μg/(kg·min)。丙泊酚输注速率与患者记忆功能的关系可以参考表5-5。当丙泊酚输注速率达到67μg/(kg·min)时,80%的患者失去记忆。
表5-5 丙泊酚镇静与记忆功能
麻醉中阿片类药持续输注的问题比较特殊。适用于持续输注的阿片类药应该是速效、短效药;长时间输注停药后药物浓度能迅速下降,达到不抑制患者自主呼吸的水平。常用的阿片类药中芬太尼最不适合持续输注。从图5-2可以看出芬太尼持续输注100分钟后的半衰期(时-量相关半衰期)已超出其输注时间本身,很难控制。但是也有依据前述的维持给药速率的计算公式计算芬太尼给药模式的方法:苏芬太尼的时-量相关半衰期特点表明它比较适合用于持续输注。图5-3显示苏芬太尼持续输注3~4小时,停止输注后血药浓度下降50%的时间为25~30分钟。苏芬太尼对心血管系统几乎没有影响,在心血管手术麻醉时可以用到很大的剂量,而安全性却非常好。唯一担心的是阿片类药的呼吸抑制作用。一般手术麻醉维持,苏芬太尼的输注速率为0.25~1.0μg/(kg·h)。相当于60kg的成人,每小时输注15~60μg。特别要提醒,如果患者准备术后即刻拔出气管导管,苏芬太尼持续输注的速率必须小于1.0μg/(kg·h),而且应在手术结束前30分钟停止输注苏芬太尼。如果间断给予苏芬太尼,剂量为2.5~10.0μg。
维持给药速率=CT×V1×(k10+k12e-k21t+k13e-k31t)
苏芬太尼的药代动力学特性表明它适用于TCI方法维持麻醉。苏芬太尼TCI配合静脉麻醉药用于麻醉诱导时,防止气管内插管引起的心血管反应的半数有效血浆浓度(C50)为1.08ng/mL(0.73~2.55ng/mL)。推荐的用法是麻醉诱导时将苏芬太尼TCI血浆靶浓度设置为2.0ng/mL,待效应室浓度上升达到0.5ng/mL时,可以满足气管插管所需的深度。术中维持TCI血浆靶浓度为0.25~ 3.0ng/mL(表5-2)。文献报道,术中血浆苏芬太尼浓度低于0.5ng/mL,会导致其他补救措施增加。同理,也需要手术结束前30分钟停止输注苏芬太尼。
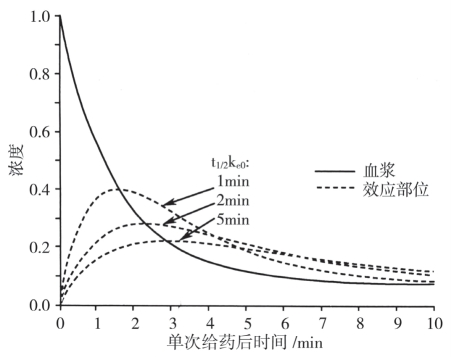
图5-2 t1/2ke0对效应室浓度的影响
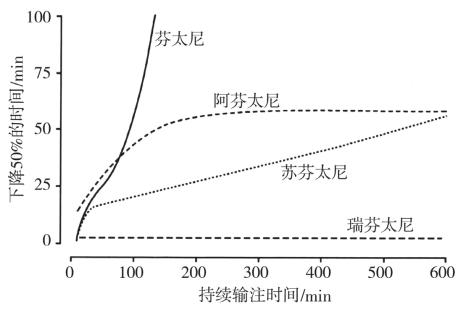
图5-3 芬太尼类药持续长时间输注后半衰期的变化(时-量相关半衰期)(https://www.daowen.com)
瑞芬太尼的速效和超短效的优越特性使其特别适合静脉麻醉维持期长时间持续输注。由于其停药后恢复时间(3~6分钟)几乎不受持续输入时间的影响,因此无论用恒速方法输注还是TCI方法输注,均能良好控制。持续输注的常用速率在0.1~1.0μg/(kg·min),剂量范围很宽,由麻醉医师根据手术刺激程度的大小和患者反应程度的强弱来调节。由于起效快,加深或减浅麻醉十分迅速,安全性也得以提高。临床麻醉维持常用的瑞芬太尼输注速率为0.2~0.4μg/(kg·min)。瑞芬太尼TCI方法给药时,术中维持血浆靶浓度为2.0~8.0ng/mL(表5-2)。
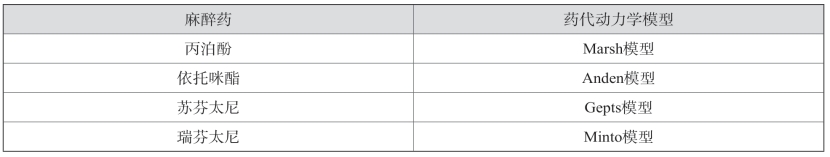
TCI是将药代动力学理论用于临床麻醉实践的典范。与持续输注方法不同,TCI自动计算出达到设置的血药浓度所需的给药速率,并使麻醉从诱导到维持成为一个连续的过程。目前临床上常用的静脉麻醉药物的TCI药代动力学模型见表5-6。
表5-6 常用的麻醉药物和药代动力学模型
TCI通常以血浆药物浓度为指标,而效应部位(室)药物浓度并不等于血浆药物浓度,常常有一个滞后现象。
ke0本应是药物从效应室转运至体外的一级速率常数。而目前通常用来表示药物从效应室转运至中央室的速率常数,即反映药物在中央室和效应室之间的平衡速度。k为一级速率常数,表示单位时间内药物的转运量与现有量之间的比值,例如k=0.1每小时,表示剩余药量中每小时有10%被转运;e表示效应室;0表示体外。效应室与中央室的滞后程度取决于ke0。药物的ke0越大,效应室与中央室平衡的时间越短。例如丙泊酚ke0为0.239每分钟,是芬太尼ke00.105每分钟的两倍,丙泊酚效应室的达峰时间仅为芬太尼的一半。
t1/2ke0是维持一个稳态血药浓度时,效应室浓度达到血浆浓度50%时所需的时间。可用0.693/ke0来计算。原则上药物的ke0越大,t1/2ke0越小,效应室平衡的时间越快(表5-7)。例如阿芬太尼ke0较大,t1/2ke0不到1分钟,达峰效应时间1.4分钟,达峰时单次剂量的阿芬太尼约60%,再分布和排出体外。而芬太尼,达峰效应时间要4分钟,达峰时80%以上的药物(单次注射)已再分布和排出体外。从图5-2可以看出,药物的t1/2ke0越小,药物效应室达到峰效应的时间越短,效应室浓度占血浆浓度的比值也越高。
TCI系统显示的血浆和效应室的靶浓度是根据药代动力学推算出来的,前提是假设患者血浆药物浓度为零,实际浓度并不知道。系统一旦中断工作,可能会有两种情况:一是操作者人为将注射泵停下来,如注射器内药液走空,需要更换,此时TCI系统会将停泵时间记录下来,并继续按药代动力学原理进行计算,一旦注射泵重新工作,可以自动调整泵速,恢复原靶浓度。二是退出系统,如发生故障;TCI重新工作时,不会考虑体内现存药量,仍将机体血浆浓度视为零,如此推算出来的靶浓度将与实际情况偏差很大。
表5-7 静脉麻醉药单次给药后t1/2ke0和效应室达到峰效应的时间
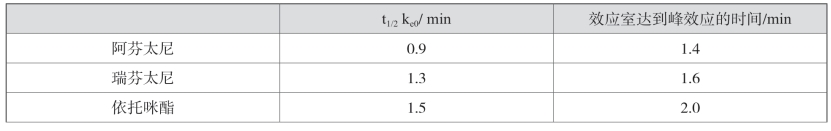
续表5-7
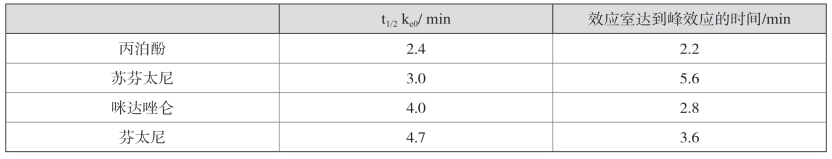
t1/2ke0是维持一个稳态血药浓度时,效应室浓度达到血浆浓度50%时所需的时间,可用0.693/ke0来计算。原则上药物的ke0越大,t1/2ke0越小,药物效应室达到峰效应的时间越短,效应室浓度占血浆浓度的比值也越高。
