药品广告的审查和发布
为加强药品广告管理,保证药品广告的真实性和合法性,《药品管理法》和《中华人民共和国药品管理法实施条例》对药品广告的管理提出了具体的要求。2018年修正的《中华人民共和国广告法》(简称《广告法》)中也有涉及药品广告的管理规定。2020年3月1日起施行的《药品、医疗器械、保健食品、特殊医学用途配方食品广告审查管理暂行办法》(简称《暂行办法》)对药品广告的申请、审查、内容要求和处罚规定进一步细化。
素质拓展
我国药品广告管理发展历史
1959年,卫生部、化工部和商业部联合发布了《关于未大批生产的药品不登宣传广告的通知》,首次对药品的广告宣传进行规定。
1982年,国务院发布了《广告管理暂行条例》,对药品广告做了专门规定。
1992年,国家原工商行政管理总局和卫生部联合发布了《药品广告管理办法》。
1995年,国家原工商行政管理总局、卫生部再次发布了《药品广告审查标准》和《药品广告审查办法》,进一步明确了药品广告的申请、审查程序和管理内容。
2000年1月1日起,我国实施处方药和非处方药分类管理制度,为加强对处方药的广告媒体和内容的管理,保证人民用药安全,2001年,原国家食品药品监督管理局先后发布了《关于国家药品监督管理局停止受理药品广告申请的通知》《关于停止在大众媒介发布小容量注射剂药品广告的通知》和《关于加强药品广告审查监督管理工作的通知》等。
2007年,原国家食品药品监督管理局和国家工商行政管理总局再次联合发布了《药品广告审查办法》和《药品广告审查发布标准》。
2018年12月21日,国家市场监督管理总局公布《市场监管总局关于修改〈药品广告审查办法〉等三部规章的决定》(国家市场监督管理总局令第4号),对《药品广告审查办法》作出修改。
2019年,国家市场监督管理总局制定出台《药品、医疗器械、保健食品、特殊医学用途配方食品广告审查管理暂行办法》,自2020年3月1日起施行。
(一)药品广告管理机构
国务院市场监督管理部门主管全国的广告监督管理工作,国务院有关部门在各自的职责范围内负责广告管理相关工作。
国家市场监督管理总局负责组织指导药品、医疗器械、保健食品和特殊医学用途配方食品广告审查工作。
各省、自治区、直辖市市场监督管理部门、药品监督管理部门负责药品、医疗器械、保健食品和特殊医学用途配方食品广告审查,依法可以委托其他行政机关具体实施广告审查。
(二)药品广告发布的内容准则
《暂行办法》中对药品广告的发布内容有如下规定:
药品广告的内容应当以国务院药品监督管理部门核准的说明书为准。药品广告涉及药品名称、药品适应证或者功能主治、药理作用等内容的,不得超出说明书范围。药品广告应当显著标明禁忌、不良反应,处方药广告还应当显著标明“本广告仅供医学药学专业人士阅读”,非处方药广告还应当显著标明非处方药标识(OTC)和“请按药品说明书或者在药师指导下购买和使用”。
医疗器械广告的内容应当以药品监督管理部门批准的注册证书或者备案凭证、注册或者备案的产品说明书内容为准。医疗器械广告涉及医疗器械名称、适用范围、作用机理或者结构及组成等内容的,不得超出注册证书或者备案凭证、注册或者备案的产品说明书范围。推荐给个人自用的医疗器械的广告,应当显著标明“请仔细阅读产品说明书或者在医务人员的指导下购买和使用”。医疗器械产品注册证书中有禁忌内容、注意事项的,广告应当显著标明“禁忌内容或者注意事项详见说明书”。
保健食品广告的内容应当以市场监督管理部门批准的注册证书或者备案凭证、注册或者备案的产品说明书内容为准,不得涉及疾病预防、治疗功能。保健食品广告涉及保健功能、产品功效成分或者标志性成分及含量、适宜人群或者食用量等内容的,不得超出注册证书或者备案凭证、注册或者备案的产品说明书范围。保健食品广告应当显著标明“保健食品不是药物,不能代替药物治疗疾病”,声明本品不能代替药物,并显著标明保健食品标志、适宜人群和不适宜人群。
特殊医学用途配方食品广告的内容应当以国家市场监督管理总局批准的注册证书和产品标签、说明书为准。特殊医学用途配方食品广告涉及产品名称、配方、营养学特征、适用人群等内容的,不得超出注册证书、产品标签、说明书范围。特殊医学用途配方食品广告应当显著标明适用人群、“不适用于非目标人群使用”“请在医生或者临床营养师指导下使用”。
药品、医疗器械、保健食品和特殊医学用途配方食品广告应当显著标明广告批准文号。
药品、医疗器械、保健食品和特殊医学用途配方食品广告中应当显著标明的内容,其字体和颜色必须清晰可见、易于辨认,在视频广告中应当持续显示。
(三)药品广告的限制要求
1.广告不得有下列情形:
(1)使用或者变相使用中华人民共和国的国旗、国歌、国徽,军旗、军歌、军徽。
(2)使用或者变相使用国家机关、国家机关工作人员的名义或者形象。
(3)使用“国家级”“最高级”“最佳”等用语。
(4)损害国家的尊严或者利益,泄露国家秘密。
(5)妨碍社会安定,损害社会公共利益。
(6)危害人身、财产安全,泄露个人隐私。
(7)妨碍社会公共秩序或者违背社会良好风尚。
(8)含有淫秽、色情、赌博、迷信、恐怖、暴力的内容。
(9)含有民族、种族、宗教、性别歧视的内容。
(10)妨碍环境、自然资源或者文化遗产保护。
(11)法律、行政法规规定禁止的其他情形。
2.医疗、药品、医疗器械广告不得含有下列内容:
(1)表示功效、安全性的断言或者保证。
(2)说明治愈率或者有效率。
(3)与其他药品、医疗器械的功效和安全性或者其他医疗机构比较。
(4)利用广告代言人作推荐、证明。
(5)法律、行政法规规定禁止的其他内容。
3.除医疗、药品、医疗器械广告外,禁止其他任何广告涉及疾病治疗功能,并不得使用医疗用语或者易使推销的商品与药品、医疗器械相混淆的用语。
4.保健食品广告不得含有下列内容:(https://www.daowen.com)
(1)表示功效、安全性的断言或者保证。
(2)涉及疾病预防、治疗功能。
(3)声称或者暗示广告商品为保障健康所必需。
(4)与药品、其他保健食品进行比较。
(5)利用广告代言人作推荐、证明。
(6)法律、行政法规规定禁止的其他内容。
5.广播电台、电视台、报刊音像出版单位、互联网信息服务提供者不得以介绍健康、养生知识等形式变相发布医疗、药品、医疗器械、保健食品广告。
6.药品、医疗器械、保健食品和特殊医学用途配方食品广告不得包含下列情形:
(1)使用或者变相使用国家机关、国家机关工作人员、军队单位或者军队人员的名义或者形象,或者利用军队装备、设施等从事广告宣传。
(2)使用科研单位、学术机构、行业协会或者专家、学者、医师、药师、临床营养师、患者等的名义或者形象作推荐、证明。
(3)违反科学规律,明示或者暗示可以治疗所有疾病、适应所有症状、适应所有人群,或者正常生活和治疗病症所必需等内容。
(4)引起公众对所处健康状况和所患疾病产生不必要的担忧和恐惧,或者使公众误解不使用该产品会患某种疾病或者加重病情的内容。
(5)含有“安全”“安全无毒副作用”“毒副作用小”;明示或者暗示成分为“天然”,因而安全性有保证等内容。
(6)含有“热销、抢购、试用”“家庭必备、免费治疗、免费赠送”等诱导性内容,“评比、排序、推荐、指定、选用、获奖”等综合性评价内容,“无效退款、保险公司保险”等保证性内容,怂恿消费者任意、过量使用药品、保健食品和特殊医学用途配方食品的内容。
(7)含有医疗机构的名称、地址、联系方式、诊疗项目、诊疗方法以及有关义诊、医疗咨询电话、开设特约门诊等医疗服务的内容。
(8)法律、行政法规规定不得含有的其他内容。
课堂互动
日常生活中,你发现过哪些涉嫌违法的药品广告?它们违反了广告法中的哪些条款?
(四)广告发布媒体的限制
处方药和特殊医学用途配方食品中的特定全营养配方食品广告只能在国务院卫生行政部门和国务院药品监督管理部门共同指定的医学、药学专业刊物上发布。
不得利用处方药或者特定全营养配方食品的名称为各种活动冠名进行广告宣传。不得使用与处方药名称或者特定全营养配方食品名称相同的商标、企业字号在医学、药学专业刊物以外的媒介变相发布广告,也不得利用该商标、企业字号为各种活动冠名进行广告宣传。
特殊医学用途婴儿配方食品广告不得在大众传播媒介或者公共场所发布。
(五)药品广告的审查
1.药品广告的审查对象 凡利用各种媒介或者形式发布的广告含有药品名称、药品适应证(功能主治)或者与药品有关的其他内容的,为药品广告,应按照《药品广告审查办法》进行审查。非处方药仅宣传药品名称(含药品通用名称和药品商品名称)的,或者处方药在指定的医学药学专业刊物上仅宣传药品名称(含药品通用名称和药品商品名称)的,无须审查。
2.药品广告审查机关和监督管理机关
(1)药品广告审查机关:国家市场监督管理总局负责组织指导药品、医疗器械、保健食品和特殊医学用途配方食品广告审查工作。各省、自治区、直辖市市场监督管理部门、药品监督管理部门(简称广告审查机关)负责药品、医疗器械、保健食品和特殊医学用途配方食品广告审查,依法可以委托其他行政机关具体实施广告审查。
(2)药品广告监督管理机关:国务院市场监督管理部门主管全国的广告监督管理工作,国务院有关部门在各自的职责范围内负责广告管理相关工作。县级以上地方市场监督管理部门主管本行政区域的广告监督管理工作,有权对违法广告依法作出处理。
3.药品广告审查规定
(1)药品广告批准文号申请人:药品注册证明文件或者备案凭证持有人及其授权同意的生产、经营企业为广告申请人(简称申请人)。申请人可以委托代理人办理药品广告审查申请。药品广告审查申请应当依法向生产企业或者进口代理人等广告主所在地广告审查机关提出。
(2)药品广告批准文号应提交的材料:申请药品广告批准文号,应当提交《药品广告审查表》,与发布内容相一致的样稿(样片、样带),以及以下真实、合法、有效的证明文件。
a.申请人的主体资格相关材料,或者合法有效的登记文件。
b.产品注册证明文件或者备案凭证、注册或者备案的产品标签和说明书,以及生产许可文件。
c.广告中涉及的知识产权相关有效证明材料。
经授权同意作为申请人的生产、经营企业,还应当提交合法的授权文件;委托代理人进行申请的,还应当提交委托书和代理人的主体资格相关材料。
申请人可以到广告审查机关受理窗口提出申请,也可以通过信函、传真、电子邮件或者电子政务平台提交药品、医疗器械、保健食品和特殊医学用途配方食品广告申请。
4.药品广告的审批程序 药品广告审查机关收到药品广告批准文号申请后,对申请材料齐全并符合法定要求的,发给药品广告受理通知书;申请材料不齐全或者不符合法定要求的,应当当场或者在5个工作日内一次告知申请人需要补正的全部内容;逾期不告知的,自收到申请材料之日起即为受理。
药品广告审查机关应当自受理之日起10个工作日内,对申请人提交的证明文件的真实性、合法性、有效性进行审查,并依法对广告内容进行审查。对审查合格的药品广告,发给药品广告批准文号;对审查不合格的药品广告,应当作出不予核发药品广告批准文号的决定,书面通知申请人并说明理由,同时告知申请人享有依法申请行政复议或者提起行政诉讼的权利。
对批准的药品广告,药品广告审查机关应当报国家药品监督管理局备案,并将批准的药品广告审查表送同级广告监督管理机关备案。对批准的药品广告,药品监督管理部门应当及时向社会予以公布。公开的信息应当包括广告批准文号、申请人名称、广告发布内容、广告批准文号有效期、广告类别、产品名称、产品注册证明文件或者备案凭证编号等内容。药品广告的审批程序如图9-2所示。
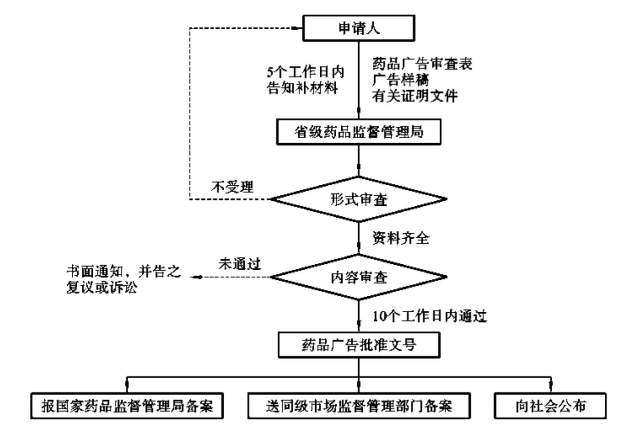
图9-2 药品广告的审批程序
5.异地发布广告的申请 在药品生产企业所在地和进口药品代理机构所在地以外的省、自治区、直辖市发布药品广告的(以下简称异地发布药品广告),在发布前应当到发布地药品广告审查机关办理备案。
异地发布药品广告备案应当提交如下材料:①药品广告审查表复印件;②批准的药品说明书复印件;③电视广告和广播广告需提交与通过审查的内容相一致的录音带、光盘或者其他介质载体。
提供规定的材料的复印件,需加盖证件持有单位印章。
