大黄《神农本草经》
本品为蓼科植物掌叶大黄Rheum palmatum L.、唐古特大黄Rheum tanguticum Maxim.ex Balf.或药用大黄Rheum officinale Baill.的干燥根和根茎。
苦,寒。归脾、胃、大肠、肝、心包经。泻下攻积,清热泻火,凉血解毒,逐瘀通经,利湿退黄。用于实热积滞便秘,血热吐衄,目赤咽肿,痈肿疔疮,肠痈腹痛,瘀血经闭,产后瘀阻,跌打损伤,湿热痢疾,黄疸尿赤,淋证,水肿;外治烧烫伤。
(一)毒性成分
大黄中大黄素等蒽醌类成分和鞣质类成分具有毒性。大黄蒽醌类成分中,大黄素含量最高,是大黄重要的毒性成分。
(二)毒性作用与机制
1.毒性作用
消化系统:大黄对肝脏具有毒性。可出现腹泻、腹痛、呕吐、恶心、肠鸣等胃肠反应,造成电解质紊乱。大黄可治疗黄疸,但疗程过长或剂量过大可引起胆红素代谢障碍,加重病情。以肝癌细胞HepG2为模型,其毒性大小顺序为:大黄酸>大黄素>芦荟大黄素>大黄酚和大黄素甲醚。大黄中的鞣质有收敛作用,可麻痹肠神经,停药后可能出现继发性便秘。鞣质、蒽醌类成分常引发结肠黑变病。
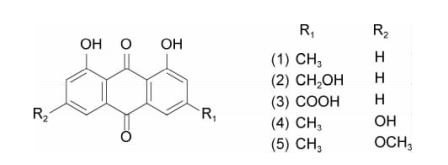
图9-1 大黄部分毒性成分
(1)大黄酚(CAS NO.:481-74-3);(2)芦荟大黄素(CAS NO.:481-72-1);(3)大黄酸(CAS NO.:478-43-3);(4)大黄素(CAS NO.:518-82-1);(5)大黄素甲醚(CAS NO.:521-61-9)
呼吸系统:支气管哮喘患者服用大黄后,可出现皮疹、水疱、哮喘加重等过敏反应。
泌尿系统:常见为肾损伤。对肾小管上皮HK-2细胞的毒性大小顺序为:大黄素甲醚>大黄酸>大黄素>芦荟大黄素>大黄酚。
免疫系统:大鼠ig大黄可引起“虚证”,胸腺、脾、肠系膜淋巴结等免疫器官减轻、变小,小鼠实验中也可引起胸腺明显萎缩。
急性毒性:单次给药毒性研究表明,小鼠单次ig生大黄粉剂的LD 50>5.00 g/kg;小鼠单次ig水煎剂的LD 50>10.00 g生药/kg,大鼠单次ig的LD 50>6.00 g生药/kg。小鼠单次ig掌叶大黄生品水煎液的LD 50为153.50 g生药/kg。单次使用大黄30 g以上,所含苷类对胃肠黏膜的强烈刺激作用可引起呕吐、峻泻等毒性反应。小鼠ig大黄后,血清ALT和γ-谷氨酰转肽酶(γ-glutamyltranspeptidase,γ-GT)随剂量增加而升高,剂量达到8.00 g/kg时可引起小鼠肝脏脂肪变性,TNF-α表达增加。
慢性毒性:重复给药毒性研究表明,昆明小鼠ig不同剂量大黄素,1次/d,共28 d,结果1 000 mg/kg剂量大黄素可使昆明小鼠产生明显的全身毒性,出现肝、肾、胆囊损伤;600 mg/kg剂量大黄素引起的肝、肾损伤较轻。另有研究发现,大鼠分别ig大黄素40 mg/kg、80 mg/kg,1次/d,共30 d,均能升高大鼠血清ALT、总胆汁酸(total bile acid,TBA)、直接胆红素(direct bilirubin,DBIL)和总胆红素(total bilirubin,TBIL)含量。
特殊毒性:对大黄的三致作用实验发现,生大黄可对妊娠个体子宫内膜形态结构产生损害,改变早期胚胎发育的良好环境,引起早期胚胎流产。对大鼠的实验研究发现,雌鼠ig大黄7.5 g/kg,连续14 d,可见性成熟期明显延缓,子宫、卵巢重量显著减轻。芦荟大黄素经多种细胞株Ames试验显示有致突变作用;大黄素及其他蒽醌类化合物在多种细胞株试验中表现有遗传毒性作用。(https://www.daowen.com)
2.毒理机制
消化系统:大黄引起肝肾毒性的成分主要为蒽醌类化合物,对肝肾的毒性大小为:总结合蒽醌>总鞣质>总游离蒽醌。炮制可减少大黄肝肾毒性,主要与炮制后大黄中的结合蒽醌和鞣质类成分降低有关。大黄素、芦荟大黄素、大黄酸、大黄酚等蒽醌类成分和鞣质水解产物是大黄肝毒性的物质基础,损伤机制与提高TNF-α表达,上调P-gp、Nrp3表达,下调钠离子-牛黄胆酸共转运蛋白[(Na+/taurocholate cotransporting)polypeptide,Ntcp]、尿苷二磷酸葡萄糖醛酸转移酶1A1(UDP-glucuronyl transferases 1A1 UGT1A1)mRNA和蛋白表达,从而引起肝脏脂肪变性,诱导肝脏纤维化相关;同时与IL介导炎症反应、通过线粒体Caspase通路诱导L02细胞和HepG2细胞凋亡、激活内质网应激能力和Ca2+通道等途径有关。与幼年大鼠相比,衰老大鼠对40 g/kg剂量的大黄提取物毒性反应更为明显,出现肝细胞坏死和小胆管增生,肝窦区枯否细胞活化和淋巴细胞浸润增多,系由IL介导的炎症反应造成肝损伤,肝细胞纤维化也参与引起了肝损伤。
泌尿系统:大黄素、大黄酸和大黄素甲醚等蒽醌类成分是大黄肾毒性的物质基础,毒理机制与升高BUN、血肌酐(serum creatinine,Scr)、β2微球蛋白(β2-microglobulin,β2 M)、胱抑素C(cystain C,Cys-C)、乳酸脱氢酶(lactate dehydrogense,LDH)、N-乙酰-β-D-氨基葡萄糖苷酶(N-acetyl-β-D-glucosaminidase,NAG)、中性粒细胞明胶酶相关脂质运载蛋白(neutrophil gelatinase-associated lipocalin,NGAL)含量和活性,上调Oat1、Oat3、Bax的mRNA和PPARγ表达水平,抑制HK-2细胞增殖促进其凋亡,阻滞人肾皮质/近曲小管细胞HK-2的细胞周期,诱导肾小管透明小滴生成和肾小管色素沉着相关,也涉及线粒体膜电位途径凋亡机制(Bax/Caspase途径),p38MAPK通路中促分裂原活化的蛋白激酶(mitogen-activated protein kinase,MAPK)和CYP1A1基因激活,以及机体氧化应激、细胞凋亡、炎症反应等途径。
(三)毒代动力学
目前尚无大黄毒代动力学报道。其药代动力学为:核素标记的大黄素单剂量口服,吸收2 h达峰,24 h时血药浓度下降为峰浓度的30%,随后下降较为缓慢;主要分布于肾、肠系膜和脂肪组织,脑、肌肉、小肠和结肠中较少分布。小鼠ig大黄素91 mg/kg,0~48 h内由尿排出的总蒽醌类衍生物约为53%,含有大黄素葡萄糖醛酸苷、其他蒽醌类代谢产物及大黄素。大黄蒽醌类衍生物在肝、肾、胆囊分布最多,均可与GA结合;经尿排泄约22.8%,2~4 h排泄达峰;由粪便排泄约23.4%。大鼠、小鼠ig大黄素甲醚,代谢产物主要为大黄素、大黄酚等,大黄酚在体内可进一步氧化为芦荟大黄素和大黄酸,仍有较强活性。Beagle犬分组经口分别给予大黄酸35 mg/kg、111 mg/kg和350 mg/kg,给药39周,各剂量大黄酸在犬体内的毒代动力学过程基本一致,单次和多次给药后的AUC和C max无明显改变。
(四)毒性作用的预防
1.病症禁忌 孕妇及月经期、哺乳期患者慎用。
2.使用注意
炮制适应证:酒大黄善清上焦血分热毒,用于目赤咽肿、齿龈肿痛;熟大黄泻下力缓、泻火解毒,用于火毒疮疡;大黄炭凉血化瘀止血,用于血热有瘀出血症。酒炖、炒制、蒸制、制炭等可消除或减弱大黄的泻下作用,同时可增强其止血等作用。
炮制减毒:实验发现,生大黄总提取物的最小中毒剂量为20 g/kg,而炮制后的熟大黄总提取物最小中毒剂量增大为40 g/kg,炮制发挥了减毒作用。
配伍减毒:比较生大黄总提取物与大黄蟅虫丸的最小中毒剂量,两者分别为20 g/kg和44 g/kg,表明配伍减轻了大黄的毒性。
用法用量:3~15 g,外用适量。
基原鉴别:应注意正品大黄之外,被混用的同属品种,如河套大黄(Rheum hotaoense C.Y.Cheng et Kao)来源的药材泻下作用较弱,但可引起腹痛,仅作兽药。
(五)中毒救治
西医救治:用0.1%鞣酸溶液洗胃,并采取其他对症治疗措施。
中医救治:生地榆、干姜各9 g,煎汤,加红糖适量服用。
