何首乌《神农本草经》
本品为蓼科植物何首乌Polygonum multiflorum Thunb.的干燥块根。
苦、甘、涩,微温。归肝、心、肾经。解毒,消痈,截疟,润肠通便。用于疮痈,瘰疬,风疹瘙痒,久疟体虚,肠燥便秘。
(一)毒性成分
何首乌的毒性与其含有的蒽醌类衍生物有关,如大黄素、大黄酸、大黄酚、大黄素甲醚(此四者参见[大黄]项)及其苷,大黄酚蒽酮及其苷等。此外,还有顺式-二苯乙烯苷(cis-TSHG)、反式-二苯乙烯苷(trans-TSHG)、鞣质等。
(二)毒性作用与机制
1.毒性作用
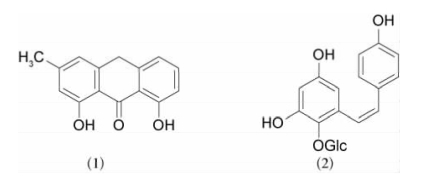
图23-5 何首乌部分毒性成分
(1)大黄酚蒽酮(CAS NO.:491-58-7);(2)顺式-二苯乙烯苷(CAS NO.:928205-59-8)
消化系统:何首乌致肝损伤的毒性有一定的蓄积性,多在连续服药4周后产生毒性反应;症状有乏力、纳差、尿黄如浓茶色,伴皮肤黄染、肝功能指标异常,表现为黄疸型肝炎。蒽醌类衍生物对肝脏可能有一定毒性作用。何首乌也含有磷脂酰胆碱,有类似肾上腺皮质激素样作用。
泌尿系统:何首乌及其炮制品制何首乌导致SD大鼠出现肾小管上皮细胞水肿颗粒样变性、肾小球体积增大、毛细血管腔开放欠佳、伴系膜细胞及基质增生等病变特征。
呼吸系统:可使肺组织出现不同程度损伤,有炎性细胞浸润、纤维组织增生等病变特征。另有报道服用何首乌后可能出现继发性肺结核。
急性毒性:大鼠ig何首乌醇渗漉液的LD 50为50 g/kg,ip何首乌的LD 50为27 g/kg,ip制何首乌的LD 50为169.4 g/kg。
慢性毒性:大鼠连续ig制首乌提取液,3个月后肝脏组织病理切片可见散在炎性细胞浸润,肝血窦充血,枯否氏细胞增生活跃并可见吞噬色素颗粒;透射电镜下大剂量给药组可见部分肝细胞核内染色质凝集或边集于核膜下,线粒体轻度肿胀,停药后恢复。此外,大鼠ig何首乌醇提物40 g/kg,连续28天后,肺脏一定程度肿大,肺脏指数显著高于对照组。(https://www.daowen.com)
特殊毒性:何首乌活性成分能使囊胚着床成功率显著下降,抑制早期胚胎发育,具有胚胎毒性。
2.毒理机制
消化系统:肝损伤的主要机制可能为:①毒性成分的蓄积作用。大鼠连续ig何首乌提取物20 g/kg,21 d后,大黄素在体内蓄积,其AUC和C max显著增加,导致胆汁淤积、胆红素及胆汁酸代谢障碍、肝细胞凋亡。此外,顺式二苯乙烯苷的肝毒性比反式高,采用类器官3D培养模型发现顺式二苯乙烯苷的毒性约为反式的4.1倍。其他毒性成分还包括鞣质类。如没食子酸通过介导内质网应激,引起肝细胞凋亡。②与肝脏代谢酶遗传缺陷有关。③何首乌在机体代谢过程中产生毒性物质,引起脂质过氧化而造成肝损伤;某种毒性物质抑制细胞膜运载胆盐的受体,影响细胞膜Na+__K+__ATP酶活性,使肝细胞正常的结构和代谢功能发生异常。④何首乌肝毒性为免疫特异质型,发现并确定了何首乌肝损伤的主要易感病证和易感物质。
泌尿系统:何首乌的肾毒性与何首乌中蒽醌类成分如大黄素相关。体外试验表明,大黄素对HK-2细胞增殖有时间依赖性和剂量依赖性的抑制作用,大黄素还能上调Caspase-3诱导细胞凋亡。
生殖系统:大黄素预处理后,细胞凋亡增加,囊胚着床成功率显著下降,体内实验也表明大黄素能够抑制细胞增殖,抑制早期胚胎发育。大黄素能降低卵母细胞成熟率和受精率、抑制胚胎发育、降低胎儿体重,通过Caspase-3依赖的凋亡过程致胚胎损伤。
(三)毒代动力学
目前尚无何首乌毒代动力学报道。其药代动力学为:大黄素在大鼠体内的药物动力学符合二室模型,血药浓度在9 min达峰,C max为3.973μg/m L,给药后24 h,血浆中药物浓度明显降低。
(四)毒性作用的预防
1.病证禁忌 大便溏泄及有湿痰者慎服。
2.使用注意
用法用量:3~6 g。忌铁器。临床使用时应严密观察药物对肝脏的反应。
炮制适应证:由于生何首乌、制何首乌药理作用和临床应用有所差别,使用时应区分,“生用则泻下,制用则补益”。
(五)中毒救治
西医救治:如中毒立即停止服用含何首乌的制剂;给予保肝解毒剂,如还原型GSH、维生素C、葡萄糖等。
