围手术期处理建议
1.术前准备·对于高风险患者,充分完备的术前准备能够降低围手术期脑卒中的发生率,术前准备主要包括术前指导患者合理使用抗血小板抗凝药物,检查患者是否术前已经存在血栓等。
(1)抗血小板聚集:抗血小板药已成为缺血性卒中一级和二级预防的重要手段,围手术期必须进行分层风险评价以决定是否继续应用抗血小板药。血栓事件低危患者可以停用,而出血风险低于动脉血栓风险的患者仍应继续应用抗血小板药[35]。
1)阿司匹林:阿司匹林服用后1 h 可使血栓素B 降低80%,单剂服药后抑制血小板聚集持续10 日,而血小板的平均寿命为7~10 日。
2)氯吡格雷:氯吡格雷通过选择性抑制二磷酸腺苷诱导的血小板聚集发挥抗血小板聚集效应。氯吡格雷预防卒中的指征明确,但手术期间如何应用尚无定论。氯吡格雷停药7 日后血小板功能恢复正常;当术前停药小于5 日时,其严重出血风险要高于阿司匹林。
3)阿司匹林+氯吡格雷联合治疗,见表5-1-4。
表5-1-4 CABG 和CEA 围手术期抗血小板治疗推荐

(2)抗凝:即使在重大外科手术前中断抗凝治疗也有可能导致灾难性后果,围手术期抗凝与否必须权衡缺血与出血之间的利弊。
对于必须中断华法林抗凝治疗的患者,应考虑术后应用肝素或低分子肝素,但目前是否必须要使用肝素桥接抗凝存在一些别的看法(参考本章节上述相关内容)。
术前抗凝治疗主要是为了降低术后并发症发生率。对于华法林治疗INR 目标值为2.0 ~3.0 的患者,停药5 日内手术应保证手术时INR 正常;老年人的INR 可能需要更长时间才能恢复正常。对于INR 目标值为2.5~3.5 的患者,停用华法林6 日后手术是合理的。术前必须监测INR,如术前1 日INR>1.5,则应口服小剂量维生素K(1~2 mg)以保证手术当日INR 正常。术后恢复应用华法林的时间依手术类型而定。表5-1-5 对术后抗凝药治疗的推荐进行了总结[36]。
表5-1-5 危险分层与术后抗凝
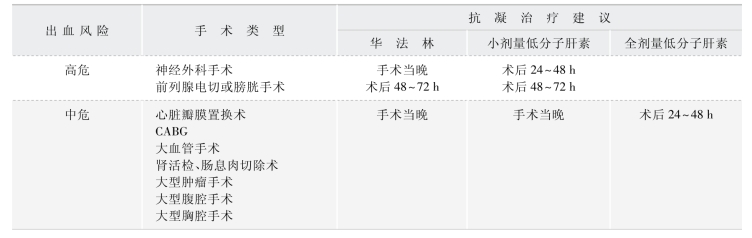
(续 表)

(3)肺炎:明确诊断者可予抗生素治疗。
(4)深静脉血栓:行B 超检查是否有下肢深静脉血栓形成,是否有必要治疗。
2.围手术期脑保护策略·围手术期与脑保护密切相关的生理学参数主要包括体温、血糖和血压的管理。动物实验证实低温对局灶性和全脑缺血均有保护作用。
(1)血压:对于脑卒中后遗症患者而言,麻醉管理的重点在于维持正常的脑组织血流灌注[28]。围手术期降压目标不是统一地把SBP、DBP、MAP 降低超过20%,而是应该以保护器官功能为准则,所以提出治疗个体化来解决既要降压还要保证脑和肾等的器官灌注。一般而言,术中MAP 下降大于基础值的30%可能增加围手术期脑卒中风险,对于既往有脑卒中病史的高危患者,MAP 降低较基础血压降低应小于20%。所以当患者出现血压下降趋势时即行扩容、升压等干预,在不增加心脏负担的前提下尽可能维持充足的脑组织灌注,避免脑缺血的发生。(https://www.daowen.com)
降压前需要筛查颅内动脉严重狭窄或闭塞者,对于双侧颈动脉狭窄在70%以下者可以常规降压治疗,对于狭窄超过70%者,降压要慎重,过度降压可使死亡率增加[37]。急性脑卒中时血压升高属于机体的自我保护机制,目前认为除非血压超过220/120 mmHg,否则不宜使用降压药物。
(2)体温:虽然有临床试验证实浅低温(33 ~35℃)能提供良好的脑保护效果,然而一项全球多中心大样本临床研究显示,对1 001 例颅内动脉瘤手术的患者,术中浅低温(33℃)并未明显减轻围手术期脑缺血损伤的发生[38]。关于低体温是否有脑保护作用的争议,可能与降温时程、低温和复温过程的不良反应等有关。
(3)血糖:血糖在决定脑缺血损伤的预后中占有重要的地位。糖尿病和短暂高血糖的患者卒中后1 年的死亡率大于血糖正常的患者。但研究也表明无论低血糖还是高血糖对于术后患者来说都是一个不利因素,与术后不良结局相关。一项研究表明,心脏手术中对于非糖尿病患者严格控制血糖围手术期卒中率高于血糖宽松控制组,而对于糖尿病患者严格控制血糖,术后的死亡率和感染率都能降低,另外,也有研究表明对于非心脏手术,避免高血糖对于糖尿病和非糖尿病患者都能获益。因此,目前对于血糖的控制仍然存在争议。建议将血糖浓度保持在最佳范围;建议采用胰岛素治疗的范围:血糖浓度超过8.4 mmol/L(150 mg/dL),绝对上限为10.08 mmol/L(180 mg/dL)时开始胰岛素治疗;如果血糖浓度低于5.6 mmol /L(100 mg /dL),且绝对下限为3.92 mmol/L(70 mg/dL),则应减少胰岛素治疗。无论如何,对于有围手术期卒中危险的患者,应经常控制血糖浓度[39,40]。
(4)麻醉与麻醉药:大量的研究证实局部麻醉药(利多卡因)、镇静药、阿片类镇痛药、静脉麻醉药和吸入麻醉药等,均可减轻动物脑缺血再灌注损伤[40]。丙泊酚能够剂量依赖性降低脑代谢率,即使在缺血后1 h 给予,仍能够减少神经元凋亡和脑梗死容积,适合用于神经外科手术。氯胺酮能够阻断NMDA 受体,被认为是有神经保护效应的麻醉药物。几乎所有的吸入麻醉药如异氟烷、七氟烷、地氟烷等均可减少缺血性脑损伤。但是否产生脑保护作用与其使用的剂量、时机、持续时间及脑缺血损伤的严重程度密切相关。依托咪酯的脑保护作用尚存争议,但临床上仍然可用于神经外科手术的麻醉。咪达唑仑不考虑作为脑保护药物。尽管大量实验研究表明麻醉药具有神经保护作用,但何种麻醉药物在临床上如何应用发挥脑保护作用目前仍无定论。
多年以来,一直认为麻醉药通过抑制脑电活动、降低脑氧代谢率而发挥脑保护。新近的研究认为,麻醉药的神经保护作用是多因素、多途径的,仍需要深入研究其神经保护作用机制。麻醉药神经保护的另一焦点问题是何时实施能达到最好效果。虽然有研究表明,麻醉药的神经保护作用可持续2~4 周,而麻醉药神经保护作用的相关临床表现可能具有一个时间窗。研究也显示麻醉药对轻、中度的脑缺血性损伤具有长期的保护作用,而对重度缺血性损伤可能无效,对于超过一定限度的严重损伤,麻醉药未必具有保护作用。另外,一些研究表明,对于处于发育过程中的神经细胞,麻醉药可引起退行性变甚至神经元细胞死亡[40]。
(5)过度通气:研究发现在动脉粥样硬化患者中,轻度高碳酸血症(PaC02 >40 ~45 mmHg)能扩张脑血管,对于改善脑灌注可能是有益的,相对的,必须避免低碳酸血症,因为它减少了区域脑血流量,大脑灰质减少尤其明显[40]。另外,也应避免低氧血症,因为低氧可导致脑血管的收缩[40]。
(6)严密的术中监测:对于围手术期卒中的防治关键是早发现,早治疗。术中可辅助使用各种神经监测措施,如脑电图、经颅多普勒超声等,术中可使用短效药物,缩短复苏时间,尽早对患者的精神状态进行判断[40]。
(7)神经保护剂:神经保护剂的研发与缺血级联反应的病理生理通路息息相关,其中包括离子紊乱、神经递质释放、程序性死亡、自由基产生、炎症反应等。
1)溶栓剂:适用于发病6 h 以内的早期患者,超过8 h 后,药物的效果则明显降低。临床常用药物主要有链激酶、尿激酶和重组组织型纤溶酶原激活物(rt-PA)等。临床医师常以rt-PA 作为首选溶栓药物,此药在发病后3 h 内使用效果显著,但易导致脑出血。
2)自由基清除剂:一些自由基清除剂或抗氧化药物在实验室研究中被证实能够产生明确的脑保护效应,如依达拉奉、NXY-059,但在临床应用的效果并不显著。
3)他汀类药物:他汀类药物可通过抗炎和斑块稳定等作用减少心脑血管事件。接受CEA 患者中,术前长期定期服用他汀类药物者围手术期卒中风险和死亡率更低。在非心血管性手术中,围手术期使用他汀类药物也可降低心肌梗死风险和平均住院时间。术前至少2 周给予他汀类药物可降低血管手术患者的卒中发生率。重大非心脏手术后停用他汀类药物与较差的心脏结局和缺血性卒中有关。对于围手术期卒中高危患者,定期服用他汀类药物可能具有保护作用,不应停用[40]。
4)镁剂:在外伤及缺血损伤的动物模型中,镁被证明有神经保护效应,并且即使在损伤发生后24 h 给予镁剂,仍然可以发挥保护效应。镁剂的神经保护作用与开始治疗时间和病种类型等有关。
(8)预处理:预处理的理论基础是预先给予大脑一个不引起脑损伤的较小刺激,能够加强大脑对将来发生的较严重的损伤性事件的耐受能力。然而,缺血预处理在临床中的不可操作性,使其应用受到很大限制。研究发现高压氧、氟醚类麻醉药、低频电针刺激,这三种非缺血预处理措施,可模拟缺血预处理效果产生远程缺血预处理(remote ischemic preconditioning,RIPC),即一个器官的短暂缺血再灌注可以通过在循环中释放生化信使或激活神经通路而对远隔器官缺血/再灌注损伤产生保护作用,对受保护的靶器官无创伤且不产生直接应激[41]。一项发表在循环杂志上的临床研究表明对于严重的颈内动脉狭窄,单纯的RIPC 也能明显增加大脑灌注量,减少斑块体积[42]。由于R1PC 无创伤、操作简便,克服了经典缺血预处理临床可操作性差等缺点,具有良好的临床应用价值。
3.围手术期脑卒中的治疗
(1)溶栓治疗:虽然早已批准rt-PA 静脉溶栓用于治疗发病3 h 内的急性缺血性卒中的治疗,但对于围手术期卒中显然是禁忌。心脏手术后在经过选择的急性缺血性卒中患者中进行动脉溶栓相当安全。在13 例心脏手术后发生缺血性卒中的患者中,12 例在6 h 内应用尿激酶(2.5 万~5 万单位,间隔5~10 min)或rt-PA(20~50 mg)进行动脉溶栓直至血管再通,38%的患者神经系统症状显著改善;仅1 例患者因胸腔出血需行胸导管引流,未予动脉溶栓[43]。另一项研究也证实了动脉溶栓治疗CEA 术后缺血性卒中的安全性[44]。
(2)机械取栓:经动脉机械取栓术是近年来出现的一项新技术,因为并非所有栓子对动脉或静脉溶栓有反应,而且围手术期溶栓治疗的应用受到严格限制,因此在围手术期卒中的治疗中扮演着重要角色。对305 例围手术期卒中患者进行了MERCI 机械取栓治疗,其中48 例为静脉rt-PA 溶栓失败者,257 例不适合溶栓。结果表明,静脉溶栓无反应的患者MERCI 治疗血管再通率较高(73% vs.63%),病死率较低(27.7% vs.40.1%),90 日时神经功能恢复也较好[43]。
(3)扩容治疗:如前所述,对于低血容量导致的分水岭梗死,仅50%的患者对扩容治疗有反应[45]。
(作者 胡静萍 谭芳,审校 蔡珺)
