吸入麻醉药的药动学
麻醉气体在各种组织器官的分配系数是决定其摄取、分布、排泄的重要因素,分配系数与麻醉诱导、维持及苏醒过程密切相关。
1.吸收 所下所述。
(1)吸入麻醉药的吸收过程包括麻醉药从麻醉机挥发罐,氧化亚氮(N2O)从气体管道经过呼吸管道到达血液循环。在向肺泡内输送气体的过程中,麻醉药吸入浓度越高,肺泡内气体浓度上升越快,此为浓度效应。若两种不同浓度的麻醉气体同时输送,则高浓度气体(称为第一气体)被吸收的同时,可提高低浓度气体(称为第二气体)的吸收速率,此种现象谓之第二气体效应(图5-1)。常用吸入麻醉药的分配系数,见表5-2。
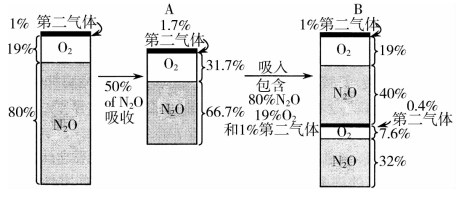
图5-1 第二气体效应
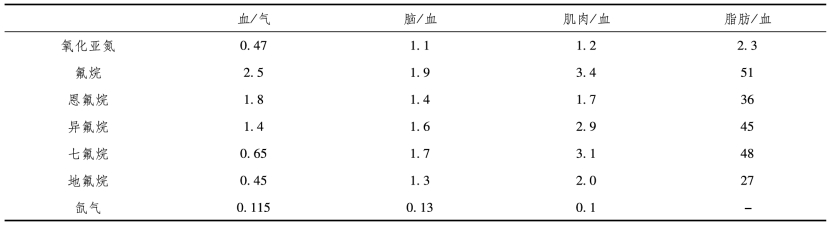
表5-2 常用吸入麻醉药的分配系数(1个大气压下,37℃)
 (https://www.daowen.com)
(https://www.daowen.com)
(2)肺循环对吸入麻醉药的摄取取决于麻醉气体的血/气分配系数(λ)、心排出量(Q)和肺泡-静脉血麻醉药分压差(PA-PV),通常用公式“摄取=[(λ)×(Q)×(PA-PV)/大气压]”表示,入大者,麻醉气体易溶于血,可经肺循环被迅速移走,使肺泡内分压上升速度慢,麻醉诱导时间长;λ小者则相反,其麻醉诱导时间缩短。肺循环与心排出量对肺内吸入麻醉药分压的影响与其同理,肺血流增加以及心排出量增加,均能使药物迅速被血流移走而降低肺泡内分压。而存在心力衰竭、休克等情况时,药物移走速度减慢,肺内分压则很快上升。
2.分布 如下所述。
(1)吸入麻醉药吸收进入血液循环后,很快随血流到达全身各组织器官。某一组织所摄取的麻醉药量与组织的容积、组织对麻醉药的亲和性或该药的溶解度密切相关。气体麻醉药在各个器官内的分布与麻醉诱导、维持以及恢复均密切相关。
(2)一般根据麻醉药的分布将不同组织分为四组:脑、心、肝、肾、内分泌器官等为血管丰富组织(VRG),在诱导早期便能摄取大量的药物,使组织内麻醉药分压与动脉血分压迅速达到平衡,在4~8min内,便能达到动脉血中的95%;肌肉和皮肤组成肌肉群(MG),在VRG达平衡后的长时间内,MG是主要的麻醉药分布系统,在2~4h内可达到平衡;脂肪群(FG)是MG达平衡后的主要药物贮藏库;由韧带、肌腱、骨骼和软组织等组成的血管稀疏组织(VPG)血流灌注少,所以并不参与麻醉药的分布。
(3)在麻醉诱导开始时,VRG的摄取决定脑内达到所需MAC的时间。在麻醉维持阶段,麻醉药在不同组织内的分布差异相当大,并影响麻醉药的用量以及药物对各器官的作用。当停止输送麻醉气体,机体转入麻醉恢复阶段时,VRG的分压迅速下降,并与肺泡内分压相等。但对MG、FG、VPG而言,麻醉时间长短决定其达到平衡与否及药物摄取量的多少。因此在麻醉恢复中,若麻醉维持时间短,血流灌注量少的组织由于吸入麻醉药量少,此时仍未与血中浓度达到平衡而继续摄取,从而使动脉血中麻醉药浓度下降,对麻醉的苏醒具有促进作用;但长时间麻醉后,上述组织群内吸入麻醉药摄取量增多并已达平衡,一旦血中麻醉药浓度降低,则低血流灌注组织中向血中释放麻醉药,再分布至VRG,使苏醒时间延长。
3.转化 各种吸入麻醉药在体内均有不同程度的生物转化,目前在临床应用的吸入麻醉药中,以地氟烷在体内代谢最少。吸入麻醉药脂溶性大,首先要在肝内进行氧化代谢以及与亲水基团结合,最后才能经肾排出体外。肝内的细胞色素P450,是主要的药物氧化代谢酶。氟烷、甲氧氟烷、N2O均有自身酶诱导作用,长时间吸入亚麻醉剂量的健康人,其肝脏药物代谢能力明显增强。
4.排泄 麻醉气体大部分通过肺部以原形排出,小部分在体内进行生物转化,极少量经手术创面、皮肤排出体外。吸入麻醉药的排泄与麻醉过程相似,亦受吸收及分布等相关因素的影响,其中最大影响因素为血液溶解度、组织/血分配系数、心排出量及肺泡通气量。组织溶解度大者,从组织释放回血液到肺泡的速率则减慢,导致苏醒延长。足够的心排出量可快速将药物从组织带到血液中,再经血液从肺泡排出。目前临床所应用的吸入麻醉药均具有苏醒快的优点,停止吸入后多能在6~10min内达到苏醒浓度以下,尤其与N2O合用时,苏醒更迅速、平稳。
