三、主要影响
1.对肾功能的影响 低血容量性休克时肾脏血流迅速下降。肾流入量下降导致肾小球滤过压下降至低于滤过至肾小囊所需的压力水平。肾脏的代谢率很高,要维持这一较高的代谢率,肾脏需要较大的血流量。因此,长时间低血压可导致肾小管坏死。
2.对代谢的影响 休克时由于微循环功能障碍,组织细胞获得的氧量减少,无氧糖酵解转换增加,ATP合成减少,组织代谢明显受损,同时乳酸生成增多,产生代谢性酸中毒。可见,影响无氧糖酵解转换的最重要的一个因素为可获得的氧量。
氧输送(oxygen delivery,DO2)、氧消耗(oxygen consumption,VO2)和氧摄取率(oxygen extraction ratio,O2ER)可由如下公式计算。
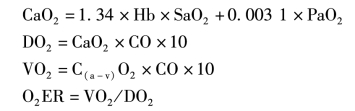
式中:CaO2代表动脉氧含量(单位ml/dl),Hb代表血红蛋白浓度(单位g/dl),SaO2代表动脉氧合血红蛋白浓度(%),PaO2代表动脉血氧分压(mmHg),CO代表心排血量(单位L/min),C(a-v)O2代表动静脉氧含量差(单位ml/dl),DO2、VO2单位ml/min。
公式表明氧输送取决于循环中的氧含量和心排血量。当低容量休克心排血量下降时,氧输送也随之下降,其下降程度不仅取决于心排血量,还取决于血红蛋白下降程度。氧供下降时,大多数器官都增加其从动脉血中的摄氧能力,因此静脉循环中的血氧饱和度相对降低。C(a-v)O2和O2ER增加是低容量性休克的代谢特征。
组织摄氧能力的差异很大。摄氧率一般在0.3左右。在正常情况下,心脏和大脑都最大限度地摄取氧,都依赖于足够的血流量来提供氧。低血容量达到一定低的阈值前,VO2都基本保持恒定不变。当达到这个阈值时,即使增加摄氧也不能满足氧供。
3.对中枢神经系统的影响 休克早期,由于血液重新分布和脑循环的自身调节,交感神经兴奋并不引起脑血管明显收缩,保证了脑的血液供应。随着休克的发展,血压进行性下降,当平均动脉压<50mmHg时,中枢神经系统血流失去自我调控或脑血管内出现DIC,脑组织缺血缺氧,意识很快丧失继之自主功能下降。(https://www.daowen.com)
4.对胃肠道的影响 休克早期腹腔内脏血管收缩,胃肠道血流量大为减少。胃肠道缺血、缺氧、淤血和DIC形成,导致胃肠黏膜变性、坏死、黏膜糜烂,形成应激性溃疡。动物实验显示,胃肠道组织含氧量急剧下降可导致缺血再灌注损伤或肠内细菌易位。
5.对免疫系统的影响 低血容量性休克可以产生一系列炎症反应,从而恶化病情。
(1)循环中的和固定的巨噬细胞的激活可诱导肿瘤坏死因子(tumor necrosis factor,TNF)产生和释放,进一步导致中性粒细胞和凝血系统的激活。中性粒细胞激活后可产生氧自由基、溶酶体酶、白三烯C4与D4。这些炎症介质和细胞因子不仅进一步激活炎症细胞,释放炎症介质和细胞因子,形成恶性循环,还可以破坏血管内皮完整性,导致血管内液向组织间隙渗出。
(2)失血性休克后,黏附分子这一糖蛋白可导致白细胞的动员和迁移。最常涉及的细胞黏附分子包括选择素、整合素及免疫球蛋白。有研究表明,损伤严重程度与可溶性细胞黏附分子(soluble cell adhesion molecules,SCAMs)的释放有关。
(3)氧不完全还原为水时则产生氧自由基,包括超氧阴离子、过氧化氢等,对脂质双层膜结构、细胞内膜、结构蛋白、核酸和糖类都有毒性作用。巨噬细胞通常会产生氧自由基来帮助消灭已消化的物质。从巨噬细胞漏出的抗氧化物质也能保护周围组织。缺血再灌注损伤可以加速炎症细胞产生有毒的氧代谢产物,导致周围组织的进一步破坏,并可能在决定短暂低容量性休克的最终预后的诸多因素中起重要作用。
(4)其他:动物实验还证实了一些低容量性休克引起的重要免疫反应,包括肝内库普弗细胞抗原递呈失败、肠道细菌易位进入体循环。
6.对血液学影响 呕吐、腹泻、烧伤或低蛋白血症产生大量腹腔积液等原因引起的体液丢失所导致的低容量性休克时,血管内血液浓缩,黏滞度增加,易导致微血管内微血栓形成,远端血管床缺血。
7.对凝血-纤溶系统影响 低容量性休克早期,由于“自身输液”作用,血液稀释,血细胞比容降低,血液黏滞度下降。当“自身输液”停止后,血浆外渗到组织间隙,且由于炎症介质或细胞因子的作用,血管内皮损伤,毛细血管通透性增加,加上组织间液亲水性增加,大量血浆和体液组分被封闭和分隔在组织间隙,引起血液浓缩,血细胞比容上升血液黏滞度升高,促进了红细胞聚集,呈现高凝状态,启动DIC的发病过程。
